2006/63/ESSměrnice Komise 2006/63/ES ze dne 14. července 2006 , kterou se mění přílohy II až VII směrnice Rady 98/57/ES o ochraně proti Ralstonia solanacearum (Smith) Yabuuchi et al.
| Publikováno: | Úř. věst. L 206, 27.7.2006, s. 36-106 | Druh předpisu: | Směrnice |
| Přijato: | 14. července 2006 | Autor předpisu: | Evropská komise |
| Platnost od: | 30. července 2006 | Nabývá účinnosti: | 30. července 2006 |
| Platnost předpisu: | Zrušen předpisem (EU) 2016/2031 | Pozbývá platnosti: | 1. ledna 2022 |
Text předpisu s celou hlavičkou je dostupný pouze pro registrované uživatele.
SMĚRNICE KOMISE 2006/63/ES
ze dne 14. července 2006,
kterou se mění přílohy II až VII směrnice Rady 98/57/ES o ochraně proti Ralstonia solanacearum (Smith) Yabuuchi et al.
KOMISE EVROPSKÝCH SPOLEČENSTVÍ,
s ohledem na Smlouvu o založení Evropského společenství,
s ohledem na směrnici Rady 98/57/ES ze dne 20. července 1998 o ochraně proti Ralstonia solanacearum (Smith) Yabuuchi et al. (1), a zejména na článek 11 uvedené směrnice,
vzhledem k těmto důvodům:
|
(1) |
Jedním z významných organismů škodlivých pro brambory a rajčata je Ralstonia solanacearum (Smith) Yabuuchi et al., původce bakteriální hnědé hniloby bramboru a bakteriálního vadnutí bramboru a rajčete (dále jen „organismus“). |
|
(2) |
Organismus se stále vyskytuje v některých částech Společenství. |
|
(3) |
Směrnice 98/57/ES stanovila podrobná opatření, která mají být přijata v členských státech na ochranu proti organismu, aby se zjistilo místo výskytu a stanovil rozsah rozšíření, předešlo se jeho výskytu a rozšíření a při zjištění výskytu se zabránilo jeho rozšíření a prováděla se ochranná opatření za účelem jeho eradikace. |
|
(4) |
Od té doby došlo k významnému pokroku v poznatcích o biologii a v postupech zjišťování a identifikace organismu a kromě toho praktické zkušenosti získané při ochraně proti organismu vyžadují přezkoumání několika technických ustanovení týkajících se ochranných opatření. |
|
(5) |
V důsledku tohoto vývoje se jeví jako nezbytné přezkoumat a aktualizovat opatření obsažená v některých přílohách směrnice 98/57/ES. |
|
(6) |
Pokud jde o postupy zjišťování a identifikace, je zapracována moderní detekční metoda fluorescenční hybridizace (FISH). Rovněž jsou zahrnuta zlepšení metody polymerázové řetězové reakce (PCR) i zlepšení různých technických prvků současných postupů pro zjištění a identifikaci a metody zjišťování a identifikace organismu v jiných hostitelských rostlinách, než je brambor, ve vodě a půdě. |
|
(7) |
Pokud jde o technické prvky ochranných opatření, jsou pro ně vypracovány zlepšené předpisy pro: způsob uchování testovaných vzorků, aby bylo zajištěno vysledování organismu, prvky potřebné ke stanovení rozsahu pravděpodobného zamoření, podrobnosti oznámení každého potvrzeného výskytu organismu a příslušných zamořených oblastí, opatření, která je třeba provést v místech produkce označených jako zamořená a v rámci vymezených oblastí. Kromě toho byly zapracovány některé předpisy pro rajče, s ohledem na význam této rostliny jako hostitelské rostliny organismu. |
|
(8) |
Opatření stanovená touto směrnicí jsou v souladu se stanoviskem Stálého rostlinolékařského výboru. |
PŘIJALA TUTO SMĚRNICI:
Článek 1
Přílohy II až VII směrnice 98/57/ES se nahrazují příslušnými zněními v příloze této směrnice.
Článek 2
1. Členské státy nejpozději do 31. března 2007 přijmou a zveřejní právní a správní předpisy nezbytné pro dosažení souladu s touto směrnicí. Neprodleně oznámí Komisi znění těchto předpisů a srovnávací tabulku mezi těmito předpisy a touto směrnicí.
Tyto předpisy použijí od 1. dubna 2007.
Tyto předpisy přijaté členskými státy musí obsahovat odkaz na tuto směrnici nebo musí být takový odkaz učiněn při jejich úředním vyhlášení. Způsob odkazu si stanoví členské státy.
2. Členské státy neprodleně sdělí Komisi znění hlavních ustanovení vnitrostátních právních předpisů, které přijmou v oblasti působnosti této směrnice.
Článek 3
Tato směrnice vstupuje v platnost třetím dnem po vyhlášení v Úředním věstníku Evropské unie.
Článek 4
Tato směrnice je určena členským státům.
V Bruselu dne 14. července 2006.
Za Komisi
Markos KYPRIANOU
člen Komise
(1) Úř. věst. L 235, 21.8.1998, s. 1.
PŘÍLOHA
PŘÍLOHA II
SCHÉMA TESTU PRO DIAGNÓZU, ZJIŠTĚNÍ A IDENTIFIKACI RALSTONIA SOLANACEARUM (SMITH) YABUUCHI ET AL.
OBLAST PŮSOBNOSTI SCHÉMATU TESTU
Předložené schéma popisuje různé postupy, které se týkají:
|
i) |
diagnózy hnědé hniloby v hlízách bramboru a bakteriálního vadnutí bramboru, rajčete a některých dalších hostitelských rostlin, |
|
ii) |
zjištění Ralstonia solanacearum ve vzorcích hlíz bramboru, hostitelských rostlin bramboru, hostitelských rostlin rajčete a jiných hostitelských rostlin, vody a půdy, |
|
iii) |
identifikace Ralstonia solanacearum (R. solanacearum). |
OBSAH
|
|
|
Strany |
||||
|
|
Obecné principy |
40 |
||||
|
ODDÍL I: |
Použití postupového diagramu |
40 |
||||
|
|
1. |
Detekční schéma pro zjištění hnědé hniloby a bakteriálního vadnutí (R. solanacearum) v hlízách bramboru a rostlinách bramboru, rajčete nebo v jiných hostitelských rostlinách vykazujících příznaky hnědé hniloby nebo bakteriálního vadnutí. |
40 |
|||
|
|
2. |
Schéma pro zjištění a identifikaci R. solanacearum ve vzorcích hlíz bramboru nevykazujících příznaky. |
43 |
|||
|
|
3. |
Schéma pro zjištění a identifikaci R. solanacearum ve vzorcích rostlin bramboru, rajčete nebo jiných hostitelských rostlin nevykazujících příznaky. |
46 |
|||
|
ODDÍL II: |
Podrobné metody pro zjištění R. solanacearum v hlízách bramboru a v rostlinách bramboru, rajčete nebo jiných hostitelských rostlinách vykazujících příznaky hnědé hniloby nebo bakteriálního vadnutí |
48 |
||||
|
|
1. |
Příznaky |
48 |
|||
|
|
2. |
Rychlé screeningové testy |
48 |
|||
|
|
3. |
Postup při izolaci |
49 |
|||
|
|
4. |
Identifikační testy R. solanacearum |
49 |
|||
|
ODDÍL III: |
1. |
Podrobné metody pro zjištění a identifikaci R. solanacearum ve vzorcích hlíz bramboru nevykazujících příznaky |
49 |
|||
|
|
|
1.1 |
Příprava vzorků |
49 |
||
|
|
|
1.2 |
Testování |
51 |
||
|
|
2. |
Podrobné metody pro zjištění a identifikaci R. solanacearum ve vzorcích rostlin bramboru, rajčete nebo jiných hostitelských rostlin nevykazujících příznaky |
51 |
|||
|
|
|
2.1 |
Příprava vzorků |
51 |
||
|
|
|
2.2 |
Testování |
52 |
||
|
ODDÍL IV: |
1. |
Schéma pro zjištění a identifikaci R. solanacearum ve vodě |
53 |
|||
|
|
2. |
Metody pro zjištění a identifikaci R. solanacearum ve vodě |
55 |
|||
|
|
|
2.1 |
Příprava vzorků |
55 |
||
|
|
|
2.2 |
Testování |
55 |
||
|
ODDÍL V: |
1. |
Schéma pro zjištění a identifikaci R. solanacearum v půdě |
56 |
|||
|
|
2. |
Metody pro zjištění a identifikaci R. solanacearum v půdě |
58 |
|||
|
|
|
2.1 |
Příprava vzorků |
58 |
||
|
|
|
2.2 |
Testování |
58 |
||
|
ODDÍL VI: |
Optimalizované protokoly pro zjištění a identifikaci R. solanacearum |
58 |
||||
|
|
A. |
Diagnostické a detekční testy |
58 |
|||
|
|
|
1. |
Test výronu ze stonku |
58 |
||
|
|
|
2. |
Detekce granulí poly-β-hydroxybutyrátu (PHB) |
58 |
||
|
|
|
3. |
Sérologické aglutinační testy |
59 |
||
|
|
|
4. |
Selektivní izolace |
60 |
||
|
|
|
|
4.1 |
Očkování na živné půdy |
60 |
|
|
|
|
|
4.2 |
Postup obohacování |
60 |
|
|
|
|
5. |
Imunofluorescenční test (IF test) |
61 |
||
|
|
|
6. |
Test polymerázové řetězové reakce (PCR test) |
64 |
||
|
|
|
|
6.1 |
Metody purifikace DNA |
65 |
|
|
|
|
|
|
a) |
Metoda podle Pastrika (2000) |
65 |
|
|
|
|
|
b) |
Jiné metody |
65 |
|
|
|
|
6.2 |
Polymerázová řetězová reakce |
66 |
|
|
|
|
|
6.3 |
Analýza produktu PCR |
66 |
|
|
|
|
7. |
Test fluorescenční hybridizace in situ (FISH test) |
67 |
||
|
|
|
8. |
Testy enzymové imunoanalýzy ELISA |
69 |
||
|
|
|
|
a) |
Nepřímé testy ELISA |
69 |
|
|
|
|
|
b) |
DASI ELISA (sendvičová enzymová imunoanalýza ELISA) |
70 |
|
|
|
|
9. |
Biotest |
71 |
||
|
|
B. |
Identifikační testy |
72 |
|||
|
|
|
1. |
Nutriční a enzymatický identifikační test |
72 |
||
|
|
|
2. |
Test IF |
72 |
||
|
|
|
3. |
Test ELISA |
73 |
||
|
|
|
4. |
Test PCR |
73 |
||
|
|
|
5. |
Test FISH |
73 |
||
|
|
|
6. |
Analýza mastných kyselin (FAP) |
73 |
||
|
|
|
7. |
Metoda charakteristiky kmene |
73 |
||
|
|
|
|
7.1 |
Stanovení biovaru |
73 |
|
|
|
|
|
7.2 |
Genomická variabilita |
74 |
|
|
|
|
|
7.3 |
Metody PCR |
74 |
|
|
|
C. |
Konfirmační test |
74 |
|||
|
|
|
Dodatek 1 |
Laboratoře podílející se na optimalizaci a validaci protokolů |
76 |
||
|
|
|
Dodatek 2 |
Živné půdy pro izolaci a pěstování R. solanacearum |
77 |
||
|
|
|
Dodatek 3 |
A) |
Komerčně dostupný standardizovaný kontrolní materiál |
79 |
|
|
|
|
|
B) |
Příprava kontrol |
80 |
|
|
|
|
Dodatek 4 |
Pufry pro testovací postupy |
82 |
||
|
|
|
Dodatek 5 |
Stanovení úrovně kontaminace při testech IF a FISH |
85 |
||
|
|
|
Dodatek 6 |
Validované protokoly a činidla PCR |
86 |
||
|
|
|
Dodatek 7 |
Validovaná činidla pro test FISH |
91 |
||
|
|
|
Dodatek 8 |
Pěstitelské podmínky rajčete a lilku |
93 |
||
|
|
|
Literatura |
|
94 |
||
OBECNÉ PRINCIPY
Optimalizované protokoly pro různé metody, schválená činidla a podrobnosti pro přípravu testovaných a kontrolních materiálů jsou uvedeny v dodatcích. Seznam laboratoří, které se podílely na optimalizaci a validaci protokolů, je v dodatku 1.
Protože protokoly obsahují zjištění karanténního organismu a budou zahrnovat použití životaschopných kultur R. solanacearum jako kontrolních materiálů, bude nutné provádět postupy za vhodných karanténních podmínek s odpovídajícím zařízením na odstraňování odpadu a za podmínek příslušných povolení vydaných úředními orgány pro karanténu rostlin.
Testovací parametry musí zajišťovat stálé a reprodukovatelné zjištění úrovní R. solanacearum jako stanovené prahy vybraných metod.
Zcela nezbytná je přesná příprava pozitivních kontrol.
Testování podle požadovaných prahů také zahrnuje správné nastavení, údržbu a kalibraci zařízení, pečlivé zacházení s činidly a jejich uchovávání a všechna opatření pro zamezení kontaminace mezi vzorky, např. oddělení pozitivních kontrol od testovaných vzorků. Musí být uplatněno standardní řízení kvality, aby se zabránilo administrativním a jiným chybám, zvláště při označování a v dokumentaci.
Podezření z výskytu, jak je uvedeno v čl. 4 odst. 2 směrnice 98/57/ES, naznačuje pozitivní výsledek z diagnostických nebo screeningových testů provedených na vzorku, jak je znázorněno v níže uvedených postupových diagramech. První pozitivní screeningový test (test IF, PCR/FISH, selektivní izolace) musí být potvrzen druhým screeningovým testem založeném na jiném biologickém principu.
Pokud je první screeningový test pozitivní, existuje podezření na infekci R. solanacearum a musí být proveden druhý screeningový test. Pokud je i druhý screeningový test pozitivní, pak je podezření potvrzeno (podezření z výskytu) a musí se pokračovat v testování podle daného schématu. Jestliže je druhý screeningový test negativní, pak vzorek není považován za infikovaný R. solanacearum.
Potvrzená přítomnost podle čl. 5 odst. 1 směrnice 98/57/ES vyžaduje izolaci a identifikaci čisté kultury R. solanacearum s potvrzením patogenity.
ODDÍL I
POUŽITÍ POSTUPOVÉHO DIAGRAMU
1. Detekční schéma pro diagnózu hnědé hniloby a bakteriálního vadnutí (Ralstonia solanacearum) hlíz bramboru a rostlin bramboru, rajčete a jiných hostitelských rostlin vykazujících příznaky hnědé hniloby nebo bakteriálního vadnutí
Postup testování je určen pro hlízy a rostliny bramboru s podezřením z výskytu nebo typickými příznaky hnědé hniloby nebo bakteriálního vadnutí. Zahrnuje rychlý screeningový test, izolaci patogena z infikovaného vodivého pletiva na selektivní živné půdě a v případě pozitivního výsledku identifikaci kultury Ralstonia solanacearum.
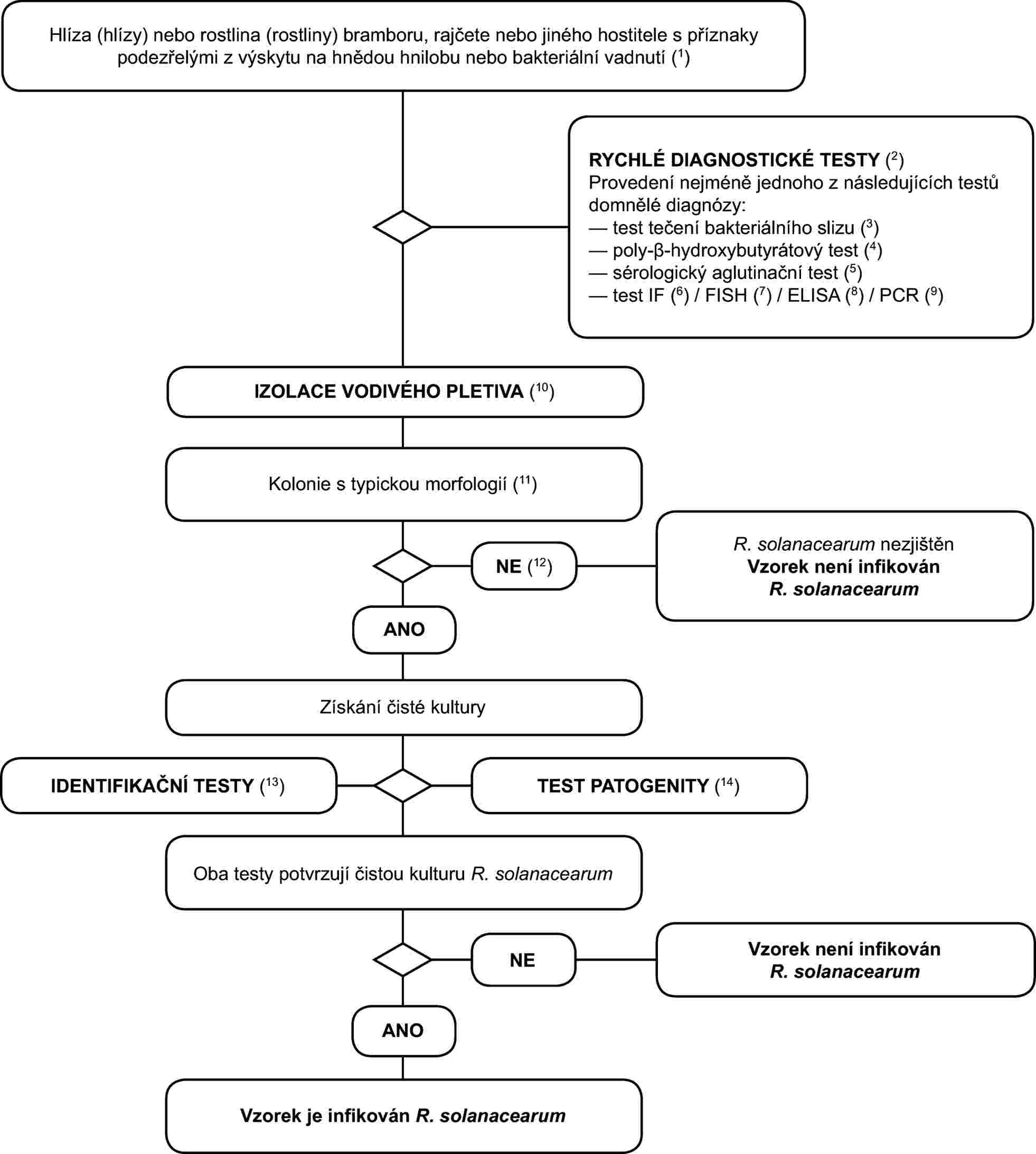

2. Schéma pro zjištění a identifikaci Ralstonia solanacearum ve vzorcích hlíz bramboru nevykazujících příznaky
Princip
Postup testování je určen ke zjištění latentních infekcí v hlízách bramboru. Pozitivní výsledek alespoň ze dvou screeningových testů (viz poznámka v diagramu 3), z nichž každý je založen na jiném biologickém principu, musí být doplněn izolací patogenu a dále, v případě izolace typických kolonií, potvrzením, že čistá kultura je R. solanacearum. Pozitivní výsledek pouze z jednoho screeningového testu není dostačující k tomu, aby byl vzorek považován za podezřelý.
Screeningové testy a izolační testy musí umožnit detekční práh 103 až 104 buněk/ml resuspendované pelety zahrnutý jako pozitivní kontroly v každé sérii testů.
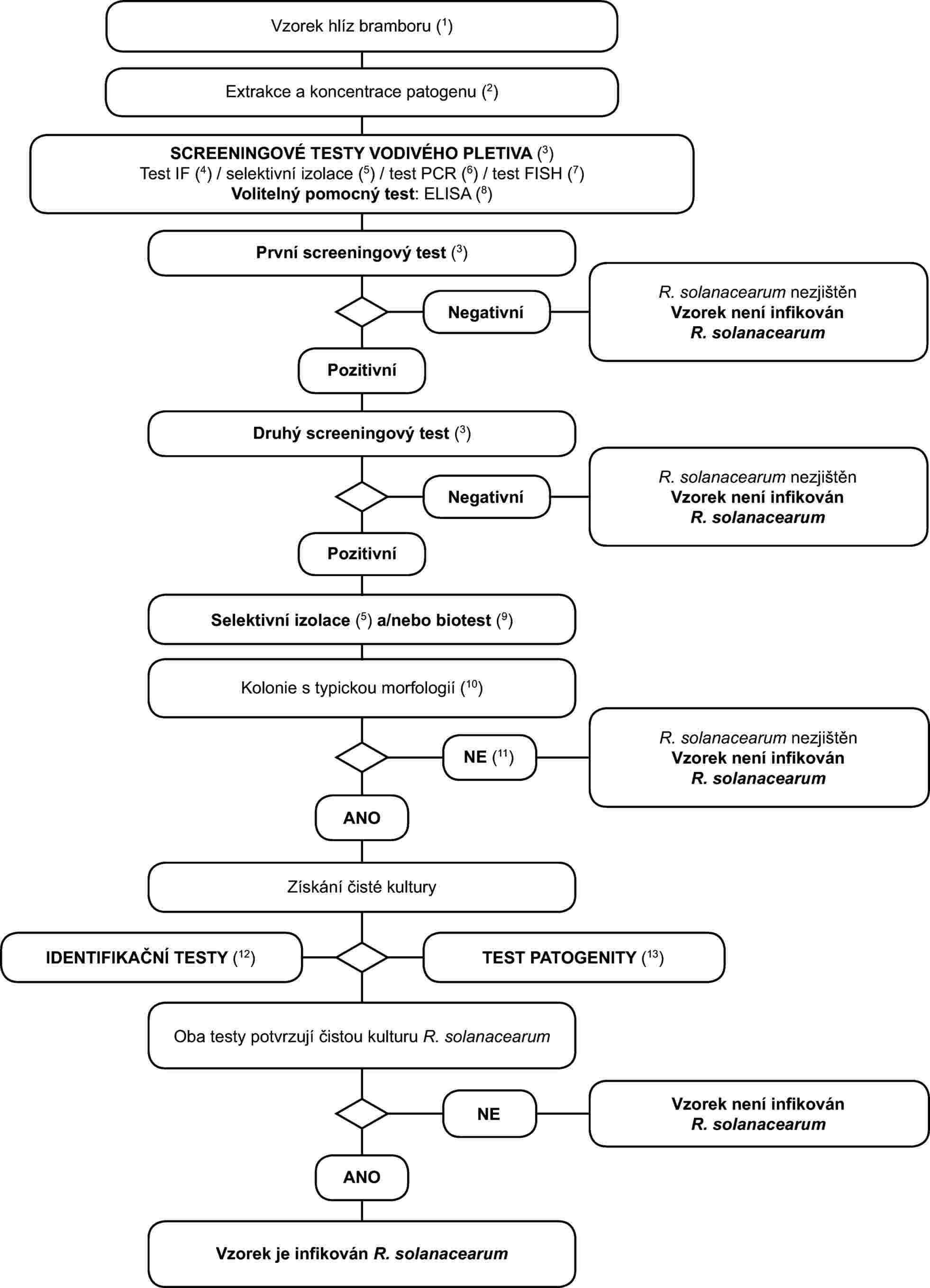

3. Schéma pro zjištění a identifikaci Ralstonia solanacearum ve vzorcích rostlin bramboru nevykazujících příznaky, rostlin rajčete nevykazujících příznaky nebo rostlin jiných hostitelských rostlin nevykazujících příznaky
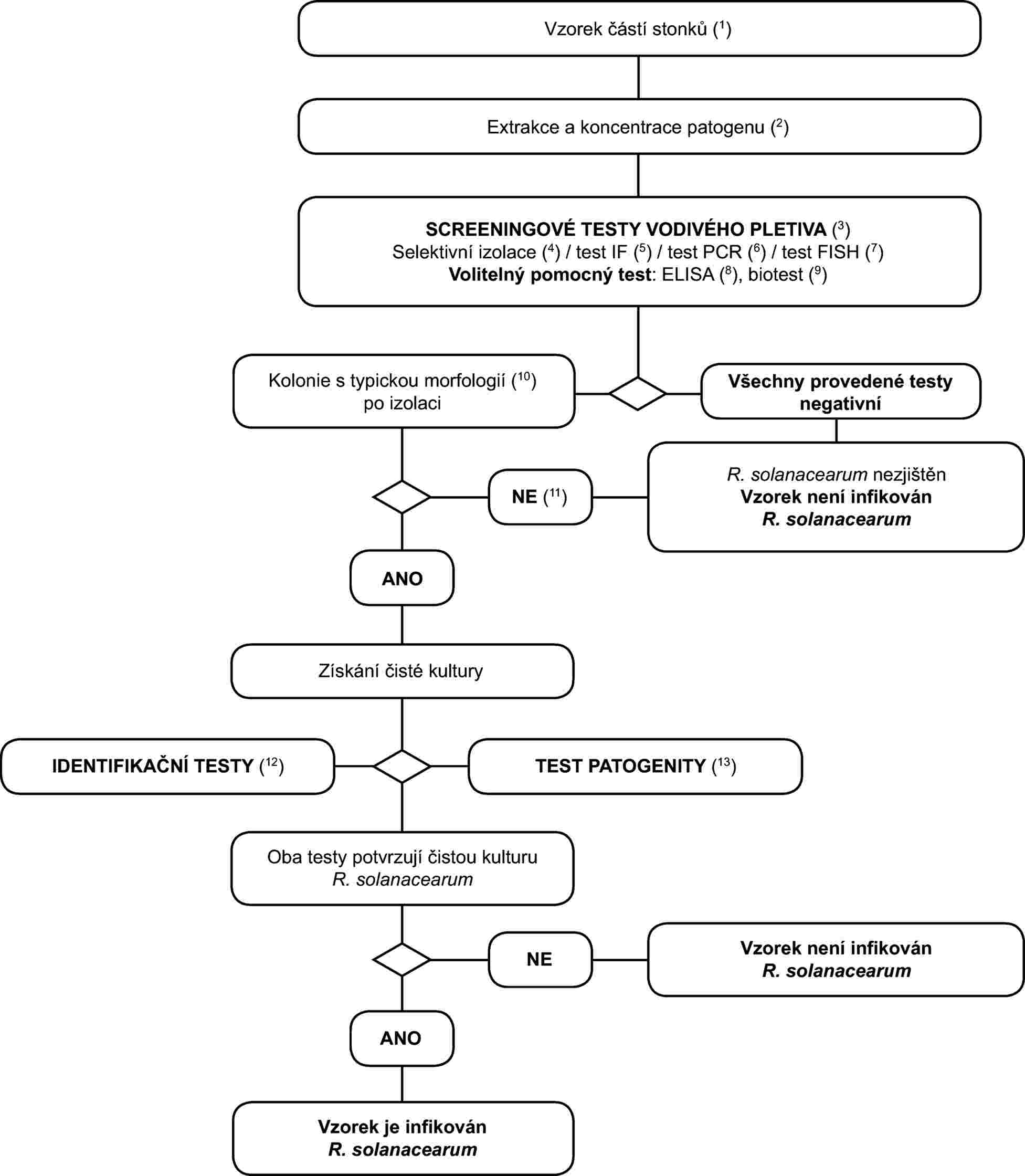

ODDÍL II
PODROBNÉ METODY PRO ZJIŠTĚNÍ RALSTONIA SOLANACEARUM V HLÍZÁCH BRAMBORU A V ROSTLINÁCH BRAMBORU, RAJČETE NEBO JINÝCH HOSTITELSKÝCH ROSTLINÁCH S PŘÍZNAKY HNĚDÉ HNILOBY NEBO BAKTERIÁLNÍHO VADNUTÍ
1. Příznaky (viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main)
1.1 Příznaky u bramboru
Rostlina bramboru. Raná fáze infekce v polních podmínkách se rozpozná vadnutím listů směrem k vrcholu rostliny při vysokých teplotách během dne, přičemž v noci dochází k zotavení. V raných fázích vadnutí zůstávají listy zelené, ale později žloutnou a objevují se hnědé nekrózy. Dochází také k ohýbání listů dolů. Vadnutí jednoho výhonku nebo celé rostliny se rychle stává nevratným a končí kolapsem a uhynutím rostliny. Z cévních svazků napříč uříznutých stonků zvadlých rostlin obvykle vytéká hnědý a mléčný bakteriální sliz nebo je možné sliz vymáčknout. Při ponoření uříznutého stonku svisle do vody se z cévních svazků táhnou vlákna slizu.
Hlíza bramboru. Hlízy bramboru je třeba překrojit napříč u pupkového konce a podélně přes pupkový konec. V rané fázi se infekce pozná podle lahvově žlutého až světle hnědého zabarvení cévního prstence, ze kterého po několika minutách začne prýštit bledý krémový bakteriální sliz. Později se cévní zbarvení stává výrazněji hnědým a odumření se může rozšířit do parenchymatického pletiva. V pokročilejších fázích se infekce rozšíří vně od pupkového konce hlízy a z oček může vytékat bakteriální sliz a způsobuje přilepení částic půdy. Na slupce se mohou objevit červenohnědá, lehce propadlá postižená místa, způsobená vnitřním kolapsem cévního pletiva. V pokročilejších fázích infekce je obvyklý sekundární rozvoj měkkých hnilob bakteriálního a houbového původu.
1.2 Příznaky u rajčete
Rostlina rajčete. Prvním viditelným příznakem je povadlý vzhled nejmladších listů. Za příznivých podmínek pro patogena (teplota půdy kolem 25 °C, při nasycené vzdušné vlhkosti) se během několika málo dní rozvine kroucení listů směrem dolů a vadnutí na jedné straně rostliny nebo celé rostliny, které končí jejím úplným odumřením. Za méně příznivých podmínek pro patogena (teplota půdy méně než 21 °C) rostlina tolik nevadne, ale na stonku se může tvořit větší počet postranních výhonů. Je možné pozorovat vodou nasáklé pruhy od spodu stonku, které jsou dokladem odumírání cévního systému. Při příčném řezu stonkem vylučují hnědě zbarvená vodivá pletiva bílý nebo nažloutlý bakteriální sliz.
1.3 Příznaky u jiných hostitelů
Rostliny Solanum dulcamara a S. nigrum. Za normálních podmínek jsou u těchto plevelných hostitelských rostlin zřídkakdy pozorovány příznaky vadnutí, pokud teploty půdy nepřevyšují 25 °C nebo není extrémně vysoká koncentrace inokula (např. u rostliny S. nigrum rostoucí u nemocné rostliny bramboru nebo rajčete). Při vadnutí jsou příznaky stejné jako u rostliny rajčete. Nevadnoucí rostliny S. dulcamara, která má stonky a kořeny ve vodě, mohou vykazovat vnitřní světle hnědé zbarvení vodivých pletiv na příčném řezu spodní části stonku nebo částí stonku pod vodou. Z řezu cévních svazků mohou vytékat bakterie nebo mohou tvořit vlákna slizu, jestliže je řez stonku ponořen svisle do vody, a to i při absenci příznaků vadnutí.
2. Rychlé screeningové testy
Rychlé screeningové testy mohou napomoci předběžné diagnóze, ale nejsou dostačující. Použijte jeden nebo více následujících platných testů:
2.1 Test na výtok slizu ze stonku
(Viz oddíl VI.A.1)
2.2 Test na přítomnost granulí poly-β-hydroxybutyrátu (PHB)
Charakteristické granule PHB v buňkách R. solanacearum jsou zviditelněny obarvením tepelně fixovaných skvrn bakteriálního slizu z infikovaného pletiva na mikroskopickém sklíčku nilskou modří A nebo súdánskou černí (Viz oddíl VI.A.2).
2.3 Sérologické aglutinační testy
(Viz oddíl VI.A.3)
2.4 Jiné testy
Dalšími vhodnými rychlými screeningovými testy jsou test IF (viz oddíl VI.A.5), test FISH (viz oddíl VI.A.7), testy ELISA (viz oddíl VI.A.8) a testy PCR (viz oddíl VI.A.6).
3. Postup při izolaci
|
a) |
Odeberte sliz nebo vrstvu zbarveného pletiva z cévního prstence hlízy bramboru nebo z cévních vláken stonku rostliny bramboru, rajčete nebo jiné vadnoucí hostitelské rostliny. Suspendujte je v malém množství sterilní destilované vody nebo 50mM fosfátového pufru (dodatek 4) a nechte 5–10 minut stát. |
|
b) |
Připravte řadu desetinásobných ředění suspenze. |
|
c) |
Přeneste 50–100 µl suspenze a roztoku na universální živnou půdu (NA, YPGA nebo SPA; viz dodatek 2) a/nebo Kelmanovo tetrazolové médium (dodatek 2) a/nebo validované selektivní médium (např. SMSA, viz dodatek 2). Rozetřete metodou zřeďovacích roztěrů. Připravte případně samostatné misky s rozředěnou buněčnou suspenzí R. solanacearum biovar 2 k pozitivní kontrole. |
|
d) |
Nechte inkubovat 2–6 dní při teplotě 28 °C.
|
4. Identifikační testy Ralstonia solanacearum
Testy potvrzující výskyt R. solanacearum v podezřelých izolátech jsou popsány v bodu VI.B.
ODDÍL III
1. Podrobné metody pro zjištění a identifikaci Ralstonia solanacearum ve vzorcích bezpříznakových hlíz bramboru
1.1 Příprava vzorků
Poznámka:
|
— |
Standardní velikost vzorku je 200 hlíz na jeden test. Intenzivnější vzorkování vyžaduje více testů na vzorcích této velikosti. Větší množství hlíz ve vzorku vedou k zpomalení nebo složitějšímu výkladu výsledků. Postup lze vhodně použít i pro vzorky s méně než 200 hlízami, pokud je k dispozici menší množství hlíz |
|
— |
Validace všech níže uvedených zjišťovacích metod je založená na testování vzorků o velikosti 200 hlíz. |
|
— |
Extrakt bramboru popsaný níže může být rovněž použit pro zjištění původce bakteriální kroužkovitosti bramboru, Clavibacter michiganensis subsp. sepedonicus. |
Nepovinné ošetření před přípravou vzorku:
|
a) |
Inkubace vzorků při teplotě 2–30 °C po dobu až 2 týdnů před testováním na podporu množení všech populací R. solanacearum. |
|
b) |
Omyjte hlízy. Použijte vhodné desinfekční prostředky (s obsahem chlóru, jestliže má být proveden PCR test, pro odstranění patogenní DNA) a mycí prostředky mezi každým vzorkem. Nechte hlízy oschnout na vzduchu. Tento postup mytí je vhodný (není však vyžadován) zvláště v případě, když je ve vzorcích příliš zeminy nebo jestliže má být proveden test PCR nebo přímá izolace. |
1.1.1 Pomocí čistého a dezinfikovaného skalpelu nebo nože na zeleninu odstraňte slupku na pupkovém konci každé hlízy, tak aby bylo viditelné vodivé pletivo. Opatrně vyřízněte malé výkrojky vodivých pletiv na pupkovém konci a množství pletiva nezahrnující cévní svazky omezte na minimum (viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main).
Pozn.: Dejte stranou všechny (hnijící) hlízy s podezřelými příznaky hnědé hniloby a testujte je odděleně.
Pokud jsou při vyříznutí výkrojku zjištěny příznaky podezření na hnědou hnilobu, mělo by být provedeno vizuální vyšetření takové hlízy na řezu hlízy na pupkovém konci Všechny naříznuté hlízy s podezřelými příznaky by se měly uchovávat po dobu nejméně 2 dnů při pokojové teplotě, aby mohlo dojít ke zkorkovatění (suberizaci) a potom by měly být hlízy uchovány v chladu (4–10 °C) za řádných karanténních podmínek. Všechny hlízy včetně hlíz s podezřelými příznaky by měly být uchovány podle přílohy III.
1.1.2 Uložte výkrojky z pupkové části do nepoužitých nádob na jedno použití, které jsou uzavíratelné a/nebo utěsnitelné (v případě, že nádoby jsou znovu používány, musí být důkladně vyčištěny a dezinfikovány prostředky s obsahem chlóru). Nejlépe je zpracovat výkrojky z pupkového konce okamžitě. Není-li to možné, uchovávejte je v nádobě bez přidání pufru; v chladu nejdéle 72 hodin nebo při pokojové teplotě nejdéle 24 hodin.
Výkrojky z pupkových konců zpracujte jedním z následujících postupů:
|
a) |
Buďto zalijte výkrojky dostatečným množstvím (přibližně 40 ml) extrakčního pufru (dodatek 4) a třepejte v rotační třepačce (50–100 ot./min) 4 hodiny při teplotě nižší než 24 °C nebo 16–24 hodin chlazené, nebo |
|
b) |
homogenizujte výkrojky dostatečným množstvím (přibližně 40 ml) extrakčního pufru (dodatek 4) buď v mixéru (např. Waring nebo Ultra Thurax) nebo drcením v utěsněném maceračním sáčku na jedno použití (např. silný polyethylenový sáček Stomacher nebo Bioreba, 150 mm × 250 mm, sterilovaný zářením) pomocí gumového tloučku nebo vhodného mlecího zařízení (např. Homex). |
Pozn.: Při homogenizaci vzorků pomocí mixéru existuje vysoké nebezpečí křížové kontaminace vzorků. Učiňte bezpečnostní opatření pro zamezení vzniku aerosolu nebo rozlití během extrakčního procesu. Zajistěte, abyste pro každý vzorek použili čerstvě sterilované nože (ostří) a nádoby. Při testu PCR zabraňte přenosu DNA na nádobách nebo v mlecím přístroji. U testu PCR se doporučuje použít drcení v sáčcích na jedno použití a použití zkumavek na jedno použití.
1.1.3 Dekantujte supernatant. Je-li příliš zakalený, pročistěte buď pomalým odstřeďováním (nejvýš 180 g po dobu 10 minut při teplotě 4–10 °C) nebo vakuovou filtrací (40–100 µm), filtr omyjte přídavkem (~10 ml) extrakčního pufru.
1.1.4 Zahustěte bakteriální frakci odstřeďováním, 7 000 g po dobu 15 minut (nebo 10 000 g po dobu 10 minut) při teplotě 4–10 °C a odstraňte supernatant, aniž by se rozvířila peleta.
1.1.5 Resuspendujte peletu v 1,5 ml peletového pufru (dodatek 4). Použijte 500 µl pro R. solanacearum, 500 µl pro Clavibacter michiganensis subsp. sepedonicus a 500 µl pro referenční účely. Přidejte sterilní glycerol na konečnou koncentraci 10–25 % (v/v) k 500 µl referenční poměrné části a ke zbývající ke zbývající části vzorku, promíchejte vířením a uložte při teplotě –16 až –24 °C (týdny) nebo –68 až –86 °C (měsíce). Extrakty uchovejte během testování při teplotě 4–10 °C.
Opakované zmrazení a rozmrazení se nedoporučuje.
Je-li nutná přeprava extraktu, zajistěte přepravu v chladícím boxu s doručením do 24 až 48 hodin.
1.1.6 Je nezbytně nutné, aby všechny pozitivní kontroly a vzorky R. solanacearum byly uchovány a zpracovány odděleně, aby se zabránilo vzájemné kontaminaci. To platí pro sklíčka IF a všechny testy.
1.2 Testování
Postupové diagramy a popisy testů a optimalizovaných protokolů najdete v příslušných dodatcích:
|
|
Selektivní izolace (viz oddíl VI.A.4) |
|
|
IF test (viz oddíl VI.A.5) |
|
|
Testy PCR (viz oddíl VI.A.6) |
|
|
Test FISH (viz oddíl VI.A.7) |
|
|
Testy ELISA (viz oddíl VI.A.8) |
|
|
Biotest (viz oddíl VI.A.9) |
2. Podrobné metody pro zjištění a identifikaci R. solanacearum ve vzorcích bezpříznakových rostlin bramboru, rajčete nebo jiných hostitelských rostlin
2.1 Příprava vzorků
Pozn.: Pro účely detekce latentních populací R. solanacearum se doporučuje testovat smíšené vzorky. Postup lze vhodně použít na smíšené vzorky o počtu až 200 stonkových částí. Provádí-li se průzkum, měl by být založen na statisticky reprezentativním vzorku zkoumané rostlinné populace.
2.1.1 Do uzavřené sterilní nádoby uložte 1–2 cm dlouhé kousky stonků podle následujícího postupu vzorkování:
Rajčatová sazenice z předpěstírny: čistým dezinfikovaným nožem odeberte kousek dlouhý 1 cm z paty každého stonku hned nad úrovní země.
Rostliny z pole nebo skleníku: čistým dezinfikovaným nožem odeberte nejspodnější postranní výhonek z každé rostliny uříznutým hned nad spojením s hlavním stonkem. Odeberte nejspodnější, 1 cm dlouhý díl z každého výhonku.
Jiné hostitelské rostliny: Čistým dezinfikovaným nožem nebo zahradnickými nůžkami odeberte 1 cm dlouhý díl z paty každého stonku hned nad úrovní země. U lilku potměchuti (S. dulcamara) nebo jiných hostitelských rostlin rostoucích ve vodě odeberte 1–2 cm díly ze stonku pod vodou nebo oddenků s vodními kořeny.
Při vzorkování určité oblasti se doporučuje testovat statisticky representativní vzorek o počtu nejméně 10 rostlin na 1 vzorkovací místo pro každou potenciální plevelnou hostitelskou rostlinu. Detekce patogenu bude nejspolehlivější v období pozdního jara, léta a podzimu, ačkoli přirozenou infekci je možné zjistit po celý rok u víceleté Solanum dulcamara rostoucí ve vodních tocích. Mezi známé hostitelské rostliny patří plevelné rostliny bramboru, Solanum dulcamara, S. nigrum, Datura stramonium a další zástupci čeledi Solanaceae. Dalšími hostitelskými rostlinami jsou rostliny rodu Pelargonium spp. a Portulaca oleracea. Některé evropské plevelné druhy, které mohou hostit populace R. solanacearum biovar 2/Race 3 v kořenech a/nebo oddencích za specifických podmínek, zahrnují Atriplex hastata, Bidens pilosa, Cerastium glomeratum, Chenopodium album, Eupatorium cannabinum, Galinsoga parviflora, Ranunculus scleratus, Rorippa spp, Rumex spp., Silene alba, S. nutans., Tussilago farfarra a Urtica dioica.
Pozn: V této fázi je možné provést vizuální šetření vnitřních příznaků (zbarvení cév nebo bakteriální sliz). Dejte stranou jakýkoli díl stonku s příznaky a testujte odděleně (viz oddíl II).
2.1.2 Krátce dezinfikujte části stonku 70 % etanolem a ihned vysušte savým papírem. Potom zpracujte části stonku jedním z následujících postupů:
|
a) |
Buďto zalijte části dostatečným množstvím (přibližně 40 ml) extrakčního pufru (dodatek 4) a třepejte na rotační třepačce (50–100 ot./min) 4 hodiny při teplotě do 24 °C nebo 16–24 hodin chlazené, nebo |
|
b) |
ihned zpracujte drcením částí v pevném maceračním sáčku (např. Stomacher nebo Bioreba) s přiměřeným množstvím extrakčního pufru (dodatek 4) pomocí gumového tloučku nebo vhodného mlecího zařízení (např. Homex). Není-li to možné, uložte části stonků v chladu nejdéle na 72 hodin nebo při pokojové teplotě na 24 hodin. |
2.1.3 Po usazení, které má trvat 15 minut, dekantujte supernatant.
2.1.4 Další pročišťování extraktu nebo zahušťování bakteriální frakce obvykle není třeba, ale lze jej provést filtrací a/nebo odstřeďováním popsaném v oddíle III. 1.1.3 až 1.1.5.
2.1.5 Rozdělte čistý nebo koncentrovaný vzorkový extrakt na dva stejné díly. Jeden díl testujte při teplotě 4–10 °C a druhý díl skladujete v 10–25 % (v/v) sterilním glycerolu při teplotě –16 až –24 °C (týdny) nebo –68 až –86 °C (měsíce) pro případné další testování.
2.2 Testování
Postupové diagramy a popisy testů a optimalizovaných protokolů najdete v příslušných dodatcích:
|
|
Selektivní izolace (viz oddíl VI.A.4) |
|
|
Test IF (viz oddíl VI.A.5) |
|
|
Testy PCR (viz oddíl VI.A.6) |
|
|
Test FISH (viz oddíl VI.A.7) |
|
|
Testy ELISA (viz oddíl VI.A.8) |
|
|
Biotest (viz oddíl VI.A.9) |
ODDÍL IV
1. Schéma pro zjištění a identifikaci R. solanacearum ve vodě
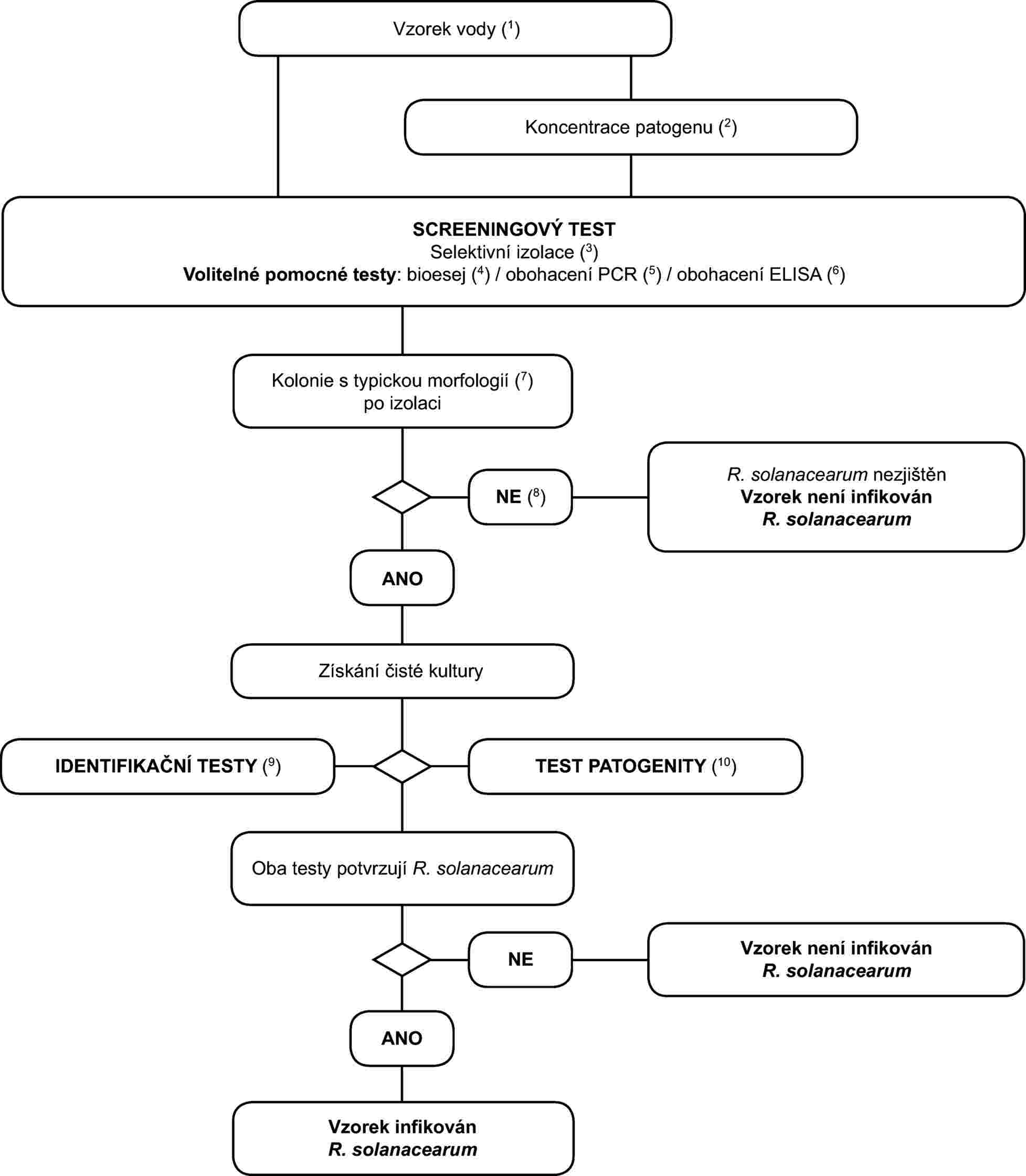

2. Metody detekce a identifikace R. solanacearum ve vodě
Princip
Validované schéma detekce popsané v tomto oddíle je použitelné k detekci patogenu ve vzorcích povrchové vody a rovněž může být použito k testování vzorků odpadní vody ze zpracování brambor a odpadní vody. Je však nutné zmínit, že očekávaná citlivost detekce se liší v závislosti na substrátu. Citlivost testu selektivní izolace je ovlivňována populacemi konkurenčních saprofytických bakterií, kterých je obecně mnohem více v odpadní vodě ze zpracování brambor a odpadní vodě než v povrchové vodě. Zatímco níže uvedené schéma předpokládá detekci asi 103 buněk/litr povrchové vody, citlivost detekce v odpadní vodě ze zpracování brambor a odpadní vodě bude pravděpodobně podstatně nižší. Z tohoto důvodu se doporučuje testovat odpadní vodu po provedení nějakého čistícího postupu (např. sedimentace nebo filtrace), při nichž dojde ke snížení saprofytických bakteriálních populací. Omezení citlivosti testovacího schématu by mělo být bráno v úvahu při hodnocení spolehlivosti v případě získání negativních výsledků. Vzhledem k tomu, že se toto schéma používá úspěšně k mapování výskytu nebo nepřítomnosti patogenu v povrchové vodě, je třeba si uvědomit jeho omezení při použití k podobnému mapování v odpadní vodě ze zpracování brambor a v odpadní vodě.
2.1 Příprava vzorků
Pozn.:
|
— |
Zjištění R. solanacearum v povrchové vodě je nejspolehlivější v období pozdního jara, léta a podzimu, kdy teplota vody překračuje 15 °C. |
|
— |
Opakované vzorkování v různé době během výše uvedených období na určených vzorkovacích místech zvýší spolehlivost zjištění snížením vlivů výkyvů povětrnostních podmínek. |
|
— |
Vezměte v úvahu účinky silných dešťů a geografii vodního toku, abyste se vyhnuli značnému zředění, které by mohlo výskyt patogenu zastřít. |
|
— |
Odeberte vzorky vody v blízkosti hostitelských rostlin, pokud jsou přítomny. |
2.1.1 Na vybraných vzorkovacích místech odeberte vzorky vody do sterilních zkumavek nebo lahviček na jedno použití, pokud možno 30 cm pod hladinou a 2 m od břehu. Při vzorkování odpadní vody ze zpracování a odpadní vody odeberte vzorky z místa výtoku odpadní vody. Doporučená velikost vzorku je 500 ml. Je-li upřednostňována menší velikost, doporučuje se odebrat vzorky nejméně 3krát pro každé vzorkovací místo, z nichž každý bude obsahovat 2 opakované dílčí vzorky o velikosti nejméně 30 ml. Při intenzivním mapování vyberte nejméně 3 vzorkovací místa na každé 3 km vodního toku a zajistěte, že přítoky jsou rovněž podrobeny vzorkování.
2.1.2 Vzorky přepravujte v chladu a temnu (4–10 °C) a testujte do 24 hodin.
2.1.3 Je-li potřeba, může být provedena koncentrace bakteriální frakce pomocí následujících metod:
|
a) |
Odstřeďujte 30–50 ml dílčí vzorky při 10 000 g po dobu 10 minut (nebo 7 000 g po dobu 15 minut), pokud možno při teplotě 4–10 °C, slijte kapalinu nad usazeninou a resuspendujte peletu v 1 ml pufru (dodatek 4). |
|
b) |
Proveďte filtraci přes membránu (minimální velikost pórů 0,45 µm) s následným promytím filtru v 5–10 ml peletového pufru a zachycením filtrátu. Tato metoda je vhodná pro velké objemy vody, které obsahují malý počet saprofytů. |
Koncentrace se obvykle nedoporučuje u vzorků vody ze zpracování brambor nebo u vzorků odpadní vody, protože zvýšená populace konkurenčních saprofytických bakterií inhibuje detekci Ralstonia solanacearum.
2.2 Testování
Viz postupový diagram a popis testů v příslušných dodatcích.
ODDÍL V
1. Schéma pro zjištění a identifikaci R. solanacearum v půdě
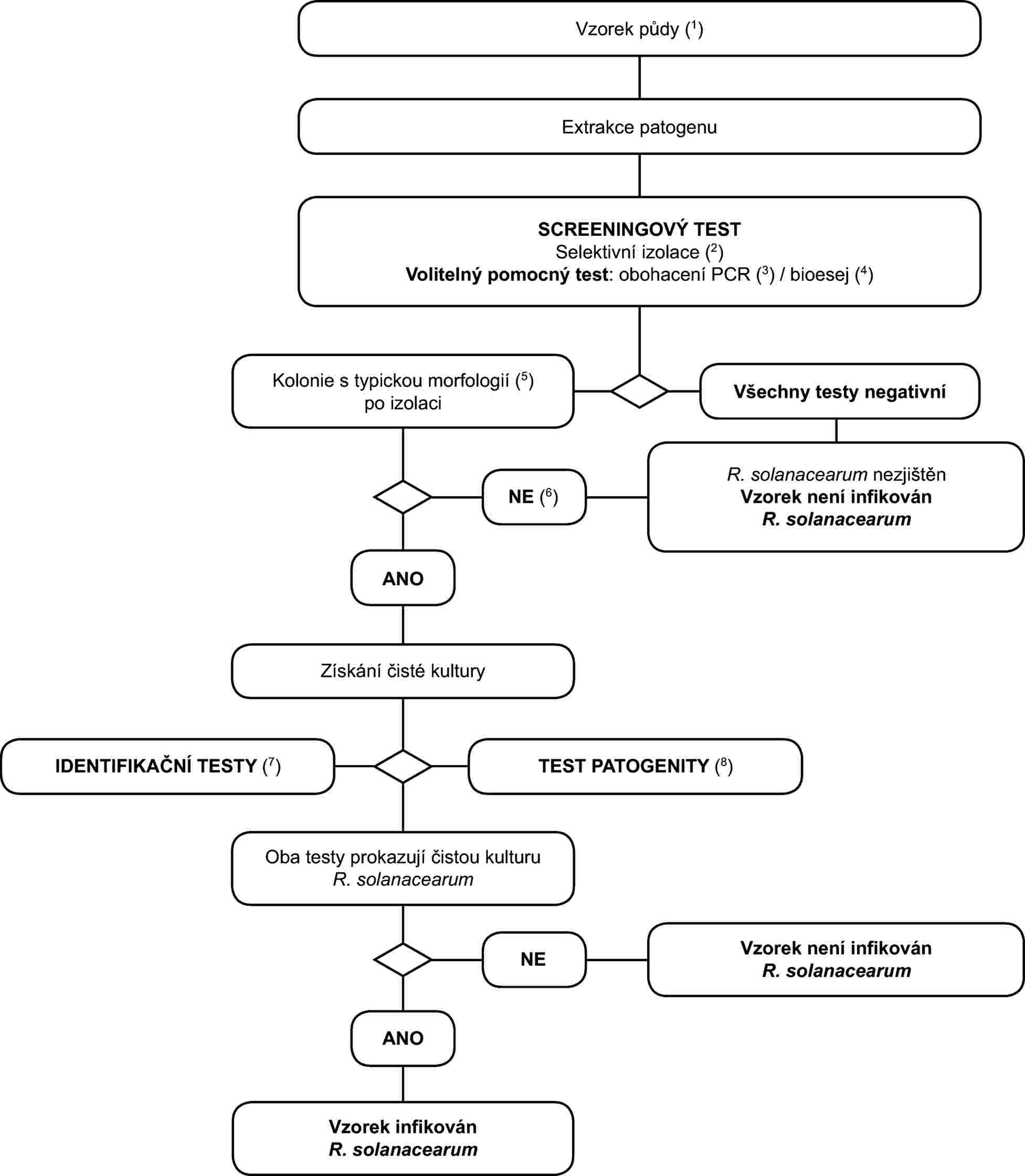

2. Metody pro zjištění a identifikaci R. solanacearum v půdě
Principy
Platné detekční schéma popsané v tomto oddíle je použitelné pro detekci patogenu ve vzorcích půdy, ale může být rovněž použito k testování vzorků pevného odpadu při zpracování brambor nebo kalu z odpadní vody. Je však nutné poznamenat, že tyto metody nejsou dostatečně citlivé, aby zaručovaly detekci nízkých nebo nepravidelně rozptýlených populací Ralstonia solanacearum, které se mohou vyskytovat v přirozeně infikovaných vzorcích těchto substrátů.
Při hodnocení spolehlivosti všech získaných negativních výsledků a také při sestavování přehledů určujících přítomnost patogenu v půdě nebo kalu je třeba vzít v úvahu omezenou citlivost tohoto testovacího schématu. Nejspolehlivějším testem přítomnosti patogenu v polní půdě je vypěstování náchylné hostitelské rostliny a její sledování, zda není infikována, ale i při použití této metody unikne nízký stupeň zamoření pozornosti.
2.1 Příprava vzorků
2.1.1 Vzorkování polní půdy by se mělo řídit standardními principy používanými pro vzorkování hlístů. Na jeden vzorek shromážděte 0,5 až 1 kg půdy ze 60 míst v 0,3 ha z hloubky 10–20 cm (nebo v mřížce 7 × 7 m). Je-li podezření na výskyt patogenu, zvyšte počet sběrných míst na 120 v 0,3 ha. Před testováním uchovejte vzorky při teplotě 12–15 °C. Kal ze zpracování brambor a kanalizace navzorkujte shromážděním celkem 1 kg z míst reprezentujících celkový objem testovaného kalu. Před testováním každý vzorek dobře promíchejte.
2.1.2 Rozptylte dílčí vzorky 10–25 g půdy nebo kalu rotační třepačkou (250 ot./min) v 60–150 ml extrakčního pufru (dodatek 4) po dobu 2 hodin. Je-li třeba, přidání 0,02 % sterilního Tween-20 a 10–20 g sterilních kamínků může napomoci disperzi.
2.1.3 Během testování udržujte suspenzi v teplotě 4 °C.
2.2 Testování
Postupový diagram a popis testů najdete v příslušném dodatku.
ODDÍL VI
OPTIMALIZOVANÉ PROTOKOLY PRO ZJIŠTĚNÍ A IDENTIFIKACI R. SOLANACEARUM
A. DIAGNOSTICKÉ A DETEKČNÍ TESTY
1. Test na výtok slizu ze stonku
Přítomnost R. solanacearum ve stoncích vadnoucích rostlin bramboru, rajčete nebo jiných hostitelských rostlin může ukázat následující jednoduchý test pravděpodobného výskytu: uřízněte stonek právě nad úrovní země. Ponořte řez stonku do zkumavky s čistou vodou. Sledujte, zda se po několika minutách objeví charakteristická samovolně proudící vlákna bakteriálního slizu z přeříznutých cévních svazků.
2. Test na přítomnost granulí poly-β-hydroxybutyrátu
|
1. |
Připravte roztěr bakteriálního slizu z infikovaného pletiva nebo ze 48 hodinové kultury na živné půdě YPGA nebo SPA (dodatek 2) na mikroskopické sklíčko. |
|
2. |
Připravte pozitivní kontrolní roztěr kmenu biovaru 2 R. solanacearum a případně negativní kontrolní roztěr o známém PHB negativním sp. |
|
3. |
Nechte je uschnout a protáhněte spodní povrch každého sklíčka rychle nad plamenem, abyste roztěry fixovali. |
|
4. |
Obarvěte preparáty buď nilskou modří nebo súdánskou černí a proveďte mikroskopická pozorování podle níže uvedeného popisu: |
Test nilskou modří:
|
a) |
Zakápněte obě sklíčka 1 % vodným roztokem nilské modři a nechte inkubovat 10 minut při teplotě 55 °C. |
|
b) |
Odstraňte barvicí roztok. Krátce opláchněte jemně tekoucí vodou z kohoutku. Odsajte přebytečnou vodu savým papírem. |
|
c) |
Zakápněte roztěr 8 % vodním roztokem kyseliny octové a nechte inkubovat 1 minutu při pokojové teplotě. |
|
d) |
Krátce opláchněte jemně tekoucí vodou z kohoutku. Odsajte přebytečnou vodu savým papírem. |
|
e) |
Znovu navlhčete kapkou vody a přiložte krycí sklíčko. |
|
f) |
Zkoumejte obarvený roztěr epifluorescenčním mikroskopem při 450 nm pod olejovou nebo vodní imersí se zvětšením 600× až 1 000× s použitím objektivu pro olejovou nebo vodní imersi. |
|
g) |
Pozorujte, zda se objeví na PHB granulích jasně oranžová fluorescence. Také pozorujte v procházejícím normálním světle, zda jsou granule intracelulární a zda je morfologie buněk typická pro R. solanacearum. |
Test súdánskou černí:
|
a) |
Zakápněte všechna sklíčka 0,3 % roztokem súdánské černi B v 70 % etanolu a inkubujte 10 minut při pokojové teplotě. |
|
b) |
Odstraňte barvicí roztok a krátce opláchněte jemně tekoucí vodou z kohoutku, odsajte přebytečnou vodu savým papírem. |
|
c) |
Ponořte sklíčka krátce do xylolu a vysajte savým papírem. Upozornění: xylol je zdraví škodlivý, učiňte nezbytná bezpečnostní opatření a pracujte v digestoři. |
|
d) |
Zakápněte sklíčka 0,5 % (w/v) vodným roztokem safraninu a nechte 10 vteřin inkubovat při pokojové teplotě. Upozornění: safranin je zdraví škodlivý, učiňte nezbytná bezpečnostní opatření a pracujte v digestoři. |
|
e) |
Opláchněte jemně tekoucí vodou z kohoutku, odsajte přebytečnou vodu savým papírem a přiložte krycí sklíčko. |
|
f) |
Zkoumejte obarvený roztěr mikroskopem s procházejícím světlem pod olejovou imersí a při zvětšení 1 000x. |
|
g) |
Pozorujte, zda uvidíte modročerné zbarvení PHB granulí v buňkách R. solanacearum s růžově zbarvenými stěnami buněk. |
3. Sérologické aglutinační testy
Aglutinace buněk R. solanacearum v bakteriálním slizu nebo v extraktech z pletiv s příznaky je nejlépe pozorovatelná pomocí validovaných protilátek (viz dodatek 3) označených příslušnými obarvenými značkovači, např. červenými buňkami Staphylococcus aureus nebo obarvenými latexovými částicemi. Při použití komerčně dostupného vybavení (viz dodatek 3) se řiďte instrukcemi výrobce. Jinak se řiďte následujícím postupem:
|
a) |
Smíchejte kapky suspense označené protilátky a bakteriálního slizu (přibližně 5 µl každé látky) na okénku testovacího víceokénkového sklíčka. |
|
b) |
Připravte pozitivní a negativní kontrolní vzorky použitím suspenzí biovaru 2 R. solanacearum a heterologního kmenu. |
|
c) |
Pozorujte, zda se v pozitivních vzorcích po jemném míchání po dobu 15 sekund objeví aglutinace. |
4. Selektivní izolace
4.1 Očkování na živnou půdu
Pozn.: Než použijete tuto metodu poprvé, proveďte předběžný test, abyste zajistili reprodukovatelnou detekci 103 až 104 jednotek tvořících kolonie R. solanacearum na 1 ml přidaných do extraktů ze vzorků, které byly předtím testovány s negativním výsledkem.
Použijte řádně validovanou selektivní živnou půdu, např. SMSA (ve znění Elphinstone et al., 1996; viz dodatek 2).
Rozlišení R. solanacearum od jiných bakterií schopných na živné půdě růst vyžaduje velkou pozornost. Dále, kolonie R. solanacearum mohou mít atypickou morfologii, jestliže Petriho misky jsou přeplněny nebo jsou rovněž přítomny antagonistické bakterie. Je-li podezření na konkurenci nebo inhibici, měl by být vzorek otestován znovu pomocí jiného testu.
Při použití čerstvě připravených extraktů ze vzorků lze očekávat, že citlivost detekce touto metodou bude velmi vysoká. Metoda je však použitelná i pro extrakty, které byly uchovány v glycerolu při teplotě od –68 do –86 °C.
Pozitivní kontroly připravte jako desetinné ředění ze suspenze 106 cfu/ml virulentního kmene biovaru 2 R. solanacearum (např. NCPPB 4156 = PD 2762 = CFBP 3857). Abyste se vyhnuli možné kontaminaci, připravte pozitivní kontrolní vzorky zcela odděleně od vzorků k testování.
U každé nově připravené šarže selektivní živné půdy by měla být před jejím použitím k rutinnímu testování vzorků nejdříve otestována její vhodnost pro kultivaci patogenu.
Kontrolní materiál testujte týmž způsobem jako vzorek (vzorky).
4.1.1 Proveďte vhodnou techniku ředění s cílem zajistit, aby všechny populace saprofytických bakterií, byly vyloučeny. Naneste 50–100 µl extraktu vzorku na 1 misku pro každé ředění.
4.1.2 Nechte misky inkubovat při teplotě 28 °C. Po 48 hodinách zkontrolujte jejich stav a pak provádějte kontrolu denně po 6 dní. Typické kolonie R. solanacearum na živné půdě SMSA jsou mléčně bílé, ploché, nepravidelné a fluidní a po 3 dnech inkubace se rozvine růžově až krvavě červené zbarvení ve středu s vnitřními pruhy nebo spirálami (viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main).
Pozn.: Někdy se na tomto médiu tvoří atypické kolonie R. solanacearum. Mohou být malé, kruhové, zcela červené a nefluidní nebo jen částečně fluidní, a proto obtížně rozeznatelné od saprofytických bakterií tvořících kolonie.
4.1.3 Předpokládané kolonie R. solanacearum rozetřete nebo očkujte metodou zřeďování na universální živnou půdu, abyste získali izolované kolonie (viz dodatek 2).
4.1.4 Uchovávejte kultury krátkodobě ve sterilní vodě (pH 6–8, bez chlóru) při pokojové teplotě v temnu nebo dlouhodobě ve vhodném ochranném médiu při teplotě –68 až –86 °C nebo lyofilizované.
4.1.5 Proveďte identifikaci podezřelých kultur (viz oddíl VI.B) a test patogenity (viz oddíl VI.C).
Interpretace výsledků testu očkováním na selektivní média.
Test očkování na selektivní média je negativní, jestliže po 6 dnech nejsou zpozorovány žádné bakterie nebo nejsou nalezeny žádné podezřelé kolonie typické pro R. solanacearum, za předpokladu, že nedošlo k inhibici jinými bakteriemi a v kontrolních vzorcích jsou nalezeny typické kolonie R. solanacearum.
Test očkování na selektivní média je pozitivní, jestliže jsou izolovány podezřelé kolonie R. solanacearum.
4.2 Obohacovací testy
Použijte validované médium pro obohacení, např. modifikovaný bujón Wilbrink (viz dodatek 2).
Tento postup lze použít pro selektivní zvětšení populací R. solanacearum v extraktech ze vzorků a zvýšení citlivosti detekce. Tímto způsobem dojde i ke zředění potenciálních inhibitorů PCR testu(1:100). Je však třeba poznamenat, že obohacení R. solanacearum může být neúspěšné z důvodů konkurence nebo antagonismu saprofytických organismů, které bývají často současně také obohaceny. Z tohoto důvodu může být izolace organismu R. solanacearum z obohacené kultury obtížná. Kromě toho, protože může dojít k rozvoji populací sérologicky příbuzných saprofytů, se pro test ELISA doporučuje použít místo polyklonálních protilátek specifické monoklonální protilátky.
4.2.1 U obohacovacího testu PCR přeneste 100 µl extraktu ze vzorku do 10 ml obohaceného bujónu (dodatek 2), který si předem připravte do sterilních zkumavek nebo baněk. U obohacovacího testu ELISA může být použit větší podíl extraktu ze vzorku do bujónu (např. 100 µl v 1,0 ml obohacené živné půdy).
4.2.2 Nechte inkubovat 72 hodin při teplotě 27 až 30 °C v třepané nebo statické kultuře s uvolněnými uzávěry, které umožní provzdušňování.
4.2.3 Před zahájením testů ELISA nebo PCR dobře promíchejte.
4.2.4 S obohaceným bujónem zacházejte týmž způsobem jako se vzorky ve výše uvedených testech.
Pozn.: Očekává-li se inhibice obohacení R. solanacearum z důvodu vysoké koncentrace konkurenčních saprofytických bakterií, lze docílit lepších výsledků obohacením extraktů ze vzorků před jakýmkoli odstřeďováním nebo jinými postupy zvyšování koncentrace.
5. Test IF
Postup
Použití testu IF jako hlavního screeningového testu se doporučuje kvůli dokázané spolehlivosti v dosažení požadovaných prahů.
Použije-li se test IF jako hlavní a výsledek IF testu je pozitivní, musí být jako druhý screeningový test použit test izolace, PCR nebo FISH. Jestliže je test IF použit jako druhý screeningový test a je pozitivní, je nutné provést další testování podle postupového diagramu, aby byla analýza úplná.
Pozn.: Použijte validovaný zdroj protilátek R. solanacearum (viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main). Doporučuje se určit titr pro každou novou šarži protilátek. Titr je definován jako nejvyšší ředění, při kterém dojde k optimální reakci při testování suspenze obsahující 105 až 106 buněk/ml homologického kmene R. solanacearum a použitím vhodného konjugátu fluorescenčního isothiokyanatanu (FITC) podle doporučení výrobce. Validovaná polyklonální antiséra mají všechna titr IF nejméně 1:2 000. Během testování by měly být použity protilátky v pracovních ředěních blízkých nebo stejných jako titr.
Test by měl být proveden na čerstvě připravených extraktech ze vzorků. Jestliže je to nutné, může být úspěšně proveden na vzorcích uchovaných při teplotě –68 až –86 °C v glycerolu. Glycerol může být ze vzorku odstraněn přidáním 1 ml pufru (dodatek 4), 15minutovým odstřeďováním při 7 000 g a resuspenzí ve stejném množství peletového pufru. Často to není potřeba, zvláště pokud jsou vzorky fixovány na sklíčka plamenem.
Připravte oddělená pozitivní kontrolní sklíčka s homologickým kmenem nebo jiným referenčním kmenem R. solanacearum suspendovaném v bramborovém extraktu, jak je uvedeno v dodatku 3 B, a nepovinně v pufru.
Pletivo infikované přirozenou cestou (uchovávané lyofilizací nebo zmrazením při teplotě –16 až –24 °C) by se mělo podle možností použít jako paralelní kontrola na stejném podložním sklíčku.
Jako negativní kontroly použijte alikvotní díly extraktů ze vzorků, které byly předtím testovány s negativním výsledkem.
Standardizované materiály k pozitivní a negativní kontrole, které lze použít pro tento test, jsou uvedeny v dodatku 3.
Použijte mikroskopická sklíčka s více okénky, pokud možno s 10 okénky s průměrem nejméně 6 mm.
Test kontrolního materiálu proveďte týmž způsobem jako test vzorků.
5.1 Připravte sklíčka k testování jedním z následujících postupů:
|
i) |
Pro pelety s relativně nízkým množstvím sedimentu škrobu: Napipetujte odměřené standardní množství (15 µl je vhodné pro průměr okénka 6 mm – u většího okénka je množství větší v příslušném poměru) resuspendované bramborové pelety v ředění 1/100 do prvního okénka. Následně napipetujte stejné množství nezředěné pelety (1/1) do zbývajících okének v řadě. Druhá řada může být použita jako duplikát nebo pro druhý vzorek, jak ukazuje obr. 1. |
|
ii) |
Pro jiné pelety: Připravte desetinná ředění (1/10, 1/100) resuspendované pelety v peletovém pufru. Napipetujte odměřené standardní množství (15 µl je vhodné pro průměr okénka 6 mm – u většího okénka je množství větší v příslušném poměru) resuspendované pelety pro každé ředění do řady okének. Druhá řada může být použita jako rezervní nebo pro druhý vzorek, jak ukazuje obr. 2. |
5.2 Vysušte kapičky při okolní teplotě nebo zahřátím na teplotu 40 až 45 °C. Fixujte bakteriální buňky na sklíčko buď zahřátím (15 minut při teplotě 60 °C), plamenem, 95 % etanolem nebo podle konkrétních instrukcí od dodavatele protilátek.
Pokud je potřeba, fixovaná sklíčka je možné skladovat ve zmrazeném stavu v suchém boxu po nezbytně krátkou dobu (maximálně 3 měsíce) před dalším testováním.
5.3 Postup IF
|
i) |
Podle přípravy sklíčka na test v odst. 5.1.i): Připravte sadu dvojnásobných zředění. První jamka by měla mít 1/2 titru (T/2), ostatní 1/4 titru (T/4), 1/2 titru (T/2), titr (T) a dvojnásobek titru (2T). |
|
ii) |
Podle přípravy sklíčka na test v odst. 5.1.ii): Připravte pracovní ředění (PŘ) protilátek v pufru IF. Pracovní ředění ovlivňuje přesnost. |
Obrázek 1. Příprava sklíčka na test podle odst. 5.1.i) a 5.3.i)
|
|
Ředění resuspendované pelety |
||||||
|
1/100 |
1/1 |
1/1 |
1/1 |
1/1 |
|
Ředění resuspendované pelety |
|
|
(T = titr) |
T/2 |
T/4 |
T/2 |
T |
2T |
|
Dvojnásobné ředění antiséra/protilátky |
|
Vzorek 1 |
|
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
5 |
|||
|
Duplikát vzorku 1 nebo vzorek 2 |
|
|
|
|
|
||
|
6 |
7 |
8 |
9 |
10 |
|||
Obrázek 2. Příprava sklíčka na test podle odst. 5.1.ii) a 5.3.ii)
|
|
Pracovní ředění antitiséra/protilátky |
||||||
|
1/1 |
1/10 |
1/100 |
prázdný |
prázdný |
|
Desetinné ředění resuspendované pelety |
|
|
Vzorek 1 |
|
|
|
|
|
|
|
|
1 |
2 |
3 |
4 |
5 |
|||
|
Duplikát vzorku 1 nebo vzorek 2 |
|
|
|
|
|
||
|
6 |
7 |
8 |
9 |
10 |
|||
5.3.1 Uspořádejte podložní sklíčka na navlhčený savý papír. Pokryjte každé testovací okénko kompletně ředěním protilátek. Množství protilátky na každém okénku musí být nejméně stejné jako množství použitého extraktu.
Pokud nemáte konkrétní pokyny od dodavatele protilátek, řiďte se následujícím postupem:
5.3.2 Podložní sklíčka inkubujte na vlhkém papíře přikrytá po dobu 30 minut při pokojové teplotě (18–25 °C).
5.3.3 Setřeste kapky ze všech podložních sklíček a pečlivě opláchněte pufrem IF. Umyjte ponořením po dobu 5 minut v pufru IF Tween (dodatek 4) a následně v pufru IF. Zabraňte vzniku aerosolu nebo přenosu kapiček, které by mohly způsobit vzájemnou kontaminaci. Pečlivě odstraňte přebytečnou vlhkost jemným osušením.
5.3.4 Umístěte sklíčka na vlhký papír. Testovací okénka pokryjte ředěním konjugátu FITC, kterým se stanovuje titr. Množství konjugátu naneseného do okének musí být stejné jako množství použité protilátky.
5.3.5 Inkubujte sklíčka zakrytá na vlhkém papíru po dobu 30 minut při pokojové teplotě (18–25 °C).
5.3.6 Setřeste kapky konjugátu ze sklíčka. Opláchněte a umyjte jako předtím (5.3.3).
Opatrně odstraňte přebytečnou vlhkost.
5.3.7 Napipetujte 5–10 µl 0,1M fosfátového pufru s glycerolem (dodatek 4) nebo komerční krycí tekutiny do každého okénka a přiložte krycí sklíčko.
5.4. Vyhodnocení IF testu
5.4.1 Prohlížejte testovací sklíčka epifluorescenčním mikroskopem s filtry vhodnými pro excitaci FITC pod olejovou nebo vodní imersí při zvětšení 500× až 1 000×. Zkoumejte okénka ve dvou navzájem kolmých průměrech a kolem obvodu. U vzorků s žádnými nebo malým počtem buněk zkoumejte nejméně 40 polí mikroskopu.
Nejdřív zkontrolujte pozitivní kontrolní vzorek. Buňky musí být jasně fluoreskující a zcela obarvené v určeném titru protilátky nebo pracovnímu ředění. Pokud je barevnost odchylná, musí být test IF opakován (odst. VI.A.5).
5.4.2 Pozorujte jasně fluoreskující buňky s charakteristickou morfologií R. solanacearum v testovacích okéncích sklíčka (viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main). Intenzita fluorescence musí být při porovnání s pozitivním kontrolním kmenem ve stejném ředění protilátky stejná nebo lepší. Buňky s neúplným zbarvením nebo slabou fluorescencí nelze brát v úvahu.
Při podezření z jakékoli kontaminace musí být test zopakován. To se může stát, když všechna sklíčka ve skupině vykazují pozitivní buňky díky kontaminaci pufru nebo při zjištění pozitivních buněk (mimo okénka sklíček) na povrchu sklíček.
5.4.3 Existuje několik problémů podstatných pro přesnost imunofluorescenčního testu. V peletách z pupkové části bramboru a částí stonku se mohou vyskytnout doprovodné populace fluoreskujících buněk s atypickou morfologií a křížově reagující saprofytické bakterie s velikostí a morfologií podobnou R. solanacearum.
5.4.4 Uvažujte pouze fluoreskující buňky s typickou velikostí a morfologií v titru nebo pracovním ředění protilátek podle 5.3.
5.4.5 Interpretace výsledků testu IF:
|
i) |
Při zjištění jasně fluoreskujících buněk s typickou morfologií odhadněte průměrný počet typických buněk v 1 mikroskopovém poli a vypočítejte počet typických buněk na 1 ml resuspendované pelety (dodatek 5). Výsledek IF je pozitivní u vzorků, kde je počet typických buněk na 1 ml resuspendované pelety nejméně 5 × 103. Vzorek je považován za potenciálně infikovaný a je povinné další testování. |
|
ii) |
Výsledek IF testu je negativní pro vzorky, které obsahují méně než 5 × 103 buněk na 1 ml resuspendované pelety a vzorek se považuje za negativní. Další testování není nutné. |
6. Testy PCR
Principy
Použije-li se test PCR jako hlavní screeningový test a výsledek je pozitivní, musí být povinně proveden druhý screeningový test, a sice izolace nebo IF. Jestliže je PCR použita jako druhý screeningový test a je pozitivní, je nutné provést další testování podle postupového diagramu, aby byla analýza úplná.
Využití této metody v celém rozsahu jako hlavního screeningového testu se doporučuje jen tehdy, je-li požadována specializovaná expertíza.
Pozn.: Předběžné testování touto metodou by mělo umožnit reprodukovatelné zjištění 103 až 104 buněk R. solanacearum na 1 ml přidaný do vzorků extraktů, které byly předtím testovány jako negativní. Dosažení maximální citlivosti a přesnosti ve všech laboratořích může vyžadovat optimalizační pokusy.
Použijte schválená činidla a protokoly PCR (viz dodatek 6). Pokud možno, vyberte metodu s interní kontrolou.
Používejte vhodná bezpečnostní opatření, abyste zabránili kontaminaci vzorku cílovou DNA. Test PCR by měl být prováděn zkušenými laboranty v laboratořích specializovaných na molekulární biologii, aby se minimalizovala možnost kontaminace cílovou DNA.
S negativními kontrolami (v průběhu extrakce DNA a PCR) by se mělo vždy zacházet jako s konečnými vzorky, aby bylo jasné, jestli došlo k přenosu DNA.
PCR test by měl zahrnovat následující negativní kontroly:
|
— |
extraktu ze vzorku, který byl předtím testován na R. solanacearum s negativním výsledkem, |
|
— |
kontroly pufru používaného pro extrakci bakterií a DNA ze vzorku, |
|
— |
reakční směs PCR. |
Měly by být zahrnuty následující pozitivní kontroly:
|
— |
alikvotní části resuspendovaných pelet, do kterých byla přidána R. solanacearum (přípravu viz dodatek 3 B); |
|
— |
suspenze 106 buněk na 1 ml R. solanacearum ve vodě z virulentního izolátu (např. NCPPB 4156 = PD 2762 = CFBP 3857; viz dodatek 3 B); |
|
— |
pokud možno, při PCR použijte také DNA extrahovanou z pozitivních kontrolních vzorků. |
Abyste zabránili případné kontaminaci, připravujte pozitivní kontroly v odděleném prostředí než vzorky, které budou testovány.
Extrakty ze vzorků by měly být pokud možno bez zeminy. V případě použití PCR testu je potřeba připravit extrakty z umytých brambor.
Standardizované materiály k pozitivní a negativní kontrole, které lze použít pro tento test, jsou uvedeny v dodatku 3.
6.1 Metody purifikace DNA
Používejte výše popsané pozitivní a negativní kontrolní vzorky (viz dodatek 3).
Test kontrolního materiálu proveďte týmž způsobem jako test vzorků.
K purifikaci cílové DNA z komplexních substrátů vzorků jsou k dispozici různé metody odstraňující inhibitory PCR a jiných enzymových reakcí a koncentrující cílovou DNA ve vzorku. Následující metoda byla optimalizována pro účely použití se schválenými metodami PCR uvedenými v dodatku 6.
a) Metoda podle Pastrika (2000)
|
1. |
Napipetujte 220 µl lyzátového pufru (100 mM NaCl, 10 mM Tris-HCl (pH 8,0), 1 mM EDTA (pH 8,0)) do 1,5 ml Eppendorfovy zkumavky. |
|
2. |
Přidejte 100 µl extraktu ze vzorku a umístěte do termobloku nebo vodní lázně s teplotou 95 °C na 10 min. |
|
3. |
Vložte mikrozkumavku na 5 min. do ledu. |
|
4. |
Přidejte 80 µl zásobního roztoku lysozymu (50 mg lysozymu/na 1 ml 10 mM TrisHCl, pH 8,0) a inkubujte při teplotě 37 °C po dobu 30 minut. |
|
5. |
Přidejte 220 µl roztoku Easy DNA® A (Invitrogen), dobře promíchejte třepáním a inkubujte při teplotě 65 °C po dobu 30 minut. |
|
6. |
Přidejte 100 µl roztoku Easy DNA® B (Invitrogen), důkladně promíchejte třepáním, pokud vzorek nezačne být stejnoměrně viskózní. |
|
7. |
Přidejte 500 µl chloroformu a promíchejte, až se viskozita sníží a směs se stane homogenní. |
|
8. |
Pro oddělení fází a vytvoření mezifáze odstřeďte při 15 000 g po dobu 20 min při teplotě 4 °C. |
|
9. |
Přeneste horní fázi do nové Eppendorfovy mikrozkumavky. |
|
10. |
Přidejte 1 ml 100 % etanolu (–20 °C), krátce promíchejte třepáním a inkubujte na ledu po dobu 10 min. |
|
11. |
Odstřeďte při 15 000 g po dobu 20 minut při teplotě 4 °C a odstraňte etanol z pelety. |
|
12. |
Přidejte 500 µl 80 % etanolu (–20 °C) a promíchejte překlápěním mikrozkumavky. |
|
13. |
Odstřeďte při 15 000 g po dobu 10 minut při teplotě 4 °C, zachovejte peletu a odstraňte etanol. |
|
14. |
Nechte peletu uschnout na vzduchu nebo v DNA odparce. |
|
15. |
Resuspendujte peletu v 100 µl sterilní UPW a nechte stát při pokojové teplotě nejméně 20 minut. |
|
16. |
Skladujte při teplotě –20 °C až do použití při PCR. |
|
17. |
Jakoukoli bílou sraženinu odstraňte odstředěním a použijte 5 µl supernatantu obsahujícího DNA pro test PCR. |
b) Jiné metody
Jiné metody extrakce DNA, např. Qiagen DNeasy Plant Kit, by se mohly použít, pokud by se prokázalo, že jsou při purifikaci DNA z kontrolních vzorků obsahujících 103 až 104 patogenních buněk na 1 ml stejně efektivní.
6.2. PCR
6.2.1 Připravte testované vzorky a kontroly pro PCR podle schválených protokolů (oddíl VI.A.6). Připravte desetinásobné ředění vzorku extraktu DNA (1:10 ve sterilní vodě).
6.2.2 Připravte příslušnou reakční směs pro PCR v prostředí, ve kterém nehrozí kontaminace podle zveřejněných protokolů (dodatek 6). Pokud možno, doporučuje se použít multiplexní protokol PCR, který rovněž zahrnuje interní protokol PCR.
6.2.3 Přidejte do sterilních PCR mikrozkumavek 5 µl extraktu DNA na 25 µl PCR reakce podle protokolů PCR (viz dodatek 6).
6.2.4 Přidejte negativní kontrolní vzorky obsahující pouze reakční směs PCR a přidejte týž zdroj UPW jako byl ten, který byl použit ve směsi PCR místo vzorku.
6.2.5 Umístěte PCR mikrozkumavky do téhož termocykleru, který byl použit při počátečním testování, a spusťte vhodně optimalizovaný program PCR (dodatek 6).
6.3. Analýza produktu PCR
6.3.1 Amplikony rozdělte elektroforézou v agarózovém gelu. Naneste nejméně 12 µl směsi amplifikované DNA z každého vzorku s 3 µl nanášecího pufru (dodatek 6) do 2,0 % (w/v) agarózovém gelu v Tris-acetát-EDTA (TAE) pufru (dodatek 6) při 5–8 V/cm. Použijte vhodný DNA marker, např. (ladder) 100 bp.
6.3.2 Detekujte proužky DNA obarvením v ethidiumbromidu (0,5 mg/l) po dobu 30–60 minut za použití vhodných bezpečnostních opatření pro zacházení s tímto mutagenem.
6.3.3 V obarveném a UV (krátké vlnové délky např. 302 nm) prosvíceném gelu hledejte amplifikované produkty PCR o očekávané velikosti a výsledek zdokumentujte.
6.3.4 U všech nových nálezů/případů zkontrolujte pravost amplikonu PCR provedením restrikční enzymové analýzy ve zbývajícím vzorku amplifikované DNA inkubací při optimální teplotě a čase shodným restrikčním enzymem a pufrem (viz dodatek 6). Rozdělte naštěpené fragmenty elektroforézou v agarózovém gelu a pozorujte charakteristický vzor restrikčních fragmentů pod UV světlem po obarvení ethidiumbromidem a porovnejte s neštěpenou a štěpenou pozitivní kontrolou.
Interpretace výsledků testu PCR
Test PCR je negativní, jestliže amplikon PCR specifický pro R. solanacearum očekávané velikosti není u zkoumaného vzorku zjištěn, ale je zjištěn u všech pozitivních kontrolních vzorků (v případě vícenásobné PCR s interními kontrolními primery specifickými pro rostlinu: druhý produkt PCR očekávané velikosti musí být amplifikován se zkoumaným vzorkem).
Test PCR je pozitivní, jestliže amplikon PCR specifický pro R. solanacearum očekávané velikosti a (případně) vzoru je zjištěn, za předpokladu, že není amplifikován u žádného vzorku negativní kontroly. Spolehlivé potvrzení pozitivního výsledku lze také získat opakováním testu s druhou sadou primerů PCR (dodatek 6).
Pozn.: Lze mít podezření na inhibici PCR, jestliže je získán očekávaný amplikon ze vzorku pozitivní kontroly obsahujícího R. solanacearum ve vodě, zatímco ze vzorku pozitivní kontroly R. solanacearum v bramborovém extraktu byly získány negativní výsledky. V multiplexních protokolech PCR s interními kontrolami PCR nasvědčuje inhibici reakce, jestliže není získán žádný ze dvou amplikonů.
V případě, že očekávaný amplikon je získán z jednoho nebo více vzorků negativních kontrol, je podezření na kontaminaci.
7. Test FISH
Princip
Když se jako první screeningový test použije FISH test a je pozitivní, musí být jako druhý povinný screeningový test provedena izolace nebo IF test. Když se FISH test provede jako druhý vyšetřovací test a je pozitivní, je k dokončení diagnózy nutné další testování podle postupového diagramu.
Poznámka: Používejte schválené oligosondy specifické pro R. solanacearum (dodatek 7). Úvodní testování touto metodou by mělo umožnit reprodukovatelné zjištění alespoň 103–104 buněk R. solanacearum na ml přidané do extraktů ze vzorku, které byly předtím testovány s negativním výsledkem.
Následující postup by měl být pokud možno proveden s čerstvě připravenými extrakty, ale je možné jej úspěšně provést s extraktem, který byl uchován v glycerolu při teplotě –16 až –24 °C nebo –68 až –86 °C.
Jako negativní kontroly používejte alikvotní část extraktu ze vzorku, který byl předtím testován na R. solanacearum s negativním výsledkem.
Jako pozitivní kontroly připravte suspenzi obsahující 105 až 106 buněk na 1 ml R. solanacearum biovar 2 (např. kmen NCPPB 4156 = PD 2762 = CFBP 3857, viz dodatek 3) v 0,01M fosfátovém pufru (PB) ze 3–5 denní kultury. Připravte samostatná sklíčka s pozitivními kontrolními vzorky homologického kmenu nebo jiného referenčního kmene R. solanacearum, suspendovaném v bramborovém extraktu, jak je uvedeno v dodatku 3 B.
Použití eubakteriálních oligosond značených FITC poskytuje kontrolu procesu hybridizace, protože zbarví všechny eubakterie přítomné ve vzorku.
Standardizovaný pozitivní a negativní kontrolní materiál, který se používá v tomto testu, je uveden v dodatku 3 bodu A.
Proveďte test kontrolního materiálu stejným způsobem jako u vzorku(ů).
7.1. Fixace bramborového extraktu
Následující protokol vychází z Wullings et al. (1998).
7.1.1 Připravte fixační roztok (viz dodatek 7).
7.1.2 Napipetujte 100 µl každého vzorkového extraktu do Eppendorfovy mikrozkumavky a odstřeďujte po dobu 7 minut na 7 000 g.
7.1.3 Odstraňte supernatant a rozpusťte peletu ve 200 µl fixačního roztoku připraveného max. 24 hodin předem. Protřepte a inkubujte 1 hodinu v chladícím zařízení.
7.1.4 Odstřeďujte 7 minut při 7 000 g, odstraňte supernatant a resuspendujte peletu v 75 µl 0,01M PB (viz dodatek 7).
7.1.5 Kápněte 16 µl fixované suspenze na čisté 10 okénkové sklíčko, jak ukazuje obrázek 7.1, přičemž použijete 2 různé vzorky na jedno sklíčko, a to neředěný a zředěný 1:100 s použitím 10 µl (v 0,01 M PB). Zbývající roztok vzorku (49 µl) může být uložen při teplotě –20 °C po přidání 1 objemového množství 96 % etanolu. V případě, že je třeba FISH metodu opakovat, odstraňte etanol odstředěním a přidejte stejné množství 0,01 PB (zamíchejte protřepáním).
Obrázek 7.1 Rozmístění na sklíčku FISH
|
Vzorek 1 |
Prázdný |
Prázdný |
Prázdný |
Vzorek 2 |
|
|
|
|
|
|
|
okénko 1 |
okénko 2 |
okénko 3 |
okénko 4 |
okénko 5 |
|
Vzorek 1 |
Prázdný |
Prázdný |
Prázdný |
Vzorek 2 |
|
|
|
|
|
|
|
okénko 6 |
okénko 7 |
okénko 8 |
okénko 9 |
okénko 10 |
|
Krycí sklíčko 1 |
|
Krycí sklíčko 2 |
||
7.1.6 Nechte sklíčka uschnout na vzduchu (nebo sušičkou sklíček při teplotě 37 °C) a fixujte nad plamenem.
V této fázi je možné postup přerušit a pokračovat v hybridizaci další den. Sklíčka by měla být skladována chráněna před prachem a v suchu při pokojové teplotě.
7.2. Hybridizace
7.2.1 Dehydratujte buňky v postupné etanolové řadě 50 %, 80 % a 96 %, pokaždé po dobu 1 minuty. Osušte vzduchem v držáku sklíček.
7.2.2. Připravte vlhkou inkubační komoru přikrytím dna vzduchotěsného boxu tkaninou nebo filtračním papírem nasáklým hybridizační směsí (1x hybmix, dodatek 7). Před inkubací ohřejte box v hybridizační peci při teplotě 45 °C po dobu nejméně 10 minut.
7.2.3 Použijte 10 μl hybridizačního roztoku (dodatek 7) na 8 okének (okénka 1, 2, 4, 5, 6, 7, 9 a 10; viz obr.7.1) na každém sklíčku, přičemž dvě středová okénka necháte prázdná (3 a 8).
7.2.4 Přiložte krycí sklíčka (24 × 24 mm) na první a poslední 4 okénka, a to tak, aby pod ně nevnikl vzduch. Umístěte sklíčka do předem zahřáté vlhké komory a nechte proběhnout proces hybridizace po dobu 5 hodin v troubě při teplotě 45 °C v temnu.
7.2.5 Připravte 3 kádinky obsahující 1 l vody s molekulární kvalitou (Milli Q), 1 l 1x hybmix (334 ml 3x hybmix a 666 ml vody s molekulární kvalitou) a 1 l 1/8x hybmixu (42 ml 3x hybmix a 958 ml vody s molekulární kvalitou). Nechte inkubovat ve vodní lázni o teplotě 45 °C.
7.2.6 Sejměte krycí sklíčka a umístěte podložní sklíčka do držáku sklíček.
7.2.7 Spláchněte nadbytek vzorku inkubací po dobu 15 minut v kádince s 1x hybmixem při teplotě 45 °C
7.2.8 Přemístěte držák sklíček do promývacího roztoku 1/8 hybmix a nechte inkubovat dalších 15 minut.
7.2.9 Ponořte sklíčka krátce do UPW (např. Milli Q water) a položte je na filtrační papír. Odstraňte nadbytečnou vlhkost lehkým zakrytím povrchu filtračním papírem. Napipetujte 5–10 μl krycího roztoku (např. Vectashield, Vecta Laboratories, CA, USA nebo podobný) do každého okénka a celé sklíčko zakryjte velkým krycím sklíčkem (24 × 60 mm).
7.3. Hodnocení FISH testu
7.3.1 Prohlížejte sklíčka ihned s mikroskopem vhodným pro epifluorescenční mikroskopii se zvětšením 630× nebo 1 000× pod olejovou imerzí. S filtrem vhodným pro fluorescein isothiokyanat (FITC) jsou eubakteriální buňky (včetně většiny gramnegativních buněk) ve vzorku zbarveny fluorescenčně zeleně. Použitím filtru pro tetramethylrhodamin-5-isothiokyanat se buňky R. solanacearum obarvené Cy3 jeví fluorescenčně červené. Porovnejte buněčnou morfologii s morfologií pozitivních kontrolních vzorků. Buňky musí být jasně fluoreskující a zcela zbarveny. Test FISH (odst. VI.A.7) musí být zopakován, pokud je zbarvení odchylné. Prohlížejte okénka napříč dvěma průměry v pravých úhlech a kolem obvodu. U vzorků, kde nejsou pozorovány žádné nebo málo buněk, pozorujte nejméně 40 polí mikroskopu.
7.3.2 Hledejte jasně fluoreskující buňky s morfologií charakteristickou pro R. solanacearum v okénkách testovacích sklíček (viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main). Intenzita fluorescence musí odpovídat nebo být lepší než u pozitivního kontrolního kmene. Buňky, které nejsou zcela zbarveny nebo vykazují slabou fluorescenci, neberte v úvahu.
7.3.3 Při podezření na jakoukoli kontaminaci musí být test opakován. To může nastat v případě, kdy všechna sklíčka ve várce ukazují pozitivní buňky z důvodu kontaminace pufru nebo jestliže jsou pozitivní buňky zjištěny (vně okénka sklíčka) na krytu sklíčka.
7.3.4 Specifičnost testu FISH s sebou nese několik problémů. Je pravděpodobné, že u pletiv z bramborových hlíz a pelet ze stonkových partií bramboru dojde k výskytu populací fluorescenčních buněk na pozadí s atypickou morfologií a ke křížové reakci se saprofytickými bakteriemi o velikosti a morfologii podobnými R. solanacearum, i když mnohem méně častěji než u testu IF.
7.3.5 V úvahu bereme pouze fluoreskující buňky s typickou velikostí a morfologií.
7.3.6 Interpretace výsledků testu FISH
|
i) |
Výsledky FISH testu jsou platné, pokud jsou při použití FITC filtru jasně zeleně fluoreskující buňky s velikostí a morfologií typickou pro R. solanacearum a při použití rhodaminového filtru jasně červeně fluoreskující buňky pozorovány ve všech pozitivních kontrolách a nejsou pozorovány v žádných negativních kontrolách. Pokud jsou přítomné jasně fluoreskující buňky s typickou morfologií, odhadněte průměrný počet typických buněk v 1 mikroskopovém poli a vypočítejte počet typických buněk v 1 ml resuspendované pelety (dodatek 4). Vzorky, které obsahují alespoň 5 × 103 typických buněk na 1 ml resuspendované pelety, se považují za pravděpodobně infikované Cms. Nutné je další testování. Vzorky, které obsahují méně než 5 × 103 typických buněk na 1 ml resuspendované pelety, se považují za negativní. |
|
ii) |
Výsledek FISH testu je negativní, pokud při použití rhodaminového filtru nejsou pozorovány jasně červeně fluoreskující buňky s velikostí a morfologií typickou pro R. solanacearum, jestliže jsou tyto typické jasně červeně fluoreskující buňky při použití rhodaminového filtru pozorovány v pozitivních kontrolách. |
8. Testy ELISA
Princip
Testy ELISA lze použít pouze jako volitelný test kromě testů IF, PCR nebo FISH pro jeho relativně nízkou citlivost. Při použití DAS ELISA je obohacení a použití monoklonálních protilátek povinné (viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main). Obohacení vzorků před použitím testu ELISA může zvýšit citlivost testu, ale může se rovněž setkat s nezdarem kvůli konkurenci jiných organismů ve vzorku.
Pozn.: Použijte validovaný zdroj protilátek R. solanacearum (viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main). Doporučuje se určení titru pro každou novou šarži protilátek. Titr je definován jako nejvyšší ředění, při kterém dojde k optimální reakci při testování suspense obsahující 105 až 106 buněk na 1 ml homologického kmene R. solanacearum a použití vhodných druhotných konjugátů protilátek podle doporučení výrobce. Při testování by měly být použity protilátky v pracovním ředění, které je blízké nebo stejné jako u titru komerční formulace.
Určete titr protilátek pro suspenzi 105 až 106 buněk na 1 ml homologického kmene R. solanacearum.
Vzorek, který jste předtím otestovali jako R. solanacearum negativní a suspenzi bakterií bez vzájemného působení v solném roztoku fosfátového pufru (PBS) použijte jako vzorky negativní kontroly.
Jako pozitivní kontrolní vzorky použijte alikvótní podíly vzorkových extraktů, které byly předtím otestovány jako negativní, s příměsí 103 až 104 buněk na 1 ml biovaru 2 R. solanacearum (např. kmen NCPPB 4156 = PD 2762 = CFBP 3857, viz dodatek 2 A a B). Pro srovnání výsledků na každé destičce použijte standardní suspenzi 105 až 106 buněk na 1 ml v PBS R. solanacearum. Zajistěte, aby byly pozitivní kontrolní vzorky dobře odděleny na mikrotitrové destičce od vzorků k testování.
Standardizované pozitivní a negativní materiály, které se používají pro tento test, jsou uvedeny v dodatku 3 bodu A.
Test kontrolního materiálu proveďte týmž způsobem jako test vzorku(ů).
Validované jsou dva protokoly ELISA.
a) Nepřímý test ELISA (Robinson Smith et al., 1995)
|
1) |
Použijte 100–200 µl vzorkového extraktu. (Zahřátí na 100 °C na 4 minuty ve vodní lázni nebo topném boxu může v některých případech redukovat vznik nespecifických výsledků). |
|
2) |
Přidejte stejné množství dvojnásobně silného uhličitanového krycího pufru (dodatek 4) a promíchejte. |
|
3) |
Nakapejte 100 µl do každé jamky mikrotitrační destičky (např. Nunc-Polysorp nebo rovnocenné) a nechte inkubovat 1 hodinu při teplotě 37 °C nebo přes noc při teplotě 4 °C. |
|
4) |
Vylijte extrakty z jamek. Vymyjte jamky třikrát pomocí PBS-Tween (dodatek 4) a nechte poslední vymývací roztok v jamce nejméně 5 minut. |
|
5) |
Připravte vhodné ředění protilátek proti R. solanacearum v blokačním pufru (dodatek 4). U validovaných komerčních protilátek použijte doporučená ředění (obvykle dvojnásobné koncentrace, než je titr). |
|
6) |
Přidejte 100 µl do každé jamky a nechte inkubovat 1 hodinu při teplotě 37 °C. |
|
7) |
Vylijte roztok protilátek z jamek a vymyjte je jako předtím (bod 4.). |
|
8) |
Připravte vhodné ředění konjugátu alkalické fosfatázy v blokačním pufru. Přidejte 100 µl do každé jamky a nechte inkubovat 1 hodinu při teplotě 37 °C. |
|
9) |
Vylijte konjugát z jamek a vymyjte jako předtím (bod 4). |
|
10) |
Přidejte 100 µl substrátového alkalického roztoku fosfatázy (dodatek 4) do každé jamky. Nechte inkubovat v temnu při pokojové teplotě a odečítejte absorbanci při 405 nm v pravidelných 90minutových intervalech. |
b) DAS-ELISA
|
1) |
Připravte vhodné ředění polyklonálního imunoglobulinu v uhličitanovém pufru pH 9.6 (dodatek 4). Přidejte 200 µl do každé jamky. Nechte inkubovat při teplotě 37 °C 4 až 5 hodin nebo 4 ° C po dobu 16 hodin. |
|
2) |
Jamky třikrát dobře vypláchnete použitím PBS-Tween (dodatek 4). Přidejte 190 µl extraktu ze vzorku do nejméně dvou jamek. Přidejte rovněž pozitivní a negativní kontrolní vzorky do dvou jamek na každé destičce. Nechte inkubovat 16 hodin při teplotě 4 °C. |
|
3) |
Jamky třikrát dobře vypláchnete použitím PBS-Tween (dodatek 4). |
|
4) |
Připravte vhodné ředění specifických monoklonálních protilátek R. solanacearum v PBS (dodatek 4) s obsahem 0,5 % hovězího sérového albuminu (BSA) a přidejte 190 µl do každé jamky. Nechte stát 2 hodiny při teplotě 37 °C. |
|
5) |
Jamky třikrát dobře vypláchnete použitím PBS-Tween (dodatek 4). |
|
6) |
Připravte ředění protimyšího imunoglobulinu konjugovaného alkalickou fosfatázou v PBS. Přidejte 190 µl do každé jamky a nechte inkubovat 2 hodiny při teplotě 37 °C. |
|
7) |
Jamky třikrát dobře vypláchnete použitím PBS-Tween (dodatek 4). |
|
8) |
Připravte roztok 1 mg p-NPP/ml alkalické fosfatázy v substrátovém pufru (dodatek 4). Přidejte 200 µl do každé jamky. Inkubujte v temnu při pokojové teplotě a čtení probíhá při absorbanci při 405 v pravidelných intervalech 90 minut. |
Interpretace výsledků testu ELISA
Test ELISA je negativní, jestliže průměrná hodnota optické hustoty (OH) z jamek se stejnými vzorky je menší než dvojnásobek OH u negativního kontrolního vzorku, pokud všechny hodnoty OH pozitivních kontrolních vzorků jsou větší než 1,0 (po 90 minutách inkubace se substrátem) a jsou větší než dvojnásobek OH získané z negativních vzorkových extraktů.
Test ELISA je pozitivní, jestliže průměrné hodnoty OH z jamek se stejným vzorkem jsou větší než dvojnásobek OH v negativním extraktu testovaného vzorku, pokud hodnoty OH ve všech negativních kontrolních vzorcích jsou menší než dvojnásobek hodnot v pozitivních kontrolních vzorcích.
Negativní hodnoty ELISA v pozitivních kontrolních vzorcích ukazují, že test nebyl proveden správně nebo že byl i inhibován. Pozitivní hodnoty ELISA v negativních kontrolních vzorcích ukazují, že došlo k vzájemné kontaminaci nebo nespecifickému vázání protilátek.
9. Biotest
Pozn.: Předběžné testování touto metodou by mělo umožnit reprodukovatelnou detekci 103 až 104 jednotek tvořících kolonie R. solanacearum na 1 ml přidaný do extraktu ze vzorku, který byl předtím testován s negativním výsledkem (přípravu viz v dodatku 3).
Nejvyšší citlivost zjištění lze očekávat při použití čerstvě připraveného extraktu ze vzorku a v optimálních růstových podmínkách. Metodu lze však také úspěšně použít na extrakty, které byly uchovány v glycerolu v teplotě –68 až –86 °C.
Následující protokol vychází z Janseho (1988):
9.1 Použijte 10 testovacích rostlin citlivé odrůdy rajčete (např. kultivaru Moneymaker nebo kultivaru s rovnocennou citlivostí podle testovací laboratoře) ve fázi třech pravých listů u každého vzorku. Podrobnosti pěstování viz v dodatku 8 nebo použijte lilek (např. kultivar Black Beauty nebo kultivary s rovnocennou citlivostí), ale jen rostliny ve fázi 2. až 3. listů až do plného rozvinu třetího pravého listu. Příznaky u lilku jsou méně výrazné a vyvíjejí se pomaleji. Pokud možno, doporučujeme proto použít sazenice rajčat.
Rozdělte 100 µl extraktu ze vzorku mezi testovací rostliny.
9.2.1 Inokulace injekční stříkačkou
Inokulujte stonky rostlin hned nad děložními listy pomocí stříkačky s podkožní jehlou (ne méně než 23G). Rozdělte vzorek mezi testovací rostliny.
9.2.2 Inokulace zářezem
Přidržte rostlinu mezi dvěma prsty a pipetou kápněte (přibližně 5–10 µl) suspendované pelety na stonek mezi děložní listy a první list.
Sterilním skalpelem udělejte příčný řez asi 1 cm dlouhý a hluboký přibližně 2/3 tloušťky stonku, přičemž řez začnete v místě kapky resuspendované pelety.
Utěsněte řez sterilní vazelínou z injekční stříkačky.
9.3 Stejnou technikou nainokulujte 5 sazenic vodnou suspenzí 105 až 106 buněk na 1 ml připravenou ze 48 hodinové kultury virulentního kmene biovaru 2 R. solanacearum jako pozitivní kontrolní vzorek a peletovým pufrem (dodatek 4) jako negativní kontrolní vzorek. Oddělte pozitivní a negativní kontrolní rostliny od ostatních rostlin, abyste zabránili vzájemné kontaminaci.
9.4 Nechte růst testovací rostliny v karanténním zařízení 4 týdny při teplotě 25–30 °C a vysoké relativní vlhkosti s přiměřeným zavlažováním, abyste zabránili jak přemokření, tak vadnutí z důvodu nedostatku vody. Abyste zabránili kontaminaci, držte pozitivní a negativní kontrolní rostliny ve zcela oddělených místech skleníku nebo vegetační komory nebo, v případě omezeného prostoru, zajistěte přísnou izolaci. Musejí-li být rostliny z různých vzorků po dobu inkubace drženy blízko sebe, oddělte je vhodnými zástěnami. Při hnojení, zalévání, prohlížení a všech ostatních činnostech věnujte zvláštní pozornost tomu, aby nedošlo k vzájemné kontaminaci. Nutné je udržovat skleník nebo vegetační prostor bez hmyzích škůdců, protože by mohli přenést bakterie mezi vzorky.
Hledejte příznaky vadnutí, epinastie, chlorózu a/nebo krnění.
9.5 Z infikovaných rostlin proveďte izolaci (odst. II.3) a identifikujte podezřelé čisté kultury (bod VI.B).
9.6 Jestliže během 3 týdnů nejsou pozorovány žádné příznaky, proveďte test IF/PCR/izolace na složeném vzorku ze segmentů stonků dlouhých 1 cm z každé testovací rostliny, který odeberete nad místem inokulace. Je-li test pozitivní, proveďte zřeďovací roztěry (bod 4.1).
9.7 Identifikujte všechny čisté kultury s podezřením na R. solanacearum (bod VI.B).
Interpretace výsledků biotestu
Platné výsledky biotestu jsou získány, jestliže pozitivní kontrolní testovací rostliny vykazují typické příznaky, bakterie mohou být z těchto rostlin znovu izolovány a negativní kontrolní rostliny nevykazují žádné příznaky.
Biotest je negativní, jestliže rostliny nejsou infikovány bakteriemi R. solanacearum, pokud byl organismus zjištěn u pozitivních kontrolních testovacích rostlin.
Biotest je pozitivní, jestliže testovací rostliny jsou infikovány bakteriemi R. solanacearum.
B. IDENTIFIKAČNÍ TESTY
Identifikujte čisté kultury izolovaného podezřelého organismu R. solanacearum použitím nejméně dvou následujících testů založených na různých biologických principech.
Zahrňte případně známé referenční kmeny pro každý provedený test (viz dodatek 3).
1. Výživové a enzymatické identifikační testy
Určete následující fenotypové vlastnosti, které jsou vesměs přítomny nebo naopak chybí u R. solanacearum, metodami Lelliott a Stead (1987), Klement et al. (1990), Schaad (2001).
|
Test |
Očekávaný výsledek |
|
Produkce fluorescenčního pigmentu |
– |
|
Poly-β-hydroxybutyrátové inkluze |
+ |
|
Test oxidace/fermentace (O/F) |
O+/F– |
|
Katalázová aktivita |
+ |
|
Oxidázový test podle Kovacse |
+ |
|
Redukce dusičnanů |
+ |
|
Využití citrátu |
+ |
|
Růst při 40 °C |
– |
|
Růst v 1 % NaCl |
+ |
|
Růst v 2 % NaCl |
– |
|
Arginin-dihydrolázová aktivita |
– |
|
Zkapalnění želatiny |
– |
|
Hydrolýza škrobů |
– |
|
Hydrolýza eskulinu |
– |
|
Produkce levanu |
– |
2. Test IF
2.1 Připravte suspenzi přibližně 106 buněk na 1 ml v pufru IF (dodatek 4).
2.2 Připravte řadu dvojnásobných zředění vhodného antiséra (viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main).
2.3 Použijte IF metodu (oddíl VI.A.5).
2.4 Test IF je pozitivní, jestliže titr IF kultury odpovídá titru pozitivní kontroly.
3. Test ELISA
Pozn.: Při provádění pouze 2 identifikačních testů nepoužívejte kromě této metody jiný sérologický test.
3.1 Připravte suspenzi přibližně 108 buněk na 1 ml v 1X PBS (dodatek 4).
3.2 Proveďte metodu ELISA se specifickou monoklonální protilátkou k R. solanacearum.
3.3 Test ELISA je pozitivní, jestliže hodnota výsledku testu ELISA získaná z této kultury je nejméně poloviční v porovnání s hodnotou z pozitivní kontroly.
4. Testy PCR
4.1 Připravte suspenzi přibližně 106 buněk na 1 ml sterilní vody (UPW = ultra pure water).
4.2 Ohřívejte 100 µl buněčné suspense v uzavřených zkumavkách v ohřívacím bloku nebo vařící vodní lázni při 100 °C 4 minuty. Vzorky mohou být uchovány při teplotě –16 až –24 °C do dalšího použití.
4.3 Použijte příslušné postupy PCR k amplifikaci amplikonů specifických pro R. solanacearum (např. Seal et al. (1993); Pastrik a Maiss (2000); Pastrik et al. (2002); Boudazin et al. (1999); Opina et al. (1997), Weller et al. (1999).
4.4 Identifikace organismu R. solanacearum je pozitivní, jestliže amplikony PCR mají stejnou velikost a mají stejnou mnohotvárnost délky fragmentů jako pozitivní kontrolní kmen.
5. Test FISH
5.1 Připravte suspenzi přibližně 106 buněk na 1 ml v UPW.
5.2 Použijte metodu FISH (oddíl VI.A.7) s nejméně 2 oligosondami specifickými pro R. solanacearum (dodatek 7).
5.3 Test FISH je pozitivní, jestliže se u kultury a pozitivní kontroly dosáhne stejných reakcí.
6. Analýza mastných kyselin (FAP)
6.1 Pěstujte kulturu na tryptikázo-sójovém agaru (Oxoid) 48 hodin při teplotě 28 °C.
6.2 Použijte metodu FAP (Janse, 1991; Stead, 1992).
6.3 Test FAP je pozitivní, jestliže je profil podezřelé kultury stejný jako profil pozitivní kontroly. Výskyt charakteristických mastných kyselin: 14:0 3OH, 16:0 2OH, 16:1 2OH a 18:1 2OH a absence 16:0 3OH poukazuje na Ralstonia sp.
7. Metody charakteristiky kmenů
Pro každý nový případ izolace organismu R. solanacearum se doporučuje charakteristika kmenu použitím jedné z následujících metod.
U každého provedeného testu zahrňte případně známé referenční kmeny (viz dodatek 3).
7.1 Stanovení biovaru
Organismus R. solanacearum je rozdělen do biovarů na základě schopnosti využití a/nebo oxidace tří disacharidů a tří hexosových alkoholů (Hayward, 1964 a Hayward et al., 1990). Živná půda pro test biovaru je popsána v dodatku 2. Test lze úspěšně provést očkováním do živné půdy s čistou kulturou R. solanacearum a inkubací při teplotě 28 °C. Je-li živná půda rozdělena na sterilní destičky s 96 jamkami (200 µl na 1 jamku), zbarvení se mění během 72 hodin od olivově zelené po žlutou a znamená pozitivní výsledek testu.
|
|
Biovar |
||||
|
|
1 |
2 |
3 |
4 |
5 |
|
Využití: |
|
||||
|
Maltosa |
– |
+ |
+ |
– |
+ |
|
Laktosa |
– |
+ |
+ |
– |
+ |
|
D (+) Cellobiosa |
– |
+ |
+ |
– |
+ |
|
Mannitol |
– |
– |
+ |
+ |
+ |
|
Sorbitol |
– |
– |
+ |
+ |
– |
|
Dulcitol |
– |
– |
+ |
+ |
– |
Dodatečné testy pro rozlišení dílčích fenotypů biovaru 2
|
|
Biovar 2A (světově rozšířen) |
Biovar 2A (Chile a Kolumbie) |
Biovar 2T (tropické oblasti) |
|
Využití trehalosy |
– |
+ |
+ |
|
Využití meso-inositolu |
+ |
– |
+ |
|
Využití D ribosy |
– |
– |
+ |
|
Pektolytická aktivita (1) |
nízká |
nízká |
vysoká |
7.2 Genomická variabilita
Molekulární identifikace kmenů komplexu R. solanacearum lze dosáhnout několikerými technikami, mezi něž patří:
7.2.1 Analýza délkového polymorfismu restrikčních fragmentů RFLP (Cook et al., 1989).
7.2.2 Repetitivní sekvenční PCR s využitím primerů REP, BOX a ERIC (Louws et al., 1995; Smith et al., 1995).
7.2.3 Analýza délkového polymorfismu amplifikovaných fragmentů AFLP (Van der Wolf et al., 1998).
7.3 Metody PCR
Specifické primery PCR (Pastrik et al, 2002; viz dodatek 6) lze použít k diferenciaci kmenů patřících do skupiny 1 (biovary 3, 4 a 5) a skupiny 2 (biovary 1, 2A a 2T) R. solanacearum, jak bylo původně definováno analýzou RFLP (Cook et al., 1989) a sekvenováním 16S rDNA (Taghavi et al., 1996).
C. KONFIRMAČNÍ TEST (TEST PATOGENITY)
Jako závěrečné potvrzení diagnózy R. solanacearum a k potvrzení virulence kultur identifikovaných jako R. solanacearum musí být proveden test patogenity.
|
1) |
Připravte inokulum o hustotě přibližně 106 buněk na 1 ml ze 24 až 48 hodinových kultur k testování a příslušný kmen pozitivní kontroly R. solanacearum (např. NCPPB 4156 = PD 2762 = CFBP 3857; viz dodatek 3). |
|
2) |
Inokulujte 5 až 10 náchylných sazenic rajčete nebo lilku ve fázi 3 pravých listů (viz odst. VI.A.9). |
|
3) |
Nechte inkubovat až 2 týdny při teplotě 25–28 °C a vysoké relativní vzdušné vlhkosti s přiměřeným zaléváním, bez vystavení rostlin zamokření nebo vyprahlosti půdy. U čistých kultur by typické vadnutí mělo nastat během 14 dnů. Neobjeví-li se po této době příznaky, kultura nemůže být považována jako patogenní forma R. solanacearum. |
|
4) |
Hledejte příznaky vadnutí a/nebo epinastie, chlorózy nebo krnění. |
|
5) |
Proveďte izolaci z rostlin vykazujících příznaky odebráním segmentu ze stonku asi 2 cm nad místem inokulace. Rozmělněte a suspendujte v malém množství sterilní destilované vody nebo 50 mM fosfátového pufru (dodatek 4). Proveďte izolaci ze suspense zřeďovacím roztěrem pokud možno na selektivní živné půdě (dodatek 2), a nechte inkubovat 48 až 72 hodin při teplotě 28 °C a vyhodnotíme na výskyt typických kolonií pro R. solanacearum. |
Dodatek 1
Laboratoře zapojené do optimalizace a schvalování protokolů
|
Laboratoř (2) |
Místo |
Země |
|
Agentur für Gesundheit und Ernährungssicherheit |
Vídeň a Linec |
Rakousko |
|
Departement Gewasbescherming |
Merelbeke |
Belgie |
|
Plantedirektoratet |
Lyngby |
Dánsko |
|
Central Science Laboratory |
York |
Anglie |
|
Scottish Agricultural Science Agency |
Edinburgh |
Skotsko |
|
Laboratoire National de la Protection des Végétaux, Unité de Bactériologie |
Angers |
Francie |
|
Laboratoire National de la Protection des Végétaux, Station de Quarantaine de la Pomme de Terre |
Le Rheu |
Francie |
|
Biologische Bundesanstalt |
Kleinmachnow |
Německo |
|
Pflanzenschutzamt Hannover |
Hannover |
Německo |
|
State Laboratory |
Dublin |
Irsko |
|
Dipartimento di Scienze e Tecnologie Agroambientali |
Boloň |
Itálie |
|
Regione Veneto Unita Periferica per i Servizi Fitosanitari |
Verona |
Itálie |
|
Nederlandse Algemene Keuringsdienst |
Emmeloord |
Nizozemsko |
|
Plantenziektenkundige Dienst |
Wageningen |
Nizozemsko |
|
Direcção-Geral de Protecção das Culturas |
Lisabon |
Portugalsko |
|
Centro Diagnostico de Aldearrubia |
Salamanca |
Španělsko |
|
Instituto Valenciano de Investigaciones Agrarias |
Valencie |
Španělsko |
|
Swedish University of Agricultural Sciences |
Uppsala |
Švédsko |
Dodatek 2
Živné půdy pro izolaci a kultivaci organismu R. solanacearum
a) živné půdy pro izolaci a kultivaci
Živný agar (NA)
|
Živný agar (Difco) |
23,0 g |
|
Destilovaná voda |
1,0 l |
Rozpusťte složky a sterilujte tlakem při teplotě 121 °C po dobu 15 minut.
Kvasnično-pepton-glukózový agar (YPGA)
|
Kvasnicový extrakt (Difco) |
5,0 g |
|
Bacto-Pepton (Difco) |
5,0 g |
|
D(+) Glukóza (monohydrát) |
10,0 g |
|
Bacto-Agar (Difco) |
15,0 g |
|
Destilovaná voda |
1,0 l |
Rozpusťte složky a sterilujte tlakem při teplotě 121 °C po dobu 15 minut.
Sacharózopeptonový agar (SPA)
|
Sacharóza |
20,0 g |
|
Bacto-Peptone (Difco) |
5,0 g |
|
K2HPO4 |
0,5 g |
|
MgSO4.7H2O |
0,25 g |
|
Bacto-Agar (Difco) |
15,0 g |
|
Destilovaná voda |
1,0 l |
|
pH 7,2–7,4 |
|
Rozpusťte složky a sterilujte v autoklávu při teplotě 121 °C po dobu 15 minut.
Kelmanovo tetrazoliové médium
|
kasein hydrolyzát (Difco) |
1,0 g |
|
Bacto-Pepton (Difco) |
10,0 g |
|
Dextróza |
5,0 g |
|
Bacto-Agar (Difco) |
15,0 g |
|
Destilovaná voda |
1,0 l |
Rozpusťte složky a sterilujte v autoklávu při teplotě 121 °C po dobu 15 minut.
Ochlaďte na 50 °C a přidejte filtrem sterilizovaný roztok 2,3,5-trifenyl-tetrazoliumchloridu (Sigma), až do dosažení konečné koncentrace 50 mg na litr.
b) Validované selektivní živné půdy
Živná půda SMSA (Englebrecht, 1994 ve znění Elphinstone et al., 1996)
|
Základní živná půda |
|
|
Casamino kyseliny (Difco) |
1,0 g |
|
Bacto-Pepton (Difco) |
10,0 g |
|
Glycerol |
5,0 ml |
|
Bacto-Agar (Difco) (viz pozn. 2) |
15,0 g |
|
Destilovaná voda |
1,0 l |
Rozpusťte složky a sterilujte v autoklávu při teplotě 121 °C po dobu 15 minut.
Ochlaďte na 50 °C a přidejte filtrem sterilizovaný vodný roztok následujících složek, abyste získali stanovenou konečnou koncentraci:
|
Krystalová violeť (Sigma) |
5 mg/l |
|
Polymixin-B-sulfát (Sigma P1004) |
600 000 U (přibližně 100 mg)/l |
|
Bacitracin (Sigma B-0125) |
1 250 U (přibližně 25 mg)/l |
|
Chloramfenikol (Sigma C-3175) |
5 mg/l |
|
Penicilín-G (Sigma P-3032) |
825 U (přibližně 0,5 mg)/l |
|
2,3,5-trifenyltetrazolium chlorid (Sigma) |
50 mg/l |
Pozn.:
|
1. |
Použití jiných reagencí výše uvedených může ovlivnit růst R. solanacearum. |
|
2. |
Místo Bacto-Agar (Difco) může být použit Oxoid Agar #1. V takovém případě bude růst R. solanacearum pomalejší, ale může to však také omezit růst konkurenčních saprofytů. Typické kolonie R. solanacearum se mohou tvořit o 1–2 dny déle a červené zbarvení může být světlejší a rozptýlenější při použití Bacto-Agar. |
|
3. |
Zvýšení koncentrace bacitracinu na 2 500 U/l může omezit populace konkurenčních bakterií bez ovlivnění růstu Ralstonia solanacearum. |
Uchovávejte a skladujte roztoky antibiotik při teplotě 4 °C v temnu a spotřebujte do 1 měsíce.
Misky s médiem by měly být před použitím zbaveny povrchové kondenzace.
Zabraňte přílišnému sušení média.
Každá nově připravená šarže živné půdy by měla být podrobena kontrole kvality živné půdy roztěrem suspense referenční kultury R. solanacearum na médium (viz dodatek 3) a pozorováním, zda se po 2 až 5 dnech při teplotě 28 °C objeví typické kolonie.
c) Validované obohacené živné půdy
Živná půda SMSA (Elphinstone et al., 1996)
Proveďte přípravu jako pro selektivní agarovou živnou půdu SMSA, ale vynechte Bacto-Agar a 2,3,5-trifenyltetrazolium chlorid.
Upravená živná půda Wilbrink (Caruso et al., 2002)
|
Sacharóza |
10 g |
|
Proteázový pepton |
5 g |
|
K2HPO4 |
0,5 g |
|
MgSO4 |
0,25 g |
|
NaNO3 |
0,25 g |
|
Destilovaná voda |
1 l |
Sterilujte tlakem při teplotě 121 °C po dobu 15 minut a ochlaďte na 50 °C.
Přidejte antibiotický zásobní roztok jako pro živnou půdu SMSA.
Dodatek 3
A. Komerční standardizovaný kontrolní materiál
a) Izolované bakteriální kultury
Následující izolované bakteriální kultury se doporučují jako standardní referenční materiál buď k pozitivní kontrole (tabulka 1) nebo během optimalizace testů, aby se zabránilo vzájemnému působení (tabulka 2). Všechny kmeny jsou komerčně dostupné a lze je získat z těchto sbírek:
|
1. |
Národní sbírka patogenních bakterií rostlin (NCPPB), Ústřední vědecká laboratoř York, UK. |
|
2. |
Sbírka kultur sekce ochrany rostlin (PD), Wageningen, Nizozemsko. |
|
3. |
Francouzská sbírka patogenních bakterií rostlin (CFBP), Ústav fytobakteriologie INRA, Angers, Francie. |
Tabulka 1 Referenční panel izolovaných bakteriálních kultur SMT R. solanacearum
|
Kód NCPPB |
SMT # |
Jiné kódy |
Země původu |
Biovar |
|
NCPPB 4153 |
6 |
CFBP 4582, Pr 3020, EURS11 |
Egypt |
2 |
|
NCPPB 4154 |
10 |
CFBP 4585, 550, EURS21 |
Turecko |
2 |
|
NCPPB 3857 |
12 |
CFBP 4587, Pr 1140, EURS26 |
Anglie |
2 |
|
NCPPB 1584 |
23 |
CFBP 4598, EURS49 |
Kypr |
2 |
|
NCPPB 2505 |
24 |
CFBP 4599, EURS50 |
Švédsko |
2 |
|
NCPPB 4155 |
26 |
CFBP 4601, 502, EURS55 |
Belgie |
2 |
|
NCPPB 4156 (3) |
71 (3) |
PD 2762, CFBP 3857 |
Nizozemsko |
2 |
|
NCPPB 4157 |
66 |
LNPV 15.59 |
Francie |
2 |
|
NCPPB 4158 |
39 |
CFBP 4608, Port 448, EURS80 |
Portugalsko |
2 |
|
NCPPB 4160 |
69 |
IVIA-1632-2 |
Španělsko |
2 |
|
NCPPB 4161 |
76 |
B3B |
Německo |
2 |
|
NCPPB 325 |
41 |
CFBP 2047, KEL60-1, R842 |
USA |
1 |
|
NCPPB 3967 |
42 |
CFBP 4610, R285, GONg7 |
Kostarika |
1 |
|
NCPPB 4028 |
43 |
CFBP 4611, R303/571, CIP310, SEQ205 |
Kolumbie |
2 |
|
NCPPB 3985 |
44 |
CFBP 4612, R578, CIP312 |
Peru |
2T |
|
NCPPB 3989 |
45 |
CFBP 4613, R568, CIP226 |
Brazílie |
2T |
|
NCPPB 3996 |
46 |
CFBP 3928, R276/355, CIP72, SEQ225 |
Peru |
3 |
|
NCPPB 3997 |
47 |
CFBP 4614, R280/363, CIP49, HAY0131a |
Austrálie |
3 |
|
NCPPB 4029 |
48 |
CFBP 4615, R297/349, CIP121, CMIb2861 |
Srí Lanka |
4 |
|
NCPPB 4005 |
49 |
CFBP 4616, R470 |
Filipíny |
4 |
|
NCPPB 4011 |
50 |
CFBP 4617, R288, HEmps2 |
Čína |
5 |
Pozn.: Spolehlivost výše uvedených kmenů může být zaručena pouze v případě, že pocházejí z původních sbírek kultur.
Tabulka 2 Referenční panel SMT sérologicky nebo geneticky příbuzných bakterií k optimalizaci detekčních testů
|
Kód NCPPB |
SMT # |
Jiné kódy |
Identifikace |
|
NCPPB 4162 |
51 |
CFBP 1954 |
Bacillus polymyxa (4) |
|
NCPPB 4163 |
52 |
CFBP 1538 |
Pseudomonas marginalis pv. marginalis (4) |
|
NCPPB 4164 |
– |
CFBP 2227 |
Burkholderia cepacia (5) |
|
NCPPB 4165 |
– |
CFBP 2459 |
Ralstonia pickettii (5) |
|
NCPPB 4166 |
58 |
CFBP 3567 CSL Pr1150 |
Ralstonia pickettii (4) |
|
NCPPB 4167 |
60 |
CFBP 4618 PD 2778 |
Ralstonia sp. (4) |
|
NCPPB 1127 |
53 |
CFBP 3575 |
Burkholderia andropogonis (4) |
|
NCPPB 353 |
54 |
CFBP 3572 |
Burkholderia caryophylli (4) |
|
NCPPB 945 |
55 |
CFBP 3569 |
Burkholderia cepacia (4) |
|
NCPPB 3708 |
56 |
CFBP 3574 |
Burkholderia glumae (4) |
|
NCPPB 3590 |
57 |
CFBP 3573 |
Burkholderia plantarii (4) |
|
NCPPB 3726 |
59 |
CFBP 3568 |
|
|
NCPPB 4168 |
61 |
CFBP 4619 IPO S339 |
Enterobacter sp. (4) |
|
NCPPB 4169 |
62 |
IPO 1695 |
Enterobacter sp. (4) |
|
NCPPB 4170 |
63 |
CFBP 4621 IPO S306 |
|
|
NCPPB 4171 |
64 |
CFBP 4622 IPO 1693 |
|
|
NCPPB 4172 |
65 |
IPO 1696a |
Pseudomonas sp. (4) |
|
NCPPB 4173 |
– |
PD 2318 |
Aureobacterium sp. (5) |
|
NCPPB 4174 |
81 |
IVIA 1844.06 |
b) Komerční standardizovaný kontrolní materiál
Následující standardní kontrolní materiál je možné získat ze sbírky kultur NCPPB.
Mražené sušené pelety bramborového extraktu ze 200 zdravých hlíz bramboru k negativní kontrole všech testů.
Mražené sušené pelety bramborového extraktu ze 200 zdravých hlíz bramboru obsahující 103 až 104 a 104 až 106 buněk biovaru 2 R. solanacearum (kmen NCPPB 4156 = PD 2762 = CFBP 3857) jako pozitivní kontroly serologických a PCR testů. Protože životaschopnost buňky je ovlivněna lyofilizací, nejsou tyto vhodné jako standardy v testech izolace a testech patogenity.
Ve formaldehydu fixované suspense biovaru 2 R. solanacearum (kmen NCPPB 4156 = PD 2762 = CFBP 3857) s 106 buňkami na 1 ml k pozitivní kontrole sérologických testů.
B. Příprava pozitivních a negativních kontrol pro screeningové testy vodivých pletiv PCR/IF a FISH
Kultivujte 48hodinovou kulturu virulentního kmene R. solanacearum rasy 3/biovaru 2 (např. kmen NCPPB 4156 = PD 2762 = CFBP 3857) na SMSA živné půdě a suspendujte v 10 mM fosfátovém pufru, abyste získali buněčnou hustotu přibližně 2 × 108 cfu na 1 ml. Obvykle se jí dosáhne jemně zakalenou suspenzí rovnající se optické hustotě 0,15 při 600 nm.
Odeberte dřeň z pupkových konců 200 hlíz z produkce odrůdy s bílou slupkou, o které víte, že je prosta R. solanacearum.
Zpracujte pupkové konce výše uvedeným postupem a resuspendujte peletu v 10 ml.
Připravte 10 sterilních 1,5 ml mikrozkumavek s 900 µl resuspendované pelety.
Přeneste 100 µl suspenze R. solanacearum do první mikrozkumavky. Protřepejte.
Proveďte desetinásobné ředění v dalších pěti mikrozkumavkách.
Těchto šest kontaminovaných mikrozkumavek bude použito jako kontrolní pozitivní vzorky. Čtyři nekontaminované mikrozkumavky budou použity jako kontrolní negativní vzorky. Mikrozkumavky řádně označte.
Připravte poměrné díly 100 µl ve sterilních 1,5 ml mikrozkumavkách, čímž získáte 9 kopií téhož kontrolního vzorku. Uskladněte při teplotě –16 až –24 °C do dalšího použití.
Přítomnost a množství organismu R. solanacearum v kontrolních vzorcích by měly být nejdříve potvrzeny testem IF.
Pro účely testu PCR proveďte extrakci DNA z pozitivních a negativních kontrolních vzorků u každé série testovacích vzorků.
Pro účely testů IF a FISH proveďte test patogenity na pozitivních a negativních kontrolních vzorcích u každé série testovacích vzorků.
Co se týče testů IF, FISH a PCR, organismus R. solanacearum musí být detekován nejméně v počtu 106 a 104 buněk/ml u pozitivních kontrolních vzorků a u žádných vzorků negativní kontroly.
Dodatek 4
Pufry pro testovací postupy
OBECNĚ: Neotevřené sterilizované pufry mohou být uchovány až jeden rok.
1. Pufry pro účely extrakce
1.1 Extrakční pufr (50 mM fosfátový pufr, pH 7,0)
Tento pufr se používá k extrakci bakterií z rostlinných pletiv homogenizací nebo třepáním.
|
Na2HPO4 (bezvodý) |
4,26 g |
|
KH2PO4 |
2,72 g |
|
Destilovaná voda |
1,00 l |
Rozpusťte složky, zkontrolujte pH a sterilizujte v autoklávu při teplotě 121 °C po dobu 15 minut.
Užitečné mohou být následující pomocné složky:
|
|
Účel |
Množství (/l) |
|
Vločky Lubrol |
protisrážlivý prostředek (7) |
0,5 g |
|
Silikonový odpěňovací prostředek DC |
Odpěňovací prostředek (7) |
1,0 ml |
|
Tetrasodiumpyrofosfát |
Antioxidační prostředek |
1,0 g |
|
Polyvinylpyrrolidone-40000 (PVP-40) |
Váže inhibitory PCR |
50 g |
1.2 Peletový pufr (10 mM fosfátový pufr, pH 7,2)
Tento pufr se používá k resuspenzi a ředění extraktů z výkrojků pupkových konců hlíz bramboru po jejich zahuštění do formy pelety odstředěním.
|
Na2HPO4.12H2O |
2,7 g |
|
NaH2PO4.2H2O |
0,4 g |
|
Destilovaná voda |
1,0 l |
Rozpusťte složky, zkontrolujte pH a sterilizujte autoklávováním při teplotě 121 °C po dobu 15 minut.
2. Pufry pro IF test
2.1 Pufr IF (10 mM roztok chloridu sodného pufrovaný fosfátem (PBS), pH 7,2)
Tento pufr se používá k ředění protilátek
|
Na2HPO4.12H2O |
2,7 g |
|
NaH2PO4.2H2O |
0,4 g |
|
NaCl |
8,0 g |
|
Destilovaná voda |
1,0 l |
Rozpusťte složky, zkontrolujte pH a sterilizujte autoklávováním při teplotě 121 °C po dobu 15 minut.
2.2 Pufr IF-Tween
Tento pufr se používá k oplachování podložních sklíček.
Přidejte 0,1 % Tween 20 do pufru IF.
2.3 Fosfátový pufr s glycerolem, pH 7,6
Tento pufr se používá jako krycí tekutina/roztok na podložní sklíčko ke zvýšení fluorescence.
|
Na2HPO4.12H2O |
3,2 g |
|
NaH2PO4.2H2O |
0,15 g |
|
Glycerol |
50 ml |
|
Destilovaná voda |
100 ml |
Krycí roztoky např Vectashield® (laboratoře Vector Laboratories) nebo Citifluor® (Leica) jsou dostupné na trhu.
3. Pufry pro účely nepřímého testu ELISA
3.1 Dvojnásobný uhličitanový potahovací pufr, pH 9,6.
|
Na2CO3 |
6,36 g |
|
NaHCO3 |
11,72 g |
|
Destilovaná voda |
1,00 l |
Rozpusťte složky, zkontrolujte pH a sterilujte autoklávováním při teplotě 121 °C po dobu 15 minut.
Pokud extrakt obsahuje vysoký podíl aromatických molekul, je možné jako antioxidant přidat siřičitan sodný (0,2 %).
3.2 Desetinásobný roztok chloridu sodného pufrovaný fosfátem (10X PBS), pH 7,4
|
NaCl |
80,0 g |
|
KH2PO4 |
2,0 g |
|
Na2HPO4.12H2O |
29,0 g |
|
KCl |
2,0 g |
|
Destilovaná voda |
1,0 l |
3.3 PBS-Tween
|
10X PBS |
100 ml |
|
10 % Tween 20 |
5 ml |
|
Destilovaná voda |
895 ml |
3.4 Blokační pufr (musí být čerstvě připraven).
|
10X PBS |
10,0 ml |
|
Polyvinylpyrrolidin-44000 (PVP-44) |
2,0 g |
|
10 % Tween 20 |
0,5 ml |
|
Sušené mléko |
0,5 g |
|
Destilovaná voda |
doplnit do 100 ml |
3.5 Roztok pro substrát alkalické fosfatázy, pH 9,8
|
Diethanolamin |
97 ml |
|
Destilovaná voda |
800 ml |
Rozpustíme a koncentrovanou HCl upravíme pH na 9,8.
Doplňte do 1 l destilovanou vodou.
Přidejte 0,2 g MgCl2.
Rozpusťte dvě 5 mg tabletky fosfatázového substrátu (Sigma) v 15 ml roztoku.
4. Pufry pro účely testu DASI ELISA
4.1 Potahovací pufr, pH 9,6.
|
Na2CO3 |
1,59 g |
|
NaHCO3 |
2,93 g |
|
Destilovaná voda |
1 000 ml |
Rozpusťte složky a zkontrolujte pH 9,6.
4.2 10X fosfátosolný pufr (PBS) pH 7,2– 7,4
|
NaCl |
80,0 g |
|
NaH2PO4.2 H2O |
4,0 g |
|
Na2HPO4.12H2O |
27,0 g |
|
Destilovaná voda |
1 000 ml |
4.3 PBS-Tween
|
10X PBS |
50 ml |
|
10 % Tween 20 |
5 ml |
|
Destilovaná voda |
950 ml |
4.4 Substrátový pufr, pH 9,8
|
Diethanolamin |
100 ml |
|
Destilovaná voda |
900 ml |
Smíchejte a nastavte hodnotu pH 9,8 koncentrovanou HCl.
Dodatek 5
Stanovení koncentrace IF a FISH pozitivních buněk
|
1. |
Spočítejte průměrný počet typických fluoreskujících buněk v jednom pozorovacím poli (c). |
|
2. |
Spočítejte počet typických fluoreskujících buněk v 1 okénku mikroskopického sklíčka (C). C = c × S/s
|
|
3. |
Vypočtěte počet typických fluorescenčních buněk na 1 ml resuspendované pelety (N). N = C × 1 000/y × F
|
Dodatek 6
Validované protokoly a reagencie PCR
Pozn.: Předběžné testování by mělo umožnit reprodukovatelnou detekci asi 103 až 104 buněk R. solanacearum na 1 ml vzorkového extraktu.
Předběžné testování by rovněž nemělo ukázat žádné falešně pozitivní výsledky na panelu vybraných bakteriálních kmenů (viz dodatek 3).
1. Protokol PCR Seal et al. (1993)
1.1 Oligonukleotidové primery
|
Přímý primer OLI-1 |
5′-GGG GGT AGC TTG CTA CCT GCC-3′ |
|
Reverzní primer Y-2 |
5′-CCC ACT GCT GCC TCC CGT AGG AGT-3′ |
Očekávaná velikost amplikonu templátové DNA R. solanacearum = 288 bp
1.2 Reakční směs PCR
|
Reagencie |
Množství v reakci |
Konečná koncentrace |
|
Sterilní UPW |
17,65 µl |
|
|
10X pufr PCR (8) (15 mM MgCl2) |
2,5 µl |
1X (1,5 mM MgCl2) |
|
Směs dNTP (20mM) |
0,25 µl |
0,2 mM |
|
Primer OLI-1 (20 µM) |
1,25 µl |
1µM |
|
Primer Y-2 (20 µM) |
1,25 µl |
1µM |
|
Taq polymerasa (5U/µl) (8) |
0,1 µl |
0,5 U |
|
Množství vzorku |
2,0 µl |
|
|
Celkové množství: |
25 µl |
|
1.3 Reakční podmínky PCR
Proveďte následující cyklický proces:
|
1 cyklus: |
i) |
2 minuty při 96 °C (denaturace templátové DNA) |
|
35 cyklů: |
ii) |
20 sekund při 94 °C (denaturace templátové DNA) |
|
|
iii) |
20 sekund při 68 °C (hybridizace primerů s templátovou DNA) |
|
|
iv) |
30 sekund při 72 °C (syntéza kopie) |
|
1 cyklus: |
v) |
10 minut při 72 °C (závěrečná syntéza) |
|
|
vi) |
ponechte při teplotě 4 °C. |
Pozn.: Tento program byl optimalizován pro použití termocykleru Perkin Elmer 9600. Použití jiných přístrojů může vyžadovat úpravu jednotlivých kroků cyklu ii), iii) a iv).
1.4 Restrikční enzymová analýza amplikonu.
Produkty PCR vzniklé amplifikací z R. solanacearum DNA vytvářejí polymorfismus délky restrikčních fragmentů s enzymem Ava II po inkubaci při teplotě 37 °C.
2. Protokol PCR Pastrika a Maisse (2000)
2.1 Oligonukleotidové primery
|
Přímý primer Ps-1 |
5′-agt cga acg gca gcg ggg g -3′ |
|
Reverzní primer Ps-2 |
5′-ggg gat ttc aca tcg gtc ttg ca -3′ |
Očekávaná velikost amplikonu templátové DNA R. solanacearum DNA = 553 bp.
2.2 Reakční směs PCR
|
Reagencie |
Množství v reakci |
Finální koncentrace |
|
Sterilní UPW |
16,025 µl |
|
|
10X pufr PCR (9) |
2,5 µl |
1X (1,5 mM MgCl2) |
|
BSA (frakce V) (10 %) |
0,25 µl |
0,1 % |
|
Směs dNTP (20mM) |
0,125 µl |
0,1 mM |
|
Primer Ps-1 (10 µM) |
0,5 µl |
0,2 µM |
|
Primer Ps-2 (10 µM) |
0,5 µl |
0,2 µM |
|
Taq polymerasa (5U/µl) (9) |
0,1 µl |
0,5 U |
|
Množství vzorku |
5,0 µl |
|
|
Celkové množství: |
25,0 µl |
|
|
Pozn.: Původně optimalizovaná pro termocykler MJ Research PTC 200 s polymerasou Gibco Taq Polymerace. Perkin Elmer AmpliTaq a pufr mohou být rovněž použity ve stejných koncentracích. |
||
2.3 Reakční podmínky PCR
Proveďte následující cyklický proces:
|
1 cyklus: |
i) |
5 minut při 95 °C (denaturace templátové DNA) |
|
35 cyklů: |
ii) |
30 sekund při 95 °C (denaturace templátové DNA) |
|
|
iii) |
30 sekund při 68 °C (hybridizace primerů s templátovou DNA) |
|
|
iv) |
45 sekund při 72 °C (syntéza kopie) |
|
1 cyklus: |
v) |
5 minut při 72 °C (syntéza extenze) |
|
|
vi) |
ponechte při teplotě 4 °C. |
Pozn.: Tento program byl optimalizován pro použití termocykleru MJ Research PTC 200. Použití jiných přístrojů bude možná vyžadovat úpravu jednotlivých kroků cyklu ii), iii) a iv).
2.4 Restrikční enzymová analýza amplikonu.
Produkty PCR vzniklé amplifikací z R. solanacearum DNA vytvářejí zřetelný polymorfismus délky restrikčních fragmentů s enzymem Taq I po inkubační době 30 minut při teplotě 65 °C. Restrikční fragmenty specifické pro R. solanacearum mají velikost 457 bp a 96 bp.
3. Protokol pro multiplexní PCR s interní kontrolou (Pastrik et al., 2002)
3.1 Oligonukleotidové primery
|
Přímý primer RS-1-F |
5′-ACT AAC GAA GCA GAG ATG CAT TA-3′ |
|
Reverzní primer RS-1-R |
5′-CCC AGT CAC GGC AGA GAC T-3′ |
|
Přímý primer NS-5-F |
5′-AAC TTA AAG GAA TTG ACG GAA G-3′ |
|
Reverzní primerNS-6-R |
5′-GCA TCA CAG ACC TGT TAT TGC CTC-3′ |
Očekávaná velikost amplikonu templátové DNA R. solanacearum = 718 bp (sada primerů RS).
Očekávaná velikost amplikonu interní kontroly PCR 18S rRNA = 310 bp (sada primerů NS).
3.2 Reakční směs PCR
|
Reagencie |
Množství v reakci |
Finální koncentrace |
|
Sterilní UPW |
12,625 µl |
|
|
10X pufr PCR (10) (15 mM MgCl2) |
2,5 µl |
1X (1,5 mM MgCl2) |
|
BSA (frakce V) (10 %) |
0,25 µl |
0,1 % |
|
Směs dNTP (20mM) |
0,125 µl |
0,1 mM |
|
Primer RS-1-F (10µM) |
2,0 µl |
0,8 µM |
|
Primer RS-1-R (10µM) |
2,0 µl |
0,8 µM |
|
Primer NS-5-F (10µM) (11) |
0,15 µl |
0,06 µM |
|
Primer NS-6-R (10µM) (11) |
0,15 µl |
0,06 µM |
|
Taq polymeráza (5U/µl) (10) |
0,2 µl |
1,0 U |
|
Množství vzorku |
5,0 µl |
|
|
Celkové množství: |
25,0 µl |
|
3.3 Reakční podmínky PCR
Proveďte následující cyklický proces:
|
1 cyklus: |
i) |
5 minut při 95 °C (denaturace templátové DNA) |
|
35 cyklů: |
ii) |
30 sekund při 95 °C (denaturace templátové DNA) |
|
|
iii) |
30 sekund při 58 °C (hybridizace primerů s templátovou DNA) |
|
|
iv) |
45 sekund při 72 °C (syntéza kopie) |
|
1 cyklus: |
v) |
5 minut při 72 °C (konečná syntéza) |
|
|
vi) |
nechte při teplotě 4 °C. |
Pozn.: Tento program byl optimalizován pro použití termocykleru MJ Research PTC 200. Použití jiných přístrojů může vyžadovat úpravu jednotlivých kroků cyklu ii), iii) a iv).
3.4 Restrikční enzymová analýza amplikonu.
Produkty PCR vzniklé amplifikací z DNA R. solanacearum vytvářejí zřetelný polymorfizsmus délky restrikčních fragmentů s enzymem Bsm I nebo Isoschizomere (např. Mva 1269 I) po inkubační době 30 minut při teplotě 65 °C.
4. Protokol PCR specifický pro biovar R. solanacearum (Pastrik et al, 2001)
4.1 Oligonukleotidové primery
|
Přímý primer Rs-1-F |
5′-ACT AAC GAA GCA GAG ATG CAT TA-3′ |
|
Reverzní primer Rs-1-R |
5′-CCC AGT CAC GGC AGA GAC T-3′ |
|
Reverzní primer Rs-3-R |
5′-TTC ACG GCA AGA TCG CTC-3′ |
Očekávaná velikost amplikonu templátové DNA R. solanacearum:
s Rs-1-F/Rs-1-R = 718 bp
s Rs-1-F/Rs-3-R = 716 bp
4.2 Reakční směs PCR
|
a) |
Protokol PCR specifický pro biovar 1/2
|
|
b) |
Protokol PCR specifický pro Biovar 3/4/5
|
4.3 Reakční podmínky PCR
Proveďte následující cyklický proces pro obě reakce specifické pro biovary 1/2- a biovary 3/4/5:
|
1 cyklus: |
i) |
5 minut při 95 °C (denaturace templátové DNA) |
|
35 cyklů: |
ii) |
30 sekund při 95 °C (denaturace templátové DNA) |
|
|
iii) |
30 sekund při 58 °C (hybridizace primerů s templátovou DNA) |
|
|
iv) |
45 sekund při 72 °C (syntéza kopie) |
|
1 cyklus: |
v) |
5 minut při 72 °C (konečná syntéza) |
|
|
vi) |
ponechte při teplotě 4 °C. |
Pozn.: Tento program byl optimalizován pro použití termocykleru MJ Research PTC 200. Použití jiných přístrojů může vyžadovat úpravu jednotlivých kroků cyklu ii), iii) a iv).
4.4 Restrikční enzymová analýza amplikonu.
Produkty PCR vzniklé amplifikací DNA R. solanacearum pomocí primerů Rs-1-F a Rs-1-R vytvářejí zřetelný polymorfizmus délky restrikčních fragmentů s enzymem Bsm I nebo Isoschizomere (např. Mva 1269 I) po inkubační době 30 minut při teplotě 65 °C. Produkty PCR vzniklé amplifikací z DNA R. solanacearum pomocí primerů Rs-1-F a Rs-3-R nemají žádná restrikční místa.
5. Příprava nanášecího pufru
5.1 Bromfenolová modř (10 % zásobní roztok)
|
Bromfenolová modř |
5 g |
|
Destilovaná voda (redestilovaná) |
50 ml |
5.2 Nanášecí pufr
|
Glycerol (86 %) |
3,5 ml |
|
Bromfenolová modř (5.1) |
300 µl |
|
Destilovaná voda (redestilovaná) |
6,2 ml |
6. Pufr 10X Tris -Acetát -EDTA (TAE), pH 8,0
|
Tris |
48,40 g |
|
Ledová kyselina octová |
11,42 ml |
|
EDTA (disodium salt) |
3,72 g |
|
Destilovaná voda |
1,00 l |
Před použitím řeďte na 1X.
Rovněž dostupný na trhu (např. Invitrogen nebo rovnocenný).
Dodatek 7
Validované reagencie pro test FISH
1. Oligosondy
Sonda specifická pro R. solanacearum OLI-1-CY3 5′-ggc agg tag caa gct acc ccc-3′
Nespecifická eubakteriální sonda EUB-338-FITC 5′-gct gcc tcc cgt agg agt-3′
2. Fixační roztok
[UPOZORNĚNÍ: USTALOVAČ JE PARAFORMALDEHYD, KTERÝ JE JEDOVATÝ. POUŽIJTE RUKAVICE A NEVDECHNĚTE. DOPORUČUJE SE PRACOVAT V DIGESTOŘI.]
|
i) |
Zahřejte 9 ml ultračisté vody (UPW) na zhruba 60 °C a přidejte 0,4 g paraformaldehydu. Paraformaldehyd se rozpouští po přidání 5 kapek 1N NaOH a míchání na magnetické míchačce. |
|
ii) |
Upravte pH na 7,0 přidáním 1 ml 0,1 M fosfátového pufru (PB; pH 7,0) a 5 kapek 1N HCl. Zkontrolujte pH indikátorovými papírky a případně upravte HCl nebo NaOH. [UPOZORNĚNÍ: V ROZTOKU S PARAFORMAL-DEHYDEM NEPOUŽÍVEJTE MĚŘIČ PH.] |
|
iii) |
Zfiltrujte roztok přes membránový filtr 0,22 µm a uchovejte chráněný před prachem při teplotě 4 °C do dalšího použití. |
3. 3X Hybmix
|
NaCl |
2,7 M |
|
Tri-HCl |
60 mM (pH 7,4) |
|
EDTA (sterilizovaný filtrací a autoklávováním) |
15 mM |
Zřeďte na 1X, podle potřeby.
4. Hybridizační roztok
|
1X Hybmix |
|
|
Dodecylsíran sodný (SDS) |
0,01 % |
|
Formamid |
30 %, |
|
Sonda EUB 338 |
5 ng/μl |
|
Sonda OLI-1 nebo OLI-2 |
5 ng/μl |
Připravte množství hybridizačního roztoku podle výpočtů v tabulce 1. Na každé podložní sklíčko (obsahující dva různé vzorky dvakrát) se požaduje 90 μl hybridizačního roztoku. UPOZORNĚNÍ: FORMAMID JE VELMI JEDOVATÝ, A PROTO POUŽIJTE RUKAVICE A UČIŇTE POTŘEBNÁ BEZPEČNOSTNÍ OPATŘENÍ!
Tabulka 1. Doporučená množství pro přípravu hybridizační směsi.
|
Počet sklíček: |
1 |
4 |
6 |
8 |
10 |
|
Sterilní ultra čistá voda |
23,1 |
92,4 |
138,6 |
184,8 |
231,0 |
|
3x hybmix |
30,0 |
120,0 |
180,0 |
240,0 |
300,0 |
|
1 % SDS |
0,9 |
3,6 |
5,4 |
7,2 |
9,0 |
|
Formamid |
27,0 |
108,0 |
162,0 |
216,0 |
270,0 |
|
Sonda EUB 338 (100 ng/μl) |
4,5 |
18,0 |
27,0 |
36,0 |
45,0 |
|
Sonda OLI-1 nebo OLI-2 (100 ng/μl) |
4,5 |
18,0 |
27,0 |
36,0 |
45,0 |
|
Celkové množství (μl) |
90,0 |
360,0 |
540,0 |
720,0 |
900,0 |
|
Pozn.: Uchovávejte všechny roztoky se světlocitlivými oligosondami v temnu při teplotě –20 °C. Při použití chraňte před přímým slunečním nebo elektrickým světlem. |
|||||
5. 0,1M fosfátový pufr, pH 7,0
|
Na2HPO4 |
8,52 g |
|
KH2PO4 |
5,44 g |
|
Destilovaná voda |
1,00 l |
Rozpusťte složky, zkontrolujte pH a autoklávujte při teplotě 121 °C po dobu 15 minut.
Dodatek 8
Pěstování lilku a rajčete
Zasejte semena rajčete (Lycopersicon esculentum) nebo lilku (Solanum melongena) do pasterizovaného výsevního substrátu. Přesaďte sazeničky s plně rozvinutými děložními listy (10 až 14 dní) do pasterizovaného pěstebního substrátu.
Rostliny lilku a rajčete by měly být před naočkováním pěstovány ve skleníku s následujícími podmínkami:
|
Délka dne |
14 hodin nebo přirozená délka dne nebo delší |
|
Teplota |
denní: 21 až 24 °C noční: 14 až 18 °C |
|
Vhodná odrůda rajčete |
‚Moneymaker‘ |
|
Vhodná odrůda lilku |
‚Black Beauty‘ |
|
Dodavatelé: |
viz internetová stránka http://forum.europa.eu.int/Public/irc/sanco/Home/main |
LITERATURA
|
1. |
Amann, R.I., L. Krumholz and D.A. Stahl. 1990. Fluorescent-oligonucleotide probing of whole cells for determinative, phylogenetic and environmental studies in microbiology. J. Bacteriol. 172: 762-770. |
|
2. |
Anon. 1998. Council Directive 98/57/EC of 20 July 1998 on the control of Ralstonia solanacearum (Smith) Yabuuchi et al. Official Journal of the European Communities L235, 1-39. |
|
3. |
Boudazin, G., A.C. Le Roux, K. Josi, P. Labarre and B. Jouan. 1999. Design of division specific primers of Ralstonia solanacearum and application to the identification of European isolates. European Journal of Plant Pathology 105; 373-380. |
|
4. |
Caruso, P., Gorris, M.T., Cambra, M., Palomo, J.L., Collar, J and Lopez, M.M. 2002. Enrichment Double-Antibody Sandwich Indirect Enzyme-Linked Immunosorbent Assay That Uses a Specific Monoclonal Antibody for sensitive Detection of Ralstonia solanacearum in Asymptomatic Potato Tubers. Applied and Environmental Microbiology, 68, 3634-3638. |
|
5. |
Cook, D., Barlow, E. and Sequeira, L. 1989. Genetic diversity of Pseudomonas solanacearum: detection of restriction fragment length polymorphisms with DNA probes that specify virulence and the hypersensitive response. Molecular Plant-Microbe Interactions 1:113-121. |
|
6. |
Elphinstone, J.G., Hennessy, J., Wilson, J.K. and Stead, D.E. 1996. Sensitivity of detection of Ralstonia solanacearum in potato tuber extracts. EPPO Bulletin 26; 663-678. |
|
7. |
Englebrecht, M.C. (1994) Modification of a semi-selective medium for the isolation and quantification of Pseudomonas solanacearum. In: A.C. Hayward (ed.) Bacterial Wilt Newsletter 10, 3-5. Australian Centre for International Agricultural Research, Canberra, Australia. |
|
8. |
Hayward, A.C. 1964. Characteristics of Pseudomonas solanacearum. Journal of Applied Bacteriology 27; 265-277. |
|
9. |
Hayward, A.C., El-Nashaar, H.M., Nydegger, U. and De Lindo, L. 1990. Variation in nitrate metabolism in biovars of Pseudomonas solanacearum. Journal of Applied Bacteriology 69; 269-280. |
|
10. |
Ito, S., Y. Ushijima, T. Fujii, S. Tanaka, M. Kameya-Iwaki, S. Yoshiwara and F. Kishi. 1998. Detection of viable cells of Ralstonia solanacearum in soil using a semi-selective medium and a PCR technique. J. Phytopathology 146; 379-384. |
|
11. |
Janse, J.D. (1988) A detection method for Pseudomonas solanacearum in symptomless potato tubers and some data on its sensitivity and specificity. Bulletin OEPP/EPPO Bulletin 18, 343-351. |
|
12. |
Janse, J.D. 1991. Infra- and intra-specific classification of Pseudomonas solanacaerum strains using whole cell fatty-acid analysis. Systematic and Applied Microbiology 14; 335-345. |
|
13. |
Kelman, A. 1954. The relationship of pathogenicity of Pseudomonas solanacearum to colony appearance on a tetrazolium medium. Phytopathology 44; 693-695. |
|
14. |
Klement Z.; Rudolph, K and D.C. Sands, 1990. Methods in Phytobacteriology. Akadémiai Kiadó, Budapest, 568 pp. |
|
15. |
Lelliott, R.A. and Stead, D.E. 1987. Methods for the diagnosis of bacterial diseases of plants. Blackwell scientific Publications Ltd., Oxford. 216 pp. |
|
16. |
Lopez, M.M., Gorris, M.T., Llop, P., Cubero, J., Vicedo, B., Cambra, M., 1997. Selective enrichment improves selective isolation, serological and molecular detection of plant pathogenic bacteria. In: H.W. Dehne et al., (eds). Klewer Academic Publishers. pp. 117-121. |
|
17. |
Louws, F.J., Fulbright, D.W., Stephens, C.T. and De Bruijn, F.J., 1994. Specific genomic fingerprints of phytopathogenic Xanthomonas and Pseudomonas pathovars and strains generated with repetitive sequences and PCR. Applied and Environmental Microbiology, 60, 2286-2295. |
|
18. |
Louws, F.J., Fulbright, D.W., Stephens, C.T. and De Bruijn, F.J. 1995. Differentiation of genomic structure by rep-PCR fingerprinting to rapidly classify Xanthomonas campestris pv. vesicatoria. Phytopathology 85; 528-536. |
|
19. |
Opina, N., F. Tavner, G. Holloway, J.-F Wang, T.-H Li, R. Maghirang, M. Fegan, A.C. Hayward, V. Krishnapillai, W.F. Hong, B.W. Holloway, J.N. Timmis. 1997. A novel method for development of species and strain-specific DNA probes and PCR primers for identifying Burkholderia solanacearum (formerly Pseudomonas solanacearum). As Pac. J. Mol. Biol. Biotechnol. 5; 19-33. |
|
20. |
Pastrik, K.H. and Maiss, E. 2000. Detection of R. solanacearum in potato tubers by polymerase chain reaction. J. Phytopathology 148; 619-626. |
|
21. |
Pastrik, K.H., Elphinstone, J.G. and Pukall, R. 2002. Sequence analysis and detection of Ralstonia solanacearum by multiplex PCR amplification of 16S-23S ribosomal intergenic spacer region with internal positive control. European Journal of Plant Pathology 108, 831-842. |
|
22. |
Robinson-Smith, A., Jones, P., Elphinstone, J.G. and Forde, S.M.D. (1995) Production of antibodies to Pseudomonas solanacearum, the causative agent of bacterial wilt. Food and Agricultural Immunology 7, 67-79. |
|
23. |
Schaad, W. 2001. Laboratory guide for identification of plant pathogenic bacteria. Schaad [Hrsg.]. - 3. ed.; St. Paul, Minnesota: 373 pp. |
|
24. |
Seal, S.E., L.A. Jackson, J.P.W. Young, and M.J. Daniels. 1993. Detection of Pseudomonas solanacearum, Pseudomonas syzygii, Pseudomonas pickettii and Blood Disease Bacterium by partial 16S rRNA sequencing: construction of oligonucleotide primers for sensitive detection by polymerase chain reaction. J. Gen. Microbiol. 139: 1587-1594. |
|
25. |
Smith, J.J., Offord, L.C., Holderness, M. and Saddler, G.S. 1995. Genetic diversity of Burkholderia solanacearum (synonym Pseudomonas solanacearum) race 3 in Kenya. Applied and Environmental Microbiology 61; 4262-4268. |
|
26. |
Stead, D.E. 1992. Grouping of plant pathogenic and some other Pseudomonas spp. using cellular fatty-acid profiles. International Journal of Systematic Bacteriology 42; 281-295. |
|
27. |
Taghavi, M., Hayward, A.C., Sly, L.I., Fegan, M. 1996. Analysiss of the phylogenetic relationships of strains of Burkholderia solanacearum, Pseudomonas syzygii, and the blood disease bacterium of banana based on 16S rRNA gene sequences. International Journal of Systematic Bacteriology 46; 10-15. |
|
28. |
Van Der Wolf, J.M., Bonants, P.J.M., Smith, J.J., Hagenaar, M., Nijhuis, E., Van Beckhoven, J.R.C., Saddler, G.S., Trigalet, A., Feuillade, R. 1998. Genetic diversity of Ralstonia solanacearum Race 3 in Western Europe as determined by AFLP, RC-PFGE and rep-PCR. In: Prior, P., Allen, C. and Elphinstone, J. (eds.) Bacterial wilt disease: Molecular and Ecological Aspects. Springer (Berlin) pp. 44-49. |
|
29. |
Weller, S.A., Elphinstone, J.G., Smith, N., Stead, D.E. and Boonham, N. 1999. Detection of Ralstonia solanacearum strains using an automated and quantitative flourogenic 5’ nuclease TaqMan assay. Applied and Environmental Microbiology 66; 2853-2858. |
|
30. |
Wullings, B.A., A.R. van Beuningen, J.D. Janse and A.D.L. Akkermans. 1998. Detection of R. solanacearum, which causes brown rot of potato, by fluorescent in situ hybridization with 23s rRNA-targeted probes. Appl. Environ. Microbiol. 64: 4546-4554. |
PŘÍLOHA III
|
1. |
Ve všech případech podezření z výskytu organismu, kdy screeningový(é) test(y) provedený(é) na uvedeném rostlinném materiálu podle vhodných metod popsaných v příloze II dopadl(y) pozitivně a na potvrzení nebo vyvrácení výsledku(ů) uvedenou metodou se ještě čeká, je třeba zadržet a vhodným způsobem konzervovat:
Uschování hlíz umožní v případě potřeby použít jinou metodu testování/Zadržení hlíz umožní případné testování odrůd. |
|
2. |
V případě potvrzení výskytu škodlivého organismu je třeba zadržet a vhodným způsobem konzervovat nejméně do jednoho měsíce od oznámení podle čl. 5 odst. 2:
|
PŘÍLOHA IV
Prvky šetření podle čl. 5 odst. 1 písm. a) bodu i) v závažných případech zahrnují:
|
i) |
místa produkce,
|
|
ii) |
povrchová voda použitá pro zavlažování nebo postřik polí nebo místa (míst) produkce nebo která zaplavila pole nebo místo (místa) produkce, u kterých se potvrdilo zamoření organismem. |
PŘÍLOHA V
|
1. |
Prvky, jež mají být zohledněny při stanovení rozsahu pravděpodobného zamoření podle čl. 5 odst. 1 písm. a) bod iii) a čl. 5 odst. 1 písm. c) bod iii), zahrnují:
|
|
2. |
Prvky, jež mají být zohledněny při určování možného rozšíření podle čl. 5 odst. 1 písm. a) bodu iv) a čl. 5 odst. 1 písm. c) bodu iii), zahrnují:
|
|
3. |
Oznámení, na které odkazuje první pododstavec čl. 5 odst. 2, zahrnuje:
Poskytnutí těchto informací se neprodleně oznámí Komisi. |
|
4. |
Podrobné dodatečné oznámení, na které odkazuje druhý pododstavec čl. 5 odst. 2, musí obsahovat toto: po dokončení všech šetření a u každého případu:
|
PŘÍLOHA VI
|
1. |
Opatření uvedená v čl. 6. odst. 1 jsou následující:
Jakýkoli zbývající odpad související s výše uvedenými možnostmi nebo vzniklý z výše uvedených možností se musí neškodně odstranit úředně schválenými metodami podle přílohy VII této směrnice. |
|
2. |
Vhodné použití nebo likvidace uvedeného rostlinného materiálu podle čl. 6 odst. 2 pod dohledem příslušných úředních subjektů daného členského státu (států), při jejich vzájemném informování za účelem zajištění kontroly v kterémkoliv okamžiku a se souhlasem příslušného úředního subjektu členského státu, v němž se brambory mají balit nebo zpracovávat, s ohledem na zařízení k odstraňování odpadů uvedená v první a druhé odrážce, zahrnuje:
|
|
3. |
Vhodné metody dekontaminace předmětů uvedených v čl. 6 odst. 3 zahrnují očistu a případnou desinfekci tak, aby nehrozilo žádné zjistitelné riziko šíření tohoto organismu; tato opatření se provádějí pod dohledem příslušných úředních subjektů členských států. |
|
4. |
Soubor opatření, uvedených v čl. 6 odst. 4, která přijmou členské státy v zóně vymezené podle čl. 5 odst. 1 písm. a) bodu iv) a písm. c) bodu iii), zahrnuje: |
|
4.1 |
Jestliže byla místa produkce prohlášena za zamořená podle čl. 5 odst. 1 písm. a) bodu ii):
|
|
4.2 |
Ve vymezené zóně, aniž budou dotčena ustanovení uvedená v bodu 4.1, členské státy:
|
PŘÍLOHA VII
Úředně schválené metody odstraňování odpadu podle přílohy VI odstavce 1 musí splňovat následující ustanovení, aby bylo vyloučeno jakékoli zjistitelné riziko šíření organismu:
|
i) |
bramborový a rajčatový odpad (včetně vyřazených brambor a bramborových slupek a rajčat) a jiný pevný odpad související s bramborami a rajčaty (včetně půdy, kamenů a jiných nečistot) se odstraní takto:
|
|
ii) |
tekutý odpad: před likvidací musí být tekutý odpad obsahující suspendované pevné částice podroben filtraci nebo sedimentaci za účelem odstranění těchto pevných částic. Tyto pevné částice musí být odstraněny podle pododstavce i). Následně musí být tekutý odpad buďto:
|
Možnosti popsané v této příloze se použijí také na odpad spojený s manipulací, odstraněním a zpracováním zamořených partií.
(1) Viz Lelliott a Stead (1987).
(2) Kontakty: viz internetová stránka .
(3) Použijte jako standardní referenční kmen R. solanacearum biovar 2 (rod 3).
(4) Potencionální křížově reagující kmen v sérologických testech (IF a/nebo ELISA) s polyklonálním antisérem.
(5) Kmen, ze kterého lze v některých laboratořích amplifikovat produkt PCR na podobnou velikost, jako je očekávaná velikost při použití specifických primerů OLI-1 a Y-2 (viz dodatek 6).
(6) Pravděpodobnost křížové reakce ve většině testů, ale výskyt znám pouze u banánů v Indonésii.
(7) Pro účely homogenizační extrakční metody.
(8) Metoda byla validována použitím Taq polymerázy Perkin Elmer (AmpliTaq) a Gibco BRL.
(9) Metoda byla validována použitím Taq polymerázy Perkin Elmer (AmpliTaq) a Gibco BRL.
Pozn.: Původně optimalizovaná pro termocykler MJ Research PTC 200 s polymerasou Gibco Taq Polymerace.
Perkin Elmer AmpliTaq a pufr mohou být rovněž použity ve stejných koncentracích.
(10) Metoda byla validována použitím Taq polymerázy Perkin Elmer (AmpliTaq) a Gibco BRL.
(11) Koncentrace primerů NS-5-F a NS-6-R byly optimalizovány pro výkrojky pletiva pupkových částí hlíz bramboru pomocí homogenizační metody a purifikace DNA podle Pastrika (2000) (viz oddíl VI.A.6.1.a)). Použití extrakční metody třepáním nebo jiných metod izolace DNA může vyžadovat nové provedení optimalizace koncentrací reagencií.
(12) Metoda byla validována použitím Taq polymerázy Perkin Elmer (AmpliTaq) a Gibco BRL.
(13) Metoda byla validována použitím Taq polymerázy Perkin Elmer (AmpliTaq) a Gibco BRL.





























