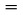(EU) č. 1152/2010Nařízení Komise (EU) č. 1152/2010 ze dne 8. prosince 2010 , kterým se přizpůsobuje technickému pokroku nařízení (ES) č. 440/2008, kterým se stanoví zkušební metody podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 o registraci, hodnocení, povolování a omezování chemických látek (REACH) Text s významem pro EHP
| Publikováno: | Úř. věst. L 324, 9.12.2010, s. 13-38 | Druh předpisu: | Nařízení |
| Přijato: | 8. prosince 2010 | Autor předpisu: | Evropská komise |
| Platnost od: | 12. prosince 2010 | Nabývá účinnosti: | 12. prosince 2010 |
| Platnost předpisu: | Ano | Pozbývá platnosti: | |
Text předpisu s celou hlavičkou je dostupný pouze pro registrované uživatele.
NAŘÍZENÍ KOMISE (EU) č. 1152/2010
ze dne 8. prosince 2010,
kterým se přizpůsobuje technickému pokroku nařízení (ES) č. 440/2008, kterým se stanoví zkušební metody podle nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 o registraci, hodnocení, povolování a omezování chemických látek (REACH)
(Text s významem pro EHP)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady č. 1907/2006 ze dne 18. prosince 2006 o registraci, hodnocení, povolování a omezování chemických látek (REACH), o zřízení Evropské agentury pro chemické látky, o změně směrnice 1999/45/ES a o zrušení nařízení Rady (EHS) č. 793/93, nařízení Komise (ES) č. 1488/94, směrnice Rady 76/769/EHS a směrnic Komise 91/155/EHS, 93/67/EHS, 93/105/ES a 2000/21/ES (1), a zejména na čl. 13 odst. 3 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Nařízení Komise (ES) č. 440/2008 (2) obsahuje zkušební metody pro určení fyzikálně-chemických vlastností, toxicity a ekotoxicity látek používaných pro účely nařízení (ES) č. 1907/2006. |
|
(2) |
Je potřebné aktualizovat nařízení (ES) č. 440/2008, s cílem prioritně zařadit dvě nové zkušební metody in vitro pro podráždění očí přijaté nedávno organizací OECD, aby se dosáhlo snížení počtu zvířat používaných pro pokusné účely v souladu se směrnicí Rady 86/609/EHS ze dne 24. listopadu 1986 o sbližování právních a správních předpisů členských států týkajících se ochrany zvířat používaných pro pokusné a jiné vědecké účely (3). Se zúčastněnými stranami byla tato předloha konzultována. |
|
(3) |
Nařízení (ES) č. 440/2008 by proto mělo být odpovídajícím způsobem změněno. |
|
(4) |
Opatření stanovená tímto nařízením jsou v souladu se stanoviskem výboru zřízeného článkem 133 nařízení (ES) č. 1907/2006, |
PŘIJALA TOTO NAŘÍZENÍ:
Článek 1
V části B přílohy nařízení (ES) č. 440/2008 se doplňují kapitoly B.47 a B.48 podle ustanovení uvedených v příloze tohoto nařízení.
Článek 2
Toto nařízení vstupuje v platnost třetím dnem po vyhlášení v Úředním věstníku Evropské unie.
Toto nařízení je závazné v celém rozsahu a přímo použitelné ve všech členských státech.
V Bruselu dne 8. prosince 2010.
Za Komisi
José Manuel BARROSO
předseda
(1) Úř. věst. L 396, 30.12.2006, s. 1.
(2) Úř. věst. L 142, 31.5.2008, s. 1.
(3) Úř. věst L 358, 18.12.1986, s. 1.
PŘÍLOHA
„B. 47 ZKUŠEBNÍ METODA PRO ZÁKAL A PROPUSTNOST ROHOVKY U SKOTU PRO ZJIŠŤOVÁNÍ LÁTEK S LEPTAVÝMI A SILNĚ DRÁŽDIVÝMI ÚČINKY NA OČI
ÚVOD
|
1. |
Zkušební metoda pro zákal a propustnost rohovky u skotu (BCOP – Bovine Corneal Opacity and Permeability) je zkušební metoda in vitro, kterou lze za určitých okolností a s některými omezeními použít pro klasifikaci látek a směsí jako ‚látky s leptavými a silně dráždivými účinky na oči‘ (1) (2) (3). Pro účely této zkušební metody jsou silné dráždivé látky definovány jako látky způsobující oční léze, které přetrvávají u králíků po dobu nejméně 21 dní po jejich podání. I když se BCOP nepovažuje za úplnou náhradu za oční test in vivo na králících, doporučuje se použít jako součást strategie stupňovitých zkoušek pro regulační klasifikaci a označování v rámci specifické oblasti použitelnosti (4) (5). Zkoušené látky a směsi (6) lze klasifikovat jako látky s leptavými nebo silně dráždivými účinky na oči bez dalšího zkoušení na králících. Látka, jejíž negativní zkoušky by si vyžádaly zkoušení na králících s použitím strategie stupňovitého zkoušení, jak je uvedeno v metodice OECD 405 (7) (kapitola B. 5 této přílohy). |
|
2. |
Účelem této zkušební metody je popsat postupy používané k hodnocení potenciálních leptavých nebo silně dráždivých účinků zkoušené látky na oči měřené její schopností způsobit zákal a zvýšit propustnost v oddělené rohovce skotu. Toxické účinky na rohovku se měří: i) sníženou propustností světla (zákal) a ii) zvýšenou prostupností barviva fluoresceinu sodného (propustnost). Hodnocení zákalu a propustnosti rohovky po expozici zkoušené látce se spojí, aby se odvodil stav podrážděnosti in vitro (IVIS – In Vitro Irritancy Score), který se používá pro klasifikaci úrovně dráždivých účinků zkoušené látky. |
|
3. |
Látky s dráždivými účinky na oči způsobující léze, které odezní nejpozději do 21 dní a nedráždivé látky byly rovněž zkoušeny s použitím zkušební metody BCOP. Přesnost a spolehlivost zkušební metody BCOP u látek těchto kategorií však nebyla oficiálně hodnocena. |
|
4. |
Definice jsou uvedeny v dodatku l. |
POČÁTEČNÍ POSOUZENÍ A OMEZENÍ
|
5. |
Tato zkušební metoda je založena na protokolu zkušební metody BCOP Koordinačního výboru mezi různými organizacemi pro ověřování platnosti alternativních metod (ICCVAM) (8) zpracovaném v návaznosti na mezinárodní studii o ověřování platnosti (4)(5)(9) s přispěním Evropského střediska pro validaci alternativních metod (ECVAM) a Japonského střediska pro validaci alternativních metod (JaCVAM). Protokol vychází z informací získaných z Institutu pro vědní obor in vitro (IIVS) a z protokolu 124 INVITTOX (10), který představuje protokol používaný pro studii o předběžném ověřování platnosti analýzy BCOP sponzorovanou Evropským společenstvím a vypracovanou v letech 1997–1998. Oba tyto protokoly jsou založeny na metodice analýzy BCOP poprvé ohlášené Gautheronem et al. (11). |
|
6. |
Stanovená omezení pro tuto zkušební metodu jsou založena na vysokých mírách falešné pozitivity pro alkoholy a ketony a na vysoké míře falešné negativity pro pevné látky sledované v databázi ověřování platnosti (viz bod 44) (5). Jsou-li látky v rámci těchto chemických a fyzikálních tříd vyřazeny z databáze, přesnost BCOP v klasifikačních systémech EU, EPA a GHS je podstatně vyšší (5). Vycházeje z účelu této analýzy (tj. zjišťovat pouze látky s leptavými/silně dráždivými účinky na oči), míry falešné negativity nejsou kritické, protože tyto látky by se následně zkoušely na králících nebo jinými náležitě validovanými zkouškami in vitro v závislosti na požadavcích právních předpisů s využitím strategie stupňovitého zkoušení v přístupu založeném na vážení důkazů. Kromě toho současná databáze ověřování platnosti neumožňuje odpovídající hodnocení některých tříd chemických látek nebo produktů (např. směsí). Výzkumníci by však mohli zvážit použití této zkušební metody pro všechny druhy zkoušených látek (včetně směsí), přičemž kladné výsledky by mohly být přijaty jako indikátor reakce očí na leptavé nebo silně dráždivé látky. Kladné výsledky získané u alkoholů a ketonů by se však měly interpretovat opatrně z důvodu rizika nepřiměřené předpovědi. |
|
7. |
V případě všech postupů týkajících se očí skotu a rohovek skotu by se měla dodržovat nařízení a postupy použitelné na zkušebny pro zacházení s materiály získanými ze zvířat, které kromě jiného zahrnují tkáně a mimobuněčné tekutiny. Doporučují se univerzální laboratorní preventivní opatření (12). |
|
8. |
Omezení zkušební metody spočívá v tom, že i když tato metoda přihlíží k některým účinkům na oči vyhodnoceným zkušební metodou podráždění očí králíků a do určité míry i k jejich síle, nebere v úvahu poškození spojivky a duhovky. A také ačkoli reverzibilitu lézí rohovky nelze v analýze BCOP hodnotit samu o sobě, na základě studií prováděných na očích králíků bylo navrženo, aby se posouzení počáteční hloubky poškození rohovky použilo k rozlišení mezi nevratnými a vratnými účinky (13). A konečně je třeba uvést, že BCOP neumožňuje posouzení možnosti soustavné toxicity spojené s expozicí očí určitým látkám. |
|
9. |
Vyvíjí se úsilí, aby se dále popsala účelnost a omezení analýzy BCOP pro zjišťování slabých dráždivých látek a nedráždivých látek (viz také bod 45). Uživatelům se rovněž doporučuje, aby organizacím pro ověřování platnosti poskytli vzorky a/nebo údaje pro oficiální hodnocení případného budoucího použití zkušební metody BCOP, včetně zjišťování slabých dráždivých látek a nedráždivých látek. |
|
10. |
Každá laboratoř, která poprvé provádí tuto analýzu, by měla použít vhodné chemické látky uvedené v dodatku 2. Laboratoř může použít tyto chemické látky k prokázání své odborné způsobilosti v provádění zkušební metody BCOP před předložením analytických údajů BCOP pro regulační účely klasifikace nebezpečnosti. |
ZÁSADA ZKOUŠKY
|
11. |
Zkušební metoda BCOP je organotypický model, který zajišťuje krátkodobé udržování běžné fyziologické a biochemické funkce rohovky skotu in vitro. V této zkušební metodě se poškození zkoušenou látkou posuzuje kvantitativním měřením změn v zákalu a propustnosti rohovky za pomoci opacitometru (přístroje na měření průhlednosti) a optického lehkého spektrofotometru. Obě měření se používají k výpočtu stavu podráždění in vitro (IVIS) za účelem přidělení kategorie klasifikace nebezpečnosti podráždění pro předpovídání potenciálu očního podráždění zkoušenou látkou in vivo (viz kritéria rozhodování). |
|
12. |
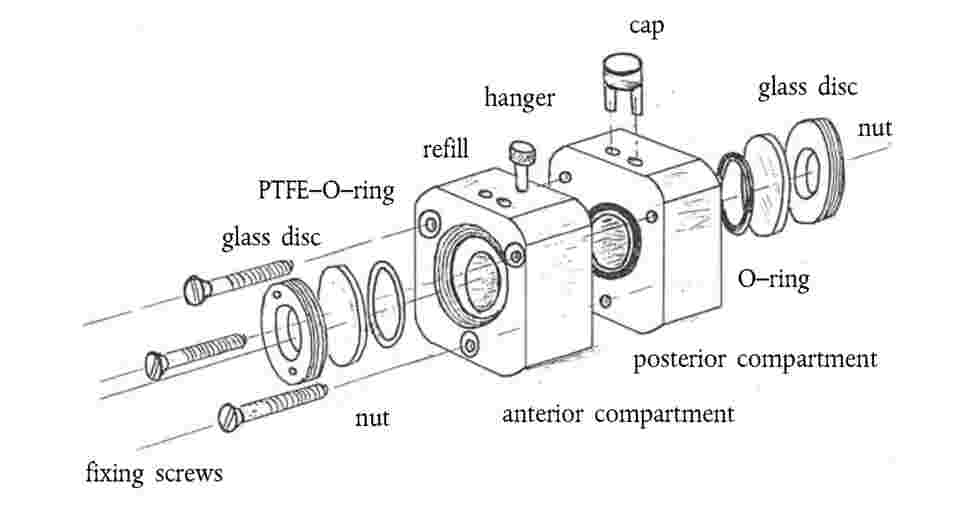
Zkušební metoda BCOP používá oddělené rohovky z očí čerstvě poráženého skotu. Zákal rohovky se měří kvantitativně jako množství průchodu světla rohovkou. Propustnost se měří kvantitativně jako množství barviva fluoresceinu sodného, které prochází celou tloušťkou rohovky a zjišťuje se v mediu zadní komory. Zkoušené látky se aplikují na epiteliální povrch rohovky přidáním do přední komory držáku rohovky. V dodatku 3 je uveden popis a schématický nákres držáku rohovky používaný v BCOP. Držáky rohovky lze komerčně získat z různých zdrojů, nebo je lze zkonstruovat. |
Zdroj a věk očí skotu a výběr druhů zvířat
|
13. |
Skot posílaný na jatka se zpravidla poráží buď pro lidskou spotřebu, nebo pro jiná komerční použití. Jako zdroj rohovek pro použití v BCOP se používají pouze zdravá zvířata, která se považují za vhodná pro vstup do lidského potravinového řetězce. Jelikož skot má široký rozsah hmotnosti v závislosti na chovu, věku a pohlaví, neexistuje žádné doporučení týkající se hmotnosti zvířat v době porážky. |
|
14. |
Mohou se vyskytnout rozdíly ve velikosti rohovky, když se používají oči od zvířat různého věku. Rohovky o vodorovném průměru > 30,5 mm a s hodnotami základní tloušťky rohovky (CCT) ≥ 1 100 μm se obvykle získávají ze skotu staršího osmi let, zatímco rohovky o vodorovném průměru < 28,5 mm a CCT < 900 μm se obvykle získávají ze skotu mladšího pěti let (14). Z těchto důvodů se zpravidla nepoužívají oči ze skotu staršího 60 měsíců. Oči ze skotu mladšího 12 měsíců se tradičně nepoužívají, protože oči se ještě vyvíjejí a tloušťka a průměr rohovky jsou mnohem menší, než jsou zaznamenány u očí dospělého skotu. Používání rohovek z mladých zvířat (tj. 6 až 12 měsíců starých) je však přípustné, jelikož mají určité výhody, např. zvýšená dostupnost, úzký věkový rozsah a nižší nebezpečnost související s potenciální expozicí zaměstnanců bovinní spongiformní encefalopatii (15). Protože by bylo účelné další hodnocení vlivu velikosti nebo tloušťky rohovky na reakci na leptavé a dráždivé látky, uživatelům se doporučuje oznamovat odhadovaný věk a/nebo hmotnost zvířat, které poskytují rohovky používané ve studii. |
Získávání a doprava očí do laboratoře
|
15. |
Oči shromažďují zaměstnanci jatek. Aby se minimalizovaly mechanické a jiné druhy poškození očí, měly by se oči odstranit co nejdříve po úmrtí. Aby se zamezilo expozici očí potenciálně dráždivým látkám, zaměstnanci jatek by neměli při oplachování hlavy zvířete používat čistící prostředky. |
|
16. |
Oči by měly být ve vhodně velké nádobě úplně ponořeny do Hanksova vyváženého solného roztoku (HBSS) a dopraveny do laboratoře tak, aby se minimalizovalo poškození a/nebo bakteriální znečištění. Jelikož oči se získávají během procesu porážení, mohou být vystaveny krvi a jiným biologickým látkám, včetně baktérií a jiných mikroorganismů. Proto je důležité zajistit, aby riziko znečištění bylo minimalizováno (např. držením nádoby, která obsahuje oči, v mokrém ledu, přidáním antibiotik do Hanksova vyváženého solného roztoku (HBSS) použitého k uchování očí během dopravy [např. penicilín se 100 m.j./ml a streptomycin se 100 μg/ml]). |
|
17. |
Časový interval mezi získáním očí a použitím rohovky v BCOP by měl být co nejkratší (získání a použití se uskutečňuje zpravidla tentýž den) a měl by být prokázán, aby se nenarušily výsledky analýzy. Tyto výsledky jsou založeny na kritériích výběru očí a také na reakcích na pozitivní a negativní kontroly. Všechny oči použité v analýze by měly být ze stejné skupiny očí získaných v určitý den. |
Kritéria výběru očí používaných v BCOP
|
18. |
Jakmile se oči dostanou do laboratoře, jsou pečlivě vyšetřeny z hlediska vad, včetně zvýšeného zákalu, škrábanců a neovaskularizace. Smějí se používat pouze rohovky z očí, které tyto vady nemají. |
|
19. |
Kvalita každé rohovky se také hodnotí v pozdějších krocích analýzy. Rohovky, které mají zákal větší než sedm zákalových jednotek, se po počáteční jednohodinové době vyrovnání vyřadí (POZNÁMKA: opacitometr by měl být kalibrován podle norem zákalu používaných k určení zákalových jednotek, viz dodatek 3). |
|
20. |
Každá zkušební skupina (zkoušená látka, paralelní negativní a pozitivní kontroly) pozůstává nejméně ze třech očí. V případě rohovek pro negativní kontrolu by se v analýze BCOP měly používat tři rohovky. Protože všechny rohovky jsou vyříznuty z celé oční boule a vloženy do komor rohovky, existuje možnost výtvorů ze zpracování jednotlivých hodnot zákalu a propustnosti rohovky (včetně negativní kontroly). Kromě toho se hodnoty zákalu a propustnosti rohovek z negativních kontrol používají k úpravě zkoušených předmětů a hodnoty zákalu a propustnosti rohovek z pozitivních kontrol se používají ve výpočtech IVIS. |
POSTUP
Příprava očí
|
21. |
Rohovky, které nemají vady, se vyřezávají s 2 až 3 mm okrajem očního bělma, který zůstává a pomáhá v následném ošetření, přičemž se musí dávat pozor, aby se zamezilo poškození epitelu a endotelu rohovky. Oddělené rohovky se zasazují do zvlášť k tomu určených držáků rohovek složených z předních a zadních částí, které se dotýkají příslušně epiteliálních a endoteliálních stran rohovky. Obě komory se úplně zaplní předehřátým Eaglovým minimálně nutným médiem (EMEM) (nejdříve zadní komora) a tím se zajistí, že se nevytvoří žádné bubliny. Zařízení se potom vyrovnává na teplotu 32 ± 1 °C nejméně po dobu jedné hodiny, aby se rohovky mohly srovnat s médiem a dosáhnout v co největším rozsahu běžné metabolické aktivity (přibližná teplota povrchu rohovky in vivo je 32 °C). |
|
22. |
Po době vyrovnání se čerstvé předehřáté médium EMEM přidá do obou komor a pro každou rohovku se odeberou základní údaje o zákalu. Všechny rohovky, které vykazují makroskopické poškození tkání (např. poškrábání, pigmentace, neovaskularizace) nebo zákal > 7 jednotek zákalu, se vyřadí. Vypočte se střední zákal vyrovnaných rohovek. Minimálně tři rohovky s hodnotami zákalu, které se blíží střední hodnotě všech rohovek, se vyberou jako rohovky pro negativní kontrolu (nebo pro kontrolu s rozpouštědlem). Zbylé rohovky se potom rozdělí do zkušebních skupin a do skupin pro pozitivní kontrolu. |
|
23. |
Jelikož tepelná kapacita vody je ve srovnání se vzduchem vyšší, voda poskytuje stabilnější teplotní podmínky pro inkubaci. Proto se doporučuje používání vodní lázně pro udržování držáku rohovky a jeho obsahu při teplotě 32 ± 1 °C. Vzduchové inkubátory však lze také použít za předpokladu, že budou přijata preventivní opatření k zachování tepelné stability (např. předehřátím držáků a medií). |
Aplikace zkoušené látky
|
24. |
Používají se dva různé zkušební protokoly, jeden pro tekutiny a smáčedla (pevné nebo tekuté) a jeden pro pevné látky, které nejsou smáčedla. |
|
25. |
Tekutiny se zkoušejí neředěné, zatímco smáčedla se zkoušejí při koncentraci 10 % objemové hmotnosti (w/v) v 0,9 % roztoku chloridu sodného, destilované vody nebo jiného rozpouštědla, u něhož se prokázalo, že nemá nepříznivé účinky na zkušební systém. Jako tekutiny se zpravidla zkoušejí polotuhé, krémové a voskovité látky. U alternativních koncentrací roztoku by mělo být předloženo příslušné zdůvodnění. Rohovky jsou vystaveny tekutinám a smáčedlům po dobu 10 minut. Použití jiných dob expozice by mělo být doprovázeno odpovídajícím vědeckým zdůvodněním. |
|
26. |
Pevné látky, které nejsou smáčedla, se zpravidla zkoušejí jako roztoky nebo suspenze při 20 % koncentraci v 0,9 % roztoku chloridu sodného, destilované vody nebo jiného rozpouštědla, u něhož se prokázalo, že nemá nepříznivé účinky na zkušební systém. Za určitých okolností a s náležitým vědeckým zdůvodněním se pevné látky mohou zkoušet také čisté s přímou aplikací na povrch rohovky a s použitím metody otevřených komor (viz bod 29). Rohovky jsou vystaveny pevným látkám po dobu čtyř hodin, ale podobně jako u tekutých látek a smáčedel lze s odpovídajícím vědeckým zdůvodněním použít alternativní doby expozice. |
|
27. |
Je možné použít různé metody zkoušení v závislosti na fyzické povaze a chemických vlastnostech zkoušené látky (např. pevné látky, tekutiny, viskózní látky versus neviskózní tekutiny). Kritický faktor zajišťuje, že zkoušená látka náležitě pokrývá epiteliální povrch a že je příslušně odstraněna během oplachování. Metoda uzavřených komor se obvykle používá pro neviskózní až mírně viskózní tekuté zkoušené látky, zatímco metoda otevřených komor se zpravidla používá pro poloviskózní a viskózní tekuté zkoušené látky a pro čisté pevné látky. |
|
28. |
V metodě uzavřených komor se dostatečné množství zkoušené látky (750 μL) k pokrytí epiteliální strany rohovky zavádí do přední komory přes dávkovací otvory na horním povrchu komory a otvory jsou potom během expozice uzavřeny komorovými zátkami. Je důležité zajistit, aby každá rohovka byla vystavena zkoušené látce po příslušnou dobu. |
|
29. |
V metodě otevřených komor se před zkoušením odstraní z přední komory zavírací klička okénka a skleněné okénko. Kontrolní nebo zkoušená látka (750 μL nebo dostatečné množství zkoušené látky, aby úplně pokryla rohovku) se aplikuje přímo na epiteliální povrch rohovky s použitím mikropipety. Pokud je zkoušenou látku obtížné pipetovat, lze ji zavést pod tlakem do objemové pipety, což pomůže v dávkování. Špička objemové pipety se zasune do dávkovací špičky injekční stříkačky tak, aby látku bylo možné zavést pod tlakem do špičky vytěsňování. Píst injekční stříkačky se stlačí současně s tím, jak se píst pipety vytahuje nahoru. Pokud se ve špičce pipety objeví vzduchové bubliny, zkoušený předmět se odstraní (vytlačí) a postup se opakuje, dokud špička není naplněná bez vzduchových bublin. V případě potřeby lze použít běžnou injekční stříkačku (bez jehly), protože umožňuje měření přesného objemu zkoušené látky a snadnější aplikaci na epiteliální povrch rohovky. Po dávkování se skleněné okénko umístí znovu na přední komoru, aby se obnovil uzavřený systém. |
Inkubace po expozici
|
30. |
Po době expozice se zkoušená látka, látka pro negativní kontrolu nebo látka pro pozitivní kontrolu odstraní z přední komory a epitel se nejméně třikrát opláchne (nebo se oplachuje tak dlouho, dokud nepřestanou být viditelné stopy zkoušené látky) médiem EMEM (obsahující fenolovou červeň). Na oplachování se používá médium obsahující fenolovou červeň, protože změnu barvy ve fenolové červeni lze sledovat, aby se zjistila účinnost oplachovacích kyselých nebo alkalických látek. Rohovky se proplachují více než třikrát, pokud je fenolová červeň ještě zbarvená (do žluta nebo do nachova), nebo pokud je zkoušená látka stále viditelná. Jakmile již v médiu není zkoušená látka, rohovky se naposledy opláchnou médiem EMEM (bez fenolové červeně). EMEM (bez fenolové červeně) se používá jako konečný oplach, aby se před měřením zákalu zajistilo odstranění fenolové červeně z přední komory. Přední komora se pak naplní čerstvým EMEM bez fenolové červeně. |
|
31. |
U tekutin nebo smáčedel se rohovky po oplachu inkubují po dobu dalších dvou hodin při teplotě 32 ± 1 °C. Delší doba po expozici by byla za určitých okolností účelná a mohla by se zvážit případ od případu. Rohovky zkoušené s pevnými látkami se důkladně propláchnou na konci doby čtyřhodinové expozice, ale nevyžadují si další inkubaci. |
|
32. |
Zákal a propustnost každé rohovky se v případě tekutých látek a smáčedel zaznamená na konci doby inkubace po expozici a v případě pevných látek, které nejsou smáčedla, na konci doby čtyřhodinové expozice. Každá rohovka se sleduje rovněž vizuálně a případná pozorování se zaznamenají (např. odlupování tkáně, zbytky zkoušené látky, nejednotné struktury rohovky). Tato pozorování by mohla být důležitá, protože mohou odrážet změny v údajích opacitometru. |
Látky pro kontrolu
|
33. |
Do každého pokusu se zařazují souběžné negativní kontroly nebo kontroly s rozpouštědlem/vehikulem a pozitivní kontroly. |
|
34. |
Když se zkouší tekutá látka při 100 % koncentraci, souběžná negativní kontrola (např. 0,9 % roztok chloridu sodného nebo destilovaná voda) se zahrne do zkušební metody BCOP tak, aby bylo možné zjistit nespecifické změny ve zkušebním systému a zajistit základnu pro koncové body analýzy. Tím se rovněž zajistí, že podmínky analýzy nebudou mít za následek nevhodnou dráždivou reakci. |
|
35. |
Když se zkouší rozředěná tekutina, smáčedlo nebo pevná látka, skupina pro souběžnou kontrolu s rozpouštědlem/vehikulem se zahrne do zkušební metody BCOP tak, aby bylo možné zjistit nespecifické změny ve zkušebním systému a zajistit základnu pro koncové body analýzy. Lze použít pouze rozpouštědlo/vehikul, u kterého se prokázalo, že nemá nepříznivé účinky na zkušební systém. |
|
36. |
Do každého pokusu se zařadí známá látka s dráždivými účinky na oči jako látka pro souběžnou pozitivní kontrolu, aby se ověřilo, že je vyvolána odpovídající reakce. Protože analýza BCOP se v této zkušební metodě používá ke zjišťování leptavých nebo silných dráždivých látek, ideálně by pro pozitivní kontrolu měla být referenční látka, která v této zkušební metodě vyvolá silnou reakci. Aby se však zajistilo, že proměnlivost v reakci na pozitivní kontrolu bude možné časem vyhodnotit, rozsah dráždivé reakce by neměl být nadměrný. |
|
37. |
Příklady tekutých zkoušených látek pro pozitivní kontrolu jsou dimetylformamid nebo 1 % hydroxid sodný. Příkladem pevných zkoušených látek pro pozitivní kontrolu je 20 % (objemové hmotnosti) imidazol v 0,9 % roztoku chloridu sodného. |
|
38. |
Srovnávací látky jsou účelné pro hodnocení potenciálu podráždění očí neznámými chemickými látkami nebo specifickými třídami chemických látek či produktů nebo pro hodnocení potenciálu relativního podráždění látkou s dráždivými účinky na oči ve specifickém rozmezí dráždivých reakcí. |
Měřené koncové body
|
39. |
Zákal se určuje množstvím světelné propustnosti rohovkou. Zákal rohovky se kvantitativně měří za pomoci opacitometru a výsledkem jsou hodnoty zákalu měřené na celém rozsahu stupnice. |
|
40. |
Propustnost se určuje množstvím barviva fluoresceinu sodného, které proniká všemi vrstvami buněk rohovky (tj. epitelem na vnějším povrchu rohovky přes endotel na vnitřním povrchu rohovky). 1 ml roztoku fluoresceinu sodného (4 nebo 5 mg/ml, když se příslušně zkoušejí tekuté látky a smáčedla nebo pevné látky, které nejsou smáčedla) se přidává do přední komory držáku rohovky, která je spojena s epiteliální stranou rohovky, zatímco zadní komora, která je spojena s endoteliální stranou rohovky, se naplní čerstvým médiem EMEM. Držák se potom ve vodorovné poloze inkubuje po dobu 90 ± 5 min. na teplotu 32 ± 1 °C. Množství fluoresceinu sodného, který přechází do zadní komory, se kvantitativně měří za pomoci spektrofotometrie UV/VIS. Spektrofotometrická měření hodnocená ve 490 nm se zaznamenají jako optická hustota (OD490) nebo hodnoty absorbance, které se měří na celém rozsahu stupnice. Hodnoty propustnosti fluoresceinu se stanoví s použitím hodnot OD490 na základě spektrofotometru viditelného světla s použitím běžné optické délky 1 cm. |
|
41. |
Alternativně se může použít analyzátor destiček s 96 jamkami, pokud i) lze stanovit lineární dosah analyzátoru destiček pro určení hodnot fluoresceinu OD490; a ii) v 96jamkové destičce je použito správné množství vzorků fluoresceinu, jehož výsledkem jsou hodnoty OD490 odpovídající běžné optické délce 1 cm (to by si mohlo vyžadovat úplně plnou jamku [obvykle 360μL]). |
ÚDAJE A PODÁVÁNÍ ZPRÁV
Hodnocení údajů
|
42. |
Jakmile se hodnoty zákalu a střední hodnoty propustnosti (OD490) upraví na zákal pozadí a hodnoty propustnosti OD490 pro negativní kontrolu, střední hodnoty zákalu a propustnosti OD490 pro každou zkušební skupinu by se měly spojit do empiricky odvozeného vzorce, aby se vypočítal stav podráždění in vitro (IVIS) pro každou zkušební skupinu takto: IVIS = střední hodnota zákalu + (15 × střední hodnota propustnosti OD490) Sina et al. (16) oznámil, že tento vzorec byl odvozen během laboratorních a mezilaboratorních studií. Údaje vytvořené pro řady 36 sloučenin v multilaboratorní studii byly předmětem vícerozměrné analýzy s cílem určit nejvhodnější rovnováhu mezi údaji in vivo a in vitro. Tuto analýzu uskutečnili ve dvou samostatných společnostech vědci, kteří odvodili téměř stejné vzorce. |
|
43. |
Hodnoty zákalu a propustnosti by se měly rovněž posuzovat samostatně, aby se určilo, zda zkoušená látka způsobuje poleptání nebo silné podráždění pomocí pouze jednoho nebo dvou koncových bodů (viz kritéria rozhodování). |
Kritéria rozhodování
|
44. |
Látka, která způsobuje IVIS ≥ 55,1, se definuje jako leptavá nebo silně dráždivá. Jak je uvedeno v bodě 1, pokud zkoušená látka není určena jako látka s leptavými nebo silně dráždivými účinky na oči, mělo by se uskutečnit další zkoušení pro účely klasifikace a označování. Zkušební metoda BCOP má celkovou přesnost 79 % (113/143) až 81 % (119/147), míru falešné pozitivity 19 % (20/103) až 21 % (22/103) a míru falešné negativity 16 % (7/43) až 25 % (10/40) ve srovnání s údaji ze zkušební metody in vivo na očích králíků klasifikovanými podle klasifikačních systémů EPA (1), EU (2) nebo GHS (3). V případě, že látky v určitých chemických třídách (tj. alkoholy, ketony) nebo fyzikálních třídách (tj. pevné látky) jsou vyloučeny z databáze, přesnost BCOP se v klasifikačních systémech EU, EPA a GHS pohybuje v rozmezí od 87 % (72/83) do 92 % (78/85), míra falešné pozitivity od 12 % (7/58) do 16 % (9/56) a míra falešné negativity od 0 % (0/27) do 12 % (3/26). |
|
45. |
I když se klasifikace látek s leptavými nebo silně dráždivými účinky na oči pro zkoušenou látku nezíská, údaje BCOP mohou být užitečné ve spojení s testovacími údaji z oční zkoušky in vivo na králících nebo z náležitě validované zkoušky in vitro, aby se dále vyhodnotila účelnost a omezení zkušební metody BCOP pro určení slabých dráždivých a nedráždivých látek (dokument s pokyny o používání zkušebních metod oční toxicity in vitro se zpracovává). |
Kritéria přijetí studie
|
46. |
Zkouška se považuje za přijatelnou, pokud pozitivní kontrola vykazuje IVIS spadající do obvyklých odchylek dosavadní střední hodnoty, kterou je třeba aktualizovat nejméně každé tři měsíce nebo pokaždé, když se přijatelná zkouška vykonává v laboratořích, kde se zkoušky nedělají často (tj. méně než jednou měsíčně). Výsledkem reakce na negativní kontrolu nebo na kontrolu s rozpouštědlem/vehikulem by měly být hodnoty zákalu a propustnosti, které jsou nižší než stanovené horní meze pro hodnoty zákalu pozadí a prostupnosti u rohovek skotu zkoušené příslušnou negativní kontrolou nebo kontrolou s rozpouštědlem/vehikulem. |
Zpráva o zkoušce
|
47. |
Zpráva o zkoušce by měla zahrnovat tyto informace, pokud se týkají uskutečňování studie: Zkoušené látky a látky pro kontrolu
Informace týkající se zadavatele a zkušebního zařízení
Zdůvodnění použité zkušební metody a protokolu Úplnost zkušební metody Postup používaný k zajištění úplnosti (tj. přesnosti a spolehlivosti) zkušební metody v průběhu času (např. pravidelné zkoušení vhodných látek, využívání dosavadních údajů negativních a pozitivních kontrol). Kritéria pro přijatelnou zkoušku
Zkušební podmínky
Výsledky
Posouzení výsledků Závěr |
LITERATURA
|
1) |
U.S. EPA (1996). Label Review Manual: 2. vydání. EPA737-B-96-001. Washington, DC: U.S. Environmental Protection Agency. |
|
2) |
Nařízení Evropského parlamentu a Rady (ES) č. ze dne 16. prosince 2008 o klasifikaci, označování a balení látek a směsí, o změně a zrušení směrnice 67/548/EHS a 1999/45/ES a o změně nařízení (ES) č. 1907/2006. Úř. věst. L 353, 31.12.2008, s. 1. |
|
3) |
OSN (2007). Globálně harmonizovaný systém klasifikace a označování chemických látek (GHC). Druhé revidované vydání, New York a Ženeva: publikace Organizace spojených národů, 2007. Dostupné na: [http://www.unece.org/trans/danger/publi/ghs/ghs_rev02/02files_e.html]. |
|
4) |
ESAC (2007). Prohlášení o uzavření retrospektivní studie ICCVAM o orgánových analýzách in vitro jako screeningové testy pro zjišťování potenciálních látek s leptavými a silně dráždivými účinky na oči. Dostupné na: [http://ecvam.jrc.it/index.htm]. |
|
5) |
ICCVAM (2007). Zpráva o hodnocení zkušebních metod – zkušební metody oční toxicity in vitro pro zjišťování látek se silně dráždivými a leptavými účinky na oči. Koordinační výbor mezi různými organizacemi pro ověřování platnosti alternativních metod (ICCVAM) a Středisko mezi různými organizacemi pro hodnocení alternativních toxikologických metod (NICEATM) národního toxikologického programu (NTP). Publikace NIH č.: 07-4517. Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_tmer.htm]. |
|
6) |
Nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006 o registraci, hodnocení, povolování a omezování chemických látek, o zřízení Evropské agentury pro chemické látky, o změně směrnice 1999/45/ES a o zrušení nařízení Rady (EHS) č. 793/93, nařízení Komise (ES) č. 1488/94, směrnice Rady 76/769/EHS a směrnic Komise 91/155/EHS, 93/67/EHS, 93/105/ES a 2000/21/ES. Úř. věst. L 396, 30.12.2006, s. 1. |
|
7) |
OECD (2002). Metodika 405. Pokyn OECD pro zkoušení chemických látek. Akutní podráždění/poleptání očí. Dostupné na: [http://www.oecd.org/document/40/0,2340,en_2649_34377_37051368_1_1_1_1,00.html]. |
|
8) |
ICCVAM (2007). Doporučený protokol zkušební metody BCOP ICCVAM. Ve: Zprávě o hodnocení zkušebních metod ICCVAM – zkušební metody oční toxicity in vitro pro zjišťování látek se silně dráždivými a leptavými účinky na oči. Koordinační výbor mezi různými organizacemi pro ověřování platnosti alternativních metod (ICCVAM) a Středisko mezi různými organizacemi pro hodnocení alternativních toxikologických metod (NICEATM) národního toxikologického programu (NTP). Publikace NIH č.: 07-4517. Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_tmer.htm]. |
|
9) |
ICCVAM. (2006). Současný stav zkušebních metod in vitro pro zjišťování látek s leptavými a silně dráždivými účinky na oči: zkušební metoda pro zákal a propustnost rohovky u skotu. Publikace NIH č.: 06-4512. Research Triangle Park: národní toxikologický program. Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_ice.htm]. |
|
10) |
INVITTOX (1999). Protokol 124: analýza zákalu a propustnosti rohovky skotu – SOP of Microbiological Associates Ltd. Ispra, Itálie: Evropské středisko pro ověřování platnosti alternativních metod (ECVAM). |
|
11) |
Gautheron, P., Dukic, M., Alix, D. and Sina, J.F. (1992). Bovine corneal opacity and permeability test: An in vitro assay of ocular irritancy. Fundam. Appl. Toxicol. 18:442-449. |
|
12) |
Siegel, J.D., Rhinehart, E., Jackson, M., Chiarello, L., and the Healthcare Infection Control Practices Advisory Committee (2007). Guideline for Isolation Precautions: Preventing Transmission of Infectious Agents in Health-care Settings. Dostupné na: [http://www.cdc.gov/ncidod/dhqp/pdf]. |
|
13) |
Maurer, J.K., Parker, R.D. and Jester, J.V. (2002). Extent of corneal injury as the mechanistic basis for ocular irritation: key findings and recommendations for the development of alternative assays. Reg. Tox. Pharmacol. 36:106-117. |
|
14) |
Doughty, M.J., Petrou, S. and Macmillan, H. (1995). Anatomy and morphology of the cornea of bovine eyes from a slaughterhouse. Can. J. Zool. 73:2159-2165. |
|
15) |
Collee, J. and Bradley, R. (1997). BSE: A decade on - Part I. The Lancet 349: 636-641. |
|
16) |
Sina, J.F., Galer, D.M., Sussman, R.S., Gautheron, P.D., Sargent, E.V., Leong, B., Shah, P.V., Curren, R.D., and Miller, K. (1995). A collaborative evaluation of seven alternatives to the Draize eye irritation test using pharmaceutical intermediates. Fundam Appl Toxicol 26:20-31. |
|
17) |
ICCVAM (2006). Základní dokument o přezkumu, současný stav zkušebních metod in vitro pro zjišťování látek s leptavými a silně dráždivými účinky na oči: zkušební metoda pro zákal a propustnost rohovky u skotu (BCOP). Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_bcop.htm]. |
|
18) |
ICCVAM (2006). Základní dokument o přezkumu, současný stav zkušebních metod In Vitro pro zjišťování látek s leptavými a silně dráždivými účinky na oči: zkušební metoda odděleného kuřecího oka (ICE). Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_bcop.htm]. |
Dodatek 1
DEFINICE
Přesnost: Přesnost shody mezi výsledky zkušební metody a přijatými referenčními hodnotami. Je to měření výsledku zkušební metody a jednoho aspektu „důležitosti“. Termín se často používá namísto „souladu“, kterým se rozumí podíl správných výsledků zkušební metody.
Srovnávací látka: Látka použitá jako norma pro srovnání se zkoušenou látkou. Srovnávací látka by měla mít tyto vlastnosti: i) nesporný a spolehlivý zdroj (nesporné a spolehlivé zdroje); ii) strukturální a funkční podobnost s třídou zkoušených látek; iii) známé fyzikální/chemické vlastnosti; iv) podpůrné údaje o známých účincích a v) známá síla v rozsahu žádoucí reakce.
Rohovka: Průhledná přední část oční bulvy, která zahrnuje duhovku a očnici a propouští světlo dovnitř oka.
Zákal rohovky: Měření rozsahu zákalu rohovky po expozici zkoušené látce. Zvýšený zákal rohovky je příznačný pro poškození rohovky. Zákal lze hodnotit subjektivně, jak se to dělá ve Draizeově oční zkoušce na králících, nebo objektivně s přístrojem jako „opacitometr“.
Propustnost rohovky: Kvantitativní měření poškození epitelu rohovky určením množství barviva fluoresceinu sodného, který prochází všemi vrstvami buněk rohovky.
Kategorie 1 EPA: Zasažení leptavou látkou (nevratné poškození oční tkáně) nebo zasažení rohovky či podráždění přetrvávající déle než 21 dní (1).
Kategorie R41 EU: Tvorba poškození tkání v oku nebo závažné fyzické slábnutí vidění po aplikaci zkoušené látky na přední plochu oka, které není plně vratné do 21 dní od aplikace (2).
Míra falešné negativity: Podíl všech pozitivních látek falešně zjištěných zkušební metodou jako negativní. Je to jeden z ukazatelů výsledku zkušební metody.
Míra falešné pozitivity: Podíl všech negativních látek falešně zjištěných zkušební metodou jako pozitivní. Je to jeden z ukazatelů výsledku zkušební metody.
GHS (Globálně harmonizovaný systém klasifikace a označování chemických látek): Systém klasifikace chemických látek (látek a směsí) podle standardizovaných typů a úrovní fyzikálních, zdravotních a environmentálních rizik a odpovídajícího označování pomocí prvků informací o nebezpečnosti, jako jsou výstražné symboly nebezpečnosti, signální slova, standardní věty o nebezpečnosti, pokyny pro bezpečné zacházení a bezpečnostní listy, aby poskytly informace o nepříznivých účincích s ohledem na ochranu lidí (včetně zaměstnavatelů, zaměstnanců, dopravců, spotřebitelů a respondérů nebezpečí) a životního prostředí (3).
Kategorie 1 GHS: Tvorba poškození tkání v oku nebo závažné fyzikální slábnutí vidění po aplikaci zkoušené látky na přední plochu oka, které není plně vratné do 21 dní od aplikace (3).
Nebezpečnost: Základní charakteristika chemické látky nebo situace, která má potenciál vyvolat nepříznivé účinky, jsou-li organismus, systém nebo (sub)populace vystaveny této látce.
Stav podráždění in vitro (IVIS): Empiricky odvozený vzorec používaný v analýze BCOP, přičemž střední hodnoty zákalu a propustnosti se pro každou zkušební skupinu spojí do jedné hodnoty in vitro pro každou zkušební skupinu. IVIS = střední hodnota zákalu + (15 x střední hodnota propustnosti).
Negativní kontrola: Nezkoušená replika, která obsahuje všechny složky zkušebního systému. Tento vzorek se zpracovává se vzorky zkoušené látky a jinými kontrolními vzorky, aby se zjistilo, zda rozpouštědlo vzájemně reaguje se zkušebním systémem.
Nedráždivá látka: Látky, které nejsou klasifikovány jako látky s dráždivými účinky na oči kategorie I, II, nebo III EPA; kategorie R41 nebo R36 EU; nebo kategorie 1, 2A, nebo 2B GHS.
Látka s leptavými účinky na oči: a) Látka, která způsobuje nevratné poškození tkání oka; b) látky které jsou klasifikovány jako látky s dráždivými účinky na oči kategorie 1 GHS, kategorie I EPA nebo kategorie R41 EU (1) (2) (3).
Látka s dráždivými účinky na oči: a) Látka, která způsobuje nevratnou změnu v oku po aplikaci na přední plochu oka; b) látky, které jsou klasifikovány jako látky s dráždivými účinky na oči kategorie II nebo III EPA, kategorie R36 EU nebo kategorie 2A nebo 2B GHS (1) (2) (3).
Látka se silně dráždivými účinky na oči: a) Látka způsobující poškození v oku po aplikaci na přední plochu oka, které neodezní do 21 dní po aplikaci, nebo způsobující závažné fyzikální slábnutí vidění; b) látky, které jsou klasifikovány jako látky s dráždivými účinky na oči kategorie 1 GHS, kategorie I EPA nebo kategorie R41 EU, (1) (2) (3).
Opacitometr: Přístroj používaný k měření „zákalu rohovky“ kvantitativním hodnocením světelné propustnosti přes rohovku. Typický přístroj má dvě části, každá s vlastním zdrojem světla a fotobuňkou. Jedna část se používá pro zkoušenou rohovku a druhá pro kalibraci a vynulování přístroje. Světlo z halogenové lampy se posílá přes kontrolní část (prázdná komora bez okének nebo tekutin) do fotobuňky a vyrovnané se světlem se posílá do fotobuňky přes zkušební část, ve které je umístěna komora obsahující rohovku. Rozdíl ve světelné propustnosti z fotobuněk se porovnává a numerická hodnota zákalu se zobrazí na digitální obrazovce.
Pozitivní kontrola: Replika obsahující všechny složky zkušebního systému a zkoušená s látkou, o níž je známo, že vyvolává pozitivní reakci. Aby se zajistilo, že proměnlivost v reakci na pozitivní kontrolu bude možné časem vyhodnotit, rozsah silné reakce by neměl být nadměrný.
Spolehlivost: Měření rozsahu, v jakém může být zkušební metoda časem reprodukovatelná v laboratořích a mezi laboratořemi, když se provádí s použitím stejného protokolu. Hodnotí se to výpočtem laboratorní a mezilaboratorní reprodukovatelnosti a laboratorní opakovatelnosti.
Kontrola s rozpouštědlem/vehikulem: Neošetřený vzorek obsahující všechny složky zkušebního systému, včetně rozpouštědla nebo vehikulu, který se zpracovává ošetřenou zkoušenou látkou a jinými kontrolními vzorky, aby se zjistila základní reakce vzorků ošetřených zkoušenou látkou rozpuštěnou ve stejném rozpouštědle nebo vehikulu. Pokud se vzorek zkouší souběžnou negativní kontrolou, ukazuje také, zda rozpouštědlo nebo vehikul vzájemně reaguje se zkušebním systémem.
Stupňovité zkoušení: Strategie postupného zkoušení, kde se všechny existující informace o zkoušené látce přezkoumávají ve stanoveném pořadí s použitím postupu váhy důkazů na každém stupni, aby se zjistilo, zda jsou k dispozici dostačující informace pro rozhodnutí o klasifikaci nebezpečnosti, než se postoupí do dalšího stupně. Pokud lze potenciál dráždivých účinků zkoušené látky určit na základě existujících informací, další zkoušení není nutné. Jestliže potenciál dráždivých účinků zkoušené látky nelze určit na základě existujících informací, použije se stupňovitý postupný postup zkoušení na zvířatech, dokud se neurčí jednoznačná klasifikace.
Validovaná zkušební metoda: zkušební metoda, pro kterou byly zpracovány validační studie s cílem určit důležitost (včetně přesnosti) a spolehlivost pro specifický účel. Je nutné poznamenat, že validovaná zkušební metoda nemusí poskytnout postačující výsledek z hlediska přesnosti a spolehlivosti, aby byla shledána přijatelnou pro navržený účel.
Váha důkazů: Postup zvažování silných a slabých stránek různých informací v dosahování a podpoře závěru týkajícího se potenciálu nebezpečnosti látky.
Dodatek 2
Vhodné látky pro zkušební metodu BCOP
Než laboratoře rutinně použijí zkušební metodu, která dodržuje tuto zkušební metodu, měly by prokázat svou odbornou způsobilost správným určením klasifikace 10 látek s dráždivými účinky na oči doporučených v tabulce 1. Tyto látky byly vybrány tak, aby představovaly rozsah reakcí v případě místního podráždění/poleptání očí, které vycházejí z výsledků očních zkoušek in vivo na králících (TG 405) (tj. kategorie 1, 2A, 2B nebo neklasifikované a označené podle GHS OSN) (3) (7). S přihlédnutím k validované účelnosti těchto analýz (tj. zjišťování pouze látek s leptavými/silně dráždivými účinky na oči) však existují pouze dva výsledky zkoušky pro klasifikační účely (leptavá/silně dráždivá látka nebo neleptavá/slabá dráždivá látka), aby byla prokázána odborná způsobilost. Dalším kritériem výběru bylo to, zda látka je komerčně dostupná, zda jsou k dispozici kvalitní referenční údaje in vivo a zda jsou kvalitní údaje ze dvou metod in vitro, pro které byly zpracovány metodiky. Z tohoto důvodu byly dráždivé látky vybrány z doporučeného seznamu 122 referenčních látek ICCVAM pro ověření platnosti zkušebních metod oční toxicity in vitro (viz dodatek H: Doporučené referenční látky ICCVAM) (5). Referenční údaje jsou dostupné v základním dokumentu o přezkumu ICCVAM pro zkušební metodu BCOP a odděleného kuřecího oka (ICE) (17) (18).
Tabulka 1
Doporučené látky k prokázání odborné způsobilosti pro BCOP
|
Látka |
CASRN |
Třída chemických látek (1) |
Fyzikální forma |
Klasifikace in vivo (2) |
Klasifikace in vitro (3) |
|
Benzalkoniumchlorid (5%) |
8001-54-5 |
Oniová sloučenina |
Tekutá |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Chlorhexidin |
55-56-1 |
Amin, amidin |
Pevná |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Dibenzoyl-L–tartarová kyselina |
2743-38-6 |
Karboxylová kyselina, ester |
Pevná |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Imidazol |
288-32-4 |
Heterocyklická |
Pevná |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Kyselina trichloroctová (30%) |
76-03-9 |
Karboxylová kyselina |
Tekutá |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Dichlorbenzoyl chlorid |
4659-45-4 |
Acylhalogenid |
Tekutá |
Kategorie 2A |
Neleptavá/slabá dráždivá látka |
|
Etyl-2-metylaceto–acetát |
609-14-3 |
Keton, ester |
Tekutá |
Kategorie 2B |
Neleptavá/slabá dráždivá látka |
|
Dusičnan amonný |
6484-52-2 |
Anorganická sůl |
Pevná |
Kategorie 2A |
Neleptavá/slabá dráždivá látka |
|
Glycerol |
56-81-5 |
Alkohol |
Tekutá |
Neoznačená |
Neleptavá/Slabá dráždivá látka |
|
n-hexan |
110-54-3 |
Uhlovodík (acyklický) |
Tekutá |
Neoznačená |
Neleptavá/slabá dráždivá látka |
|
Zkratky: CASRN = registrační číslo podle služby chemických abstrakt |
|||||
Dodatek 3
DRŽÁK ROKOVEK BCOP
|
1. |
Držáky rohovek BCOP se vyrábějí z inertního materiálu (např. polypropylenu). Držáky se skládají ze dvou polovin (přední a zadní komora) a mají dvě podobné cylindrické vnitřní komory. Každá komora pojme obsah 5 ml a končí ve skleněném okénku, přes které se zaznamenávají měření zákalu. Každá vnitřní komora má průměr 1,7 cm a hloubku 2,2 cm (4). Použije se těsnící kroužek umístěný na zadní komoře, aby se zamezilo úniku látky. Rohovky jsou umístěny na endoteliální straně pod těsnícím kroužkem zadních komor a přední komory se nacházejí na epiteliální straně rohovek. Komory se udržují na místě za pomoci třech nerezavých šroubů umístěných na vnějších okrajích komory. Na konci každé komory se nachází skleněné okénko, které lze odstranit, aby byl snadný přístup k rohovce. Jeden těsnící kroužek je také umístěn mezi skleněným okénkem a komorou, aby se zamezilo úniku látky. Dva otvory v horní části každé komory umožňují zavedení a odstranění média a zkoušených směsí. Po dobu zkoušení a inkubace jsou uzavřeny gumovými uzávěry.
|
OPACITOMETR
|
2. |
Opacitometr je přístroj pro měření světelné propustnosti. Světlo z halogenové lampy se posílá přes kontrolní část (prázdná komora bez okének nebo tekutiny) do fotobuňky a vyrovnané se světlem se posílá do fotobuňky přes zkušební část, ve které se nachází komora obsahující rohovku. Rozdíl ve světelné propustnosti z fotobuněk se porovnává a numerická hodnota zákalu se zobrazí na digitální obrazovce. Tím se určí zákalové jednotky. |
|
3. |
Opacitometr by měl poskytnout lineární odezvu za pomoci řady údajů o zákalu, které zahrnují mezní hodnoty používané pro různé klasifikace popsané v modelu předpovědí (tj. až do mezní hodnoty, která určuje leptavost/silnou dráždivost). Aby se zajistily lineární a přesné údaje až do 75 – 80 zákalových jednotek, je nutné opacitometr kalibrovat s použitím řady kalibračních přístrojů. Kalibrátory (neprůhledné fólie z polyesteru) se umístí do kalibrační komory (komora rohovky určena k držení kalibrátorů) a čtou se na opacitometru. Kalibrační komora je určena k držení kalibrátorů přibližně ve stejné vzdálenosti mezi světlem a fotobuňkou, v jaké se umístí rohovky během měření zákalu. Opacitometr se nejdříve kalibruje na 0 zákalových jednotek s použitím kalibrační komory bez kalibrátoru. Potom se tři různé kalibrátory umístí jeden po druhém do kalibrační komory a měří se zákaly. Výsledkem kalibrátorů 1, 2 a 3 by měly být údaje o zákalu rovnající se příslušně nastaveným hodnotám 75, 150, a 225 zákalových jednotek, ± 5 %. |
B. 48 ZKUŠEBNÍ METODA ODDĚLENÉHO KUŘECÍHO OKA PRO ZJIŠŤOVÁNÍ LÁTEK S LEPTAVÝMI A SILNĚ DRÁŽDIVÝMI ÚČINKY NA OČI
ÚVOD
|
1. |
Zkušební metoda odděleného kuřecího oka (ICE – Isolated Chicken Eye) je zkušební metoda in vitro, kterou lze za určitých okolností a s některými omezeními použít pro klasifikaci látek a směsí jako látky s leptavými a silně dráždivými účinky na oči (1) (2) (3). Pro účely této zkušební metody jsou silně dráždivé látky definovány jako látky způsobující oční léze, které přetrvávají u králíků po dobu nejméně 21 dní po jejich podání. I když se metoda ICE nepovažuje za úplnou náhradu za oční test in vivo na králících, doporučuje se použít ji jako součást strategie stupňovitých zkoušek pro regulační klasifikaci a označování v rámci specifické oblasti použitelnosti (4) (5). Zkoušené látky a směsi (6), které jsou v této analýze pozitivní, lze klasifikovat jako látky s leptavými nebo silně dráždivými účinky na oči bez dalšího zkoušení na králících. Látka s negativním výsledkem zkoušky by si vyžádala zkoušení na králících s použitím strategie stupňovitého zkoušení, jak je uvedeno v metodice OECD 405 (7) (kapitola B. 5 této přílohy). |
|
2. |
Účelem této zkušební metody je popsat postupy používané k hodnocení potenciálních testovacích látek s leptavými nebo silně dráždivými účinky na oči měřené její schopností způsobit toxicitu v odstraněném kuřecím oku. Toxické účinky na rohovku se měří i) kvalitativním hodnocením zákalu, ii) kvalitativním hodnocením poškození epitelu na základě aplikace fluoresceinu do oka (zadržování fluoresceinu), iii) kvantitativním měřením zvýšené tloušťky (otok) a iv) kvalitativním hodnocením makroskopického morfologického poškození povrchu. Hodnocení zákalu a otoku rohovky a poškození po expozici zkoušené látce se posuzuje samostatně a potom se spojí za účelem odvození klasifikace dráždivých účinků na oči. |
|
3. |
Látky s dráždivými účinky na oči způsobující léze, které odezní nejpozději do 21 dní a nedráždivé látky byly rovněž zkoušeny s použitím zkušební metody ICE. Přesnost a spolehlivost zkušební metody ICE u látek těchto kategorií však nebyla oficiálně hodnocena. |
|
4. |
Definice jsou uvedeny v dodatku l. |
POČÁTEČNÍ POSOUZENÍ A OMEZENÍ
|
5. |
Tato zkušební metoda je založena na protokolu zkušební metody ICE Koordinačního výboru mezi různými organizacemi pro ověřování platnosti alternativních metod (ICCVAM) (8) zpracovanému v návaznosti na mezinárodní studii o ověřování platnosti (4) (5) (9) s přispěním Evropského střediska pro ověřování platnosti alternativních metod, Japonského střediska pro validaci alternativních metod a oddělení toxikologie a aplikované farmakologie TNO Quality of Life (Nizozemsko). Protokol vychází z informací získaných z uveřejněných protokolů a také z aktuálního protokolu, který používá TNO (10) (11) (12) (13) (14). |
|
6. |
Omezení stanovená pro tuto metodu jsou založena na míře falešné pozitivity pro alkoholy a na mírách falešné negativity pro pevné látky a smáčedla (viz bod 47) (4). Jsou-li látky v rámci těchto chemických a fyzikálních tříd vyřazeny z databáze, přesnost ICE v klasifikačních systémech EU, EPA a GHS je podstatně vyšší (4). Vycházeje z účelu této analýzy (tj. zjišťovat pouze látky s leptavými/silně dráždivými účinky na oči), míry falešné negativity nejsou kritické, protože tyto látky by se následně zkoušely na králících nebo jinými náležitě validovanými zkouškami in vitro v závislosti na požadavcích právních předpisů s využitím strategie stupňovitého zkoušení v přístupu založeném na vážení důkazů. Kromě toho současná databáze ověřování platnosti neumožňuje odpovídající hodnocení některých chemických tříd nebo tříd produktů (např. směsí). Výzkumníci by však mohli zvážit použití této zkušební metody pro zkoušení všech druhů látek (včetně směsí), přičemž kladný výsledek by mohl být přijat jako příznak reakce očí na leptavé nebo silně dráždivé látky. Kladné výsledky získané u alkoholů by se však měly interpretovat opatrně z důvodu rizika nepřiměřené předpovědi. |
|
7. |
Veškeré postupy u kuřecích očí by měly dodržovat nařízení a postupy použitelné na zkušebny pro zacházení s lidskými materiály nebo materiály získanými ze zvířat, které kromě jiného zahrnují tkáně a mimobuněčné tekutiny. Doporučují se univerzální laboratorní preventivní opatření (15). |
|
8. |
Omezení zkušební metody spočívá v tom, že i když přihlíží k některým účinkům na oči vyhodnoceným metodou zkoušení podráždění očí na králících a do určité míry i k jejich síle, nebere v úvahu poškození spojivky a duhovky. Ačkoli reverzibilitu lézí rohovky nelze ve zkušební metodě ICE hodnotit samu o sobě, na základě studií o očích králíků bylo přesto navrženo, že by se posouzení počáteční hloubky poškození rohovky mohlo použít k rozlišení mezi nevratnými a vratnými účinky (16). A konečně je třeba uvést, že zkušební metoda ICE neumožňuje posouzení potenciálu soustavné toxicity spojené s expozicí očí. |
|
9. |
Vyvíjí se úsilí, aby se dále popsala účelnost a omezení zkušební metody ICE pro zjišťování slabých dráždivých látek a nedráždivých látek (viz také bod 48). Uživatelům se rovněž doporučuje, aby organizacím pro ověřování platnosti poskytli vzorky a/nebo údaje pro oficiální hodnocení případného budoucího použití zkušební metody ICE, včetně zjišťování látek se slabými dráždivými a nedráždivými účinky na oči. |
|
10. |
Každá laboratoř, která poprvé provádí tuto analýzu, by měla použít osvědčené chemické látky uvedené v dodatku 2. Laboratoř může použít tyto chemické látky k prokázání své odborné způsobilosti v používání zkušební metody ICE před předložením údajů ICE pro regulační účely klasifikace nebezpečí. |
ZÁSADA ZKOUŠKY
|
11. |
Zkušební metoda ICE je organotypický model, který zajišťuje krátkodobé uchování kuřecího oka in vitro. V této zkušební metodě se poškození zkoušenou látkou posuzuje určením otoku a zákalu rohovky a zadržování fluoresceinu. Zatímco dva poslední parametry se týkají kvalitativního hodnocení, analýza otoku rohovky zajišťuje kvantitativní hodnocení. Každé měření se buď převádí na kvantitativní hodnotu používanou k výpočtu celkového ukazatele podráždění, nebo je přiřazeno kvalitativní kategorizaci, která se používá ke stanovení klasifikace leptavých a silné dráždivých účinků na oči in vitro. Každý z těchto výsledků potom může být použit k předvídání potenciálu zkoušené látky působit jako látka s leptavými a silně dráždivými účinky na oči in vivo (viz kritéria rozhodování). |
Zdroj a věk kuřecích očí
|
12. |
Tradičně se pro tuto analýzu používají kuřecí oči získané z jatek, kde se kuřata zabíjejí pro lidskou spotřebu, čímž se eliminuje potřeba laboratorních zvířat. Používají se pouze oči zdravých zvířat, které se považují za vhodné pro vstup do lidského potravinového řetězce. |
|
13. |
Ačkoli nebyla zpracována kontrolní studie pro hodnocení optimálního věku kuřat, věk a hmotnost kuřat tradičně používaných v této zkušební metodě odpovídá mladým kuřatům tradičně zpracovávaným na jatkách pro drůbež (tj. přibližně 7 týdnů staré, o váze 1,5 – 2,5 kg). |
Shromažďování a doprava očí do laboratoře
|
14. |
Hlavy by se měly odstranit ihned po usmrcení kuřat obvykle elektrickým šokem a naříznutím krku za účelem zbavení krve. Místní zdroj kuřat blízko laboratoře by měl být umístěn tak, aby hlavy kuřat mohly být dopraveny z jatek do laboratoře dostatečně rychle s cílem minimalizovat zkažení a/nebo bakteriální znečištění. Časový interval mezi shromážděním kuřecích hlav a použitím očí ve zkušební metodě ICE by měl být co nejkratší (zpravidla do dvou hodin) a měl by být prokázán, aby se nenarušily výsledky analýzy. Tyto výsledky vycházejí z kritérií výběru očí a také z reakcí na pozitivní a negativní kontroly. Všechny oči použité v analýze by měly být ze stejné skupiny očí shromážděných v určitý den. |
|
15. |
Protože oči se oddělují v laboratoři, neporušené hlavy se dopravují z jatek za okolní teploty v umělohmotných krabicích, které jsou navlhčeny ručníky namočenými v izotonickém fyziologickém roztoku. |
Kritéria výběru očí používaných v ICE
|
16. |
Oči, které mají vysoké základní zbarvení fluoresceinem (tj. > 0,5) nebo vysokou hodnotu zákalu rohovky (tj. > 0,5) se po jejich odstranění vyřadí. |
|
17. |
Každá zkušební skupina a souběžná pozitivní kontrola pozůstává nejméně ze třech očí. Skupina pro negativní kontrolu nebo pro kontrolu s rozpouštědlem (používá-li se jiné rozpouštědlo než fyziologický roztok) pozůstává nejméně z jednoho oka. |
POSTUP
Příprava očí
|
18. |
Oční víčka se opatrně vyříznou a přitom se dává pozor, aby se nepoškodila rohovka. Neporušenost rohovky se rychle posoudí kápnutím 2 % (objemové hmotnosti) fluoresceinu sodného aplikovaného na povrch rohovky po dobu několika vteřin, který se potom opláchne izotonickým fyziologickým roztokem. Oči ošetřené fluoresceinem se pak zkoumají pod mikroskopem se štěrbinovou lampou, aby se zajistilo, že se rohovka nepoškodí (tj. hodnoty zadržení fluoresceinu a zákalu rohovky ≤ 0,5). |
|
19. |
Není-li oko poškozeno, vyřízne se z lebky a přitom se dává pozor, aby se nepoškodila rohovka. Oční bulbus se vyjme z očnice tak, že se chirurgickou pinzetou pevně uchopí mžurka a oční sval se ustřihne zahnutými tupými nůžkami zakončenými hrotem. Je důležité zamezit poškození rohovky nadměrným tlakem (tj. kompresní artefakty). |
|
20. |
Když je oko vyjmuto z očnice, viditelná část očního nervu by se měla nechat spojena. Jakmile se oko vyjme z očnice, položí se na absorpční podložku a mžurka a jiné pojivové tkáně se ustřihnou. |
|
21. |
Odstraněné oko se nasadí na nerezavý ocelový držák s rohovkou ve svislé poloze. Držák se potom přenese do komory chladícího přístroje (16). Držáky by se měly v chladícím přístroji postavit tak, aby kapky izotonického fyziologického roztoku dostávala celá rohovka. Teplota komor chladicího přístroje by měla být řízena na 32 ± 1,5 °C. V dodatku 3 je schématický nákres typického chladícího přístroje a očních držáků, které je možné obchodně získat nebo zkonstruovat. Přístroje mohou být upraveny, aby splňovaly potřeby jednotlivé laboratoře (např. umístění různého počtu očí). |
|
22. |
Když se oči vloží do chladícího přístroje, znovu se prozkoumají pod mikroskopem se štěrbinovou lampou, aby se zjistilo, zda nebyly poškozeny během vyřezávání. Tloušťka rohovky by se v této době měla také měřit na vrcholu rohovky s použitím zařízení pro měření hlouby na mikroskopu se štěrbinovou lampou. Oči s: i) hodnotou zadržení fluoresceinu > 0,5; ii) zákalem rohovky > 0,5; nebo iii) jakýmikoli dalšími znaky poškození by se měly vyměnit. V případě očí nevyřazených na základě jakéhokoli z těchto kritérií se musí vyřadit jednotlivé oči s tloušťkou rohovky, která se o víc než 10 % odchyluje od střední hodnoty pro všechny oči. Uživatelé by si měli být vědomi toho, že mikroskopy se štěrbinovou lampou by mohly ukazovat měření různé tloušťky rohovky, je-li rozdílné nastavení šířky štěrbiny. Šířka štěrbiny by se měla nastavit na 0,095 mm. |
|
23. |
Poté, co byly oči prozkoumány a schváleny, inkubují se po dobu přibližně 45 až 60 minut, aby se uvedly do rovnováhy se zkušebním systémem před dávkováním. Po době vyrovnání se pro tloušťku rohovky a zákal zaznamená nulové referenční měření, které slouží jako základ (tj. čas = 0). Hodnota fluoresceinu stanovená při oddělování se pro tento koncový bod používá jako základní měření. |
Aplikace zkoušené látky
|
24. |
Oči se (v držáku) ihned po nulovém referenčním měření vyberou z chladícího přístroje, postaví se do vodorovné polohy a na rohovku se aplikuje zkoušená látka. |
|
25. |
Tekuté zkoušené látky se zpravidla zkoušejí neředěné, mohou se však ředit, pokud se to považuje za nutné (např. jako součást návrhu studie). Preferovaným ředidlem pro ředěné látky je fyziologický roztok. Za řízených podmínek lze však také použít alternativní ředidla, ale vhodnost jiných ředidel než fyziologického roztoku by se měla prokázat. |
|
26. |
Tekuté zkoušené látky se aplikují na rohovku tak, že celý povrch rohovky se rovnoměrně pokryje zkoušenou látkou; obvyklý objem je 0,03 ml. |
|
27. |
Podle možnosti by se pevné látky měly co nejjemněji položit do třecí misky a těrky nebo do srovnatelného drtícího prostředku. Prášek se aplikuje na rohovku tak, že se povrch stejnoměrně pokryje zkoušenou látkou; obvyklé množství je 0,03 g. |
|
28. |
Zkoušená látka (tekutá nebo pevná) se aplikuje po dobu 10 vteřin a pak se z oka opláchne izotonickým fyziologickým roztokem (přibližně 20 ml) při okolní teplotě. Oko (v držáku) se potom v původní svislé poloze vrátí do chladícího přístroje. |
Látky pro kontrolu
|
29. |
Do každého pokusu by měly být zařazeny souběžné negativní kontroly nebo kontroly s rozpouštědlem/vehikulem a pozitivní kontroly. |
|
30. |
Když se zkoušejí 100 % tekuté látky nebo pevné látky, fyziologický roztok se ve zkušební metodě ICE používá pro souběžnou negativní kontrolu, aby se zjistily nespecifické změny ve zkušebním systému a aby se zajistilo, že podmínky analýzy nebudou mít za následek nevhodnou dráždivou reakci. |
|
31. |
Když se zkoušejí zředěné tekuté látky, do zkušební metody se zařadí skupina pro souběžnou kontrolu s rozpouštědlem/vehikulem, aby se zjistily nespecifické změny ve zkušebním systému a aby se zajistilo, že podmínky analýzy nebudou mít za následek nevhodnou dráždivou reakci. Jak je uvedeno v bodě 25, lze použít pouze rozpouštědlo/vehikul, u kterého se prokázalo, že nemá nepříznivé účinky na zkušební systém. |
|
32. |
Do každého pokusu se zařadí známá látka s dráždivými účinky na oči jako souběžná pozitivní kontrola, aby se ověřilo, že je vyvolána odpovídající reakce. Protože analýza ICE se v této zkušební metodě používá ke zjišťování leptavých nebo silných dráždivých látek, pozitivní kontrola by měla být referenční látkou, která v této zkušební metodě vyvolá silnou reakci. Aby se však zajistilo, že proměnlivost v reakci na pozitivní kontrolu bude možné časem vyhodnotit, rozsah silné reakce by neměl být nadměrný. Měl by se vytvořit dostatek údajů in vitro pro pozitivní kontrolu, aby bylo možné vypočítat statisticky stanovený, přijatelný rozsah pozitivní kontroly. Nejsou-li údaje o zkušební metodě ICE z minulosti pro určitou pozitivní kontrolu k dispozici, bude nutné uskutečnit studie za účelem získání těchto informací. |
|
33. |
Příklady tekutých zkoušených látek pro pozitivní kontroly jsou 10 % kyselina octová nebo 5 % benzalkonium chlorid, zatímco příklady pevných zkoušených látek pro pozitivní kontroly jsou hydroxid sodný nebo imidazol. |
|
34. |
Srovnávací látky jsou účelné pro hodnocení potenciálu podráždění očí neznámými chemickými látkami nebo specifickými třídami chemických látek nebo produktů nebo pro hodnocení relativního potenciálu podráždění látkou s dráždivými účinky na oči ve specifickém rozmezí dráždivých reakcí. |
Měřené koncové body
|
35. |
Zkoušené rohovky se hodnotí předběžně ošetřené a hodnocení začíná ve 30, 75, 120, 180 a 240 minutách (± 5 minut) po oplachu po ošetření. Tyto časové body zajišťují odpovídající počet měření během čtyřhodinové doby zkoušení a přitom ponechávají dostatek času mezi měřeními, aby potřebná pozorování byla uskutečněna pro všechny oči. |
|
36. |
Hodnocené koncové body jsou zákal a otok rohovky, zadržování fluoresceinu a morfologické účinky (např. tvoření jizev nebo uvolňování epitelu). Všechny koncové body kromě zadržování fluoresceinu (který je stanoven pouze v předběžné úpravě a 30 minut po expozici zkoušené látce) se určují v každém výše uvedeném časovém bodu. |
|
37. |
Doporučují se fotografické snímky, aby se zdokumentoval zákal rohovky, zadržování fluoresceinu, morfologické účinky a histopatologie, pokud se provádí. |
|
38. |
Uživatelům se po konečné zkoušce doporučuje, aby po uplynutí doby čtyř hodin uložili oči do vhodného fixačního prostředku (např. neutrální pufrovaný formalín) pro případné histopatologické vyšetření. |
|
39. |
Otok rohovky se určuje měřením tloušťky rohovky, které se provádí optickým pachymetrem pod mikroskopem se štěrbinovou lampou. Vyjadřuje se jako procento a vypočítává se z měření tloušťky rohovky podle následujícího vzorce:
|
|
40. |
Střední procento otoku rohovky se u všech zkoušených očí vypočítává pro všechny časové body pozorování. Na základě nejvyšší střední hodnoty otoku rohovky pozorované v jakémkoli časovém bodu se potom každé zkoušené látce přidělí celková hodnota kategorie. |
|
41. |
Zákal rohovky se vypočítává s použitím plochy rohovky pro hodnocení, která je nejvíce zakalena. Střední hodnota zákalu rohovky se u všech zkoušených očí vypočítává pro všechny časové body pozorování. Na základě nejvyšší střední hodnoty zákalu rohovky pozorované v jakémkoli časovém bodě se potom každé zkoušené látce přidělí celková hodnota kategorie (tabulka 1). Tabulka 1 Hodnoty zákalu rohovky
|
|
42. |
Střední hodnota zadržování fluoresceinu se u všech zkoušených očí vypočítává pouze pro časový bod 30minutového pozorování, který se používá pro celkovou hodnotu kategorie přidělenou každé zkoušené látce (tabulka 2). Tabulka 2 Hodnoty zadržování fluoresceinu
|
|
43. |
Morfologické účinky zahrnují ‚jizvy‘ na epiteliálních buňkách rohovky, ‚uvolňování‘ epitelu, ‚zdrsnění‘ povrchu rohovky a ‚nalepení‘ zkoušené látky na rohovku. Tato zjištění se mohou ve své závažnosti měnit a mohou se vyskytovat souběžně. Klasifikace těchto zjištění je subjektivní podle interpretace výzkumníka. |
ÚDAJE A PODÁVÁNÍ ZPRÁV
Hodnocení údajů
|
44. |
Výsledky ze zákalu a otoku rohovky a zadržování fluoresceinu by se měly hodnotit zvlášť, aby se pro každý koncový bod vytvořila třída ICE. Třídy ICE pro každý koncový bod se pak spojí za účelem vytvoření klasifikace dráždivých účinků pro každou zkoušenou látku. |
Kritéria rozhodování
|
45. |
Poté, co byl každý koncový bod vyhodnocen, lze na základě předem určeného rozmezí přiřadit třídy ICE. Interpretace tloušťky (tabulka 3) a zákalu rohovky (tabulka 4) a zadržování fluoresceinu (tabulka 5) s použitím čtyř tříd ICE se uskutečňuje podle těchto měřítek: Tabulka 3 Klasifikační kritéria ICE pro tloušťku rohovky
Tabulka 4 Klasifikační kritéria ICE pro zákal
Tabulka 5 Klasifikační kritéria ICE pro střední zadržování fluoresceinu
|
|
46. |
Klasifikace celkových dráždivých účinků in vitro pro zkoušenou látku se posuzuje z údajů klasifikace dráždivých účinků, která odpovídá kombinaci kategorií získaných pro otok rohovky, zákal rohovky a zadržování fluoresceinu a s použitím schématu uvedeného v tabulce 6. Tabulka 6 Klasifikace celkových dráždivých účinků in vitro
|
|
47. |
Jak je uvedeno v bodě 1, pokud zkoušená látka není zjištěna jako látka s leptavými nebo silně dráždivými účinky na oči, mělo by se uskutečnit další zkoušení pro účely klasifikace a označování. Zkušební metoda ICE má celkovou přesnost 83 % (120/144) až 87 % (134/154), míru falešné pozitivity 6 % (7/122) až 8 % (9/116) a míru falešné negativity 41 % (13/32) až 50 % (15/30) pro identifikaci látek s leptavými a silně dráždivými účinky na oči, ve srovnání s údaji ze zkušební metody in vivo na očích králíků, klasifikovanými podle klasifikačních systémů EPA (1), EU (2) nebo GHS (3). V případě, že látky v určitých chemických (tj. alkoholy a smáčedla) a fyzikálních (tj. pevné látky) třídách jsou vyloučeny z databáze, přesnost ICE se v klasifikačních systémech EU, EPA a GHS pohybuje v rozmezí od 91 % (75/82) do 92 % (69/75), míra falešné pozitivity od 5 % (4/73) do 6 % (4/70) a míra falešné negativity od 29 % (2/7) do 33 % (3/9) (4). |
|
48. |
I když se klasifikace látek s leptavými nebo silně dráždivými účinky na oči pro zkoušenou látku nezíská, údaje ICE mohou být užitečné ve spojení s testovacími údaji z oční zkoušky in vivo na králících nebo z náležitě validované zkoušky in vitro, aby se dále vyhodnotila účelnost a omezení zkušební metody ICE pro zjištění slabých dráždivých a nedráždivých látek (dokument s pokyny o používání zkušebních metod oční toxicity in vitro se zpracovává). |
Kritéria přijetí studie
|
49. |
Zkouška se považuje za přijatelnou, pokud souběžné negativní kontroly s vehikulem/ rozpouštědlem a souběžné pozitivní kontroly poskytnou klasifikaci dráždivých účinků, které spadají příslušně do tříd nedráždivých a silně dráždivých/leptavých látek. |
Zpráva o zkoušce
|
50. |
Zpráva o zkoušce by měla zahrnovat tyto informace, pokud se týkají uskutečňování studie: Zkoušené látky a látky pro kontrolu
Informace týkající se zadavatele a zkušebního zařízení
Zdůvodnění použité zkušební metody a protokolu Úplnost zkušební metody Postup používaný k zajištění úplnosti (tj. přesnost a spolehlivost) zkušební metody v průběhu času (např. pravidelné zkoušení vhodných látek, využívání dosavadních údajů negativních a pozitivních kontrol). Kritéria pro přijatelnou zkoušku případně přijatelné rozsahy souběžných srovnávacích kontrol na základě dosavadních údajů. Zkušební podmínky
Výsledky
Posouzení výsledků Závěr |
LITERATURA
|
1) |
U.S. EPA (1996). Label Review Manual: 2nd Edition. EPA737-B-96-001. Washington, DC: U.S. Environmental Protection Agency. |
|
2) |
Nařízení Evropského parlamentu a Rady (ES) č. 1272/2008 ze dne 16. prosince 2008 o klasifikaci, označování a balení látek a směsí, o změně a zrušení směrnice 67/548/EHS a 1999/45/ES a o změně nařízení (ES) č. 1907/2006. Úř. věst. L 353, 31.12.2008, s. 1. |
|
3) |
Organizace spojených národů (OSN) (2007). Globálně harmonizovaný systém klasifikace a označování chemických látek (GHC), druhé revidované vydání, OSN New York a Ženeva, 2007. Dostupné na: [http://www.unece.org/trans/danger/publi/ghs/ghs_rev02/02files_e.html]. |
|
4) |
ICCVAM (2007). Zpráva o hodnocení zkušební metody – zkušební metody oční toxicity in vitro pro zjišťování látek se silně dráždivými a leptavými účinky na oči. Koordinační výbor mezi různými organizacemi pro ověřování platnosti alternativních metod (ICCVAM) a Středisko mezi různými organizacemi pro hodnocení alternativních toxikologických metod (NICEATM) národního toxikologického programu (NTP). Publikace NIH č.: 07-4517. Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_tmer.htm]. |
|
5) |
ESAC (2007). Prohlášení o uzavření retrospektivní studie ICCVAM o orgánových analýzách in vitro jako screeningové testy pro zjišťování potenciálních látek s leptavými a silně dráždivými účinky na oči. Dostupné na: [http://ecvam.jrc.it/index.htm]. |
|
6) |
Nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006 o registraci, hodnocení, povolování a omezování chemických látek, o zřízení Evropské agentury pro chemické látky, o změně směrnice 1999/45/ES a o zrušení nařízení Rady (EHS) č. 793/93, nařízení Komise (ES) č. 1488/94, směrnice Rady 76/769/EHS a směrnic Komise 91/155/EHS, 93/67/EHS, 93/105/ES a 2000/21/ES. Úř. věst. L 396, 30.12.2006, s. 1. |
|
7) |
OECD (2002). Metodika 405. Pokyn OECD pro zkoušení chemických látek. Akutní podráždění/poleptání očí. Dostupné na: [http://www.oecd.org/document/40/0,2340,en_2649_34377_37051368_1_1_1_1,00.html]. |
|
8) |
ICCVAM (2007). Doporučený protokol zkušební metody ICE ICCVAM. Ve: Zprávě o hodnocení zkušební metody ICCVAM – zkušební metody oční toxicity in vitro pro zjišťování látek se silně dráždivými a leptavými účinky na oči. Koordinační výbor mezi různými organizacemi pro ověřování platnosti alternativních metod (ICCVAM) a Středisko mezi různými organizacemi pro hodnocení alternativních toxikologických metod (NICEATM) národního toxikologického programu (NTP). Publikace NIH č.: 07-4517. Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_tmer.htm] |
|
9) |
ICCVAM. (2006). Současný stav zkušebních metod In Vitro pro zjišťování látek s leptavými a silně dráždivými účinky na oči: zkušební metoda odděleného kuřecího oka (ICE). Publikace NIH č.: 06-4513. Research Triangle Park: národní toxikologický program. Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_ice.htm]. |
|
10) |
Prinsen, M.K. and Koëter, B.W.M. (1993). Justification of the enucleated eye test with eyes of slaughterhouse animals as an alternative to the Draize eye irritation test with rabbits. Fd. Chem. Toxicol. 31:69-76. |
|
11) |
INVITTOX (1994). Protokol 80: Zkouška odstraněného kuřecího oka (CEET). Dostupné na: [http://ecvam.jrc.it/index.htm]. |
|
12) |
Balls, M., Botham, P.A., Bruner, L.H. and Spielmann H. (1995). The EC/HO international validation study on alternatives to the Draize eye irritation test. Toxicol. In Vitro 9:871-929. |
|
13) |
Prinsen, M.K. (1996). The chicken enucleated eye test (CEET): A practical (pre)screen for the assessment of eye irritation/corrosion potential of test materials. Food Chem. Toxicol. 34:291-296. |
|
14) |
Chamberlain, M., Gad, S.C., Gautheron, P. and Prinsen, M.K. (1997). IRAG Working Group I: Organotypic models for the assessment/prediction of ocular irritation. Food Chem. Toxicol. 35:23-37. |
|
15) |
Siegel, J.D., Rhinehart, E., Jackson, M., Chiarello, L., and the Healthcare Infection Control Practices Advisory Committee (2007). Guideline for Isolation Precautions: Preventing Transmission of Infectious Agents in Healthcare Settings. Dostupné na: [http://www.cdc.gov/ncidod/dhqp/pdf/isolation2007.pdf]. |
|
16) |
Maurer, J.K., Parker, R.D. and Jester, J.V. (2002). Extent of corneal injury as the mechanistic basis for ocular irritation: key findings and recommendations for the development of alternative assays. Reg. Tox. Pharmacol. 36:106-117. |
|
17) |
Burton, A.B.G., M. York and R.S. Lawrence (1981). The in vitro assessment of severe irritants. Fd. Cosmet.- Toxicol.- 19, 471-480. |
|
18) |
ICCVAM (2006). Základní dokument o přezkumu, současný stav zkušebních metod in vitro pro zjišťování látek s leptavými a silně dráždivými účinky na oči: zkušební metoda pro zákal a propustnost rohovky u skotu (BCOP). Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_bcop.htm]. |
|
19) |
ICCVAM (2006). Základní dokument o přezkumu, současný stav zkušebních metod in vitro pro zjišťování látek s leptavými a silně dráždivými účinky na oči: zkušební metoda odděleného kuřecího oka (ICE). Dostupné na: [http://iccvam.niehs.nih.gov/methods/ocutox/ivocutox/ocu_brd_bcop.htm]. |
Dodatek 1
DEFINICE
Přesnost: Přesnost shody mezi výsledky zkušební metody a přijatými referenčními hodnotami. Je to měření výsledku zkušební metody a jednoho aspektu „důležitosti“. Termín se často používá namísto „souladu“, kterým se rozumí podíl správných výsledků zkušební metody.
Srovnávací látka: Látka použitá jako norma pro srovnání se zkoušenou látkou. Srovnávací látka by měla mít tyto vlastnosti: i) nesporný a spolehlivý zdroj (nesporné a spolehlivé zdroje); ii) strukturální a funkční podobnost s třídou zkoušených látek; iii) známé fyzikální/chemické vlastnosti; iv) podpůrné údaje o známých účincích a v) známá síla v rozsahu žádoucí reakce.
Rohovka: Průhledná přední část oční bulvy, která zahrnuje duhovku a očnici a propouští světlo dovnitř oka.
Zákal rohovky: Měření rozsahu zákalu rohovky po expozici zkoušené látce. Zvýšený zákal rohovky je příznačný pro poškození rohovky.
Otok rohovky: Objektivní měření rozsahu zduření rohovky ve zkoušce ICE po expozici zkoušené látce. Vyjadřuje se procentuálně a vypočítává se z měření základní tloušťky rohovky (před dávkováním) a tloušťky zaznamenávané v pravidelných intervalech po vystavení zkoušené látce ve zkoušce ICE. Stupeň otoku rohovky je příznačný pro poškození rohovky.
Kategorie 1 EPA: Zasažení poleptáním (nevratné poškození oční tkáně) nebo zasažení rohovky či dráždění přetrvávající déle než 21 dní (1).
Kategorie R41 EU: Tvorba poškození tkání v oku nebo závažné fyzikální slábnutí vidění po aplikaci zkoušené látky na přední plochu oka, které není plně vratné do 21 dní od aplikace (2).
Míra falešné negativity: Podíl všech pozitivních látek falešně zjištěných zkušební metodou jako negativní. Je to jeden z ukazatelů výsledku zkušební metody.
Míra falešné pozitivity: Podíl všech negativních látek falešně zjištěných zkušební metodou jako pozitivní. Je to jeden z ukazatelů výsledku zkušební metody.
Zadržování fluoresceinu: Subjektivní měření rozsahu fluoresceinu sodného ve zkoušce ICE, který je zadržován buňkami epitelu v rohovce po expozici zkoušené látce. Stupeň zadržování fluoresceinu je příznačný pro poškození epitelu rohovky.
GHS (Globálně harmonizovaný systém klasifikace a označování chemických látek): Systém klasifikace chemických látek (látek a směsí) podle standardizovaných typů a úrovní fyzikálních, zdravotních a environmentálních rizik a odpovídajícího označpvání pomocí prvků informací o nebezpečnosti, jako jsou výstražné symboly nebezpečnosti, signální slova, standardní věty o nebezpečnosti, pokyny pro bezpečné zacházení a bezpečnostní listy, aby byly poskytnuty informace o jejich nepříznivých účincích s ohledem na ochranu lidí (včetně zaměstnavatelů, zaměstnanců, dopravců, spotřebitelů a respondérů nebezpečí) a životního prostředí (3).
Kategorie 1 GHS: Tvorba poškození tkání v oku nebo závažné fyzikální slábnutí vidění po aplikaci zkoušené látky na přední plochu oka, které není plně vratné do 21 dní od aplikace (3).
Nebezpečnost: Základní charakteristika látky nebo situace, která má potenciál vyvolat nepříznivé účinky, jsou-li organismus, systém nebo (sub)populace vystaveny této látce.
Negativní kontrola: Nezkoušená replika, která obsahuje všechny složky zkušebního systému. Tento vzorek se zpracovává se vzorky zkoušené látky a jinými kontrolními vzorky, aby se určilo, zda rozpouštědlo vzájemně reaguje se zkušebním systémem.
Nedráždivá látka: Látky, které nejsou klasifikovány jako látky s dráždivými účinky na oči kategorie I, II, nebo III EPA; kategorie R41 nebo R36 EU; nebo kategorie 1, 2A, nebo 2B GHS (1)(2)(3).
Látka s leptavými účinky na oči: a) Látka, která způsobuje nevratné poškození tkání očí. b) Látky, které jsou klasifikovány jako látky s dráždivými účinky na oči kategorie 1 GHS, kategorie I EPA nebo kategorie R41 EU (1)(2)(3).
Látka s dráždivými účinky na oči: a) látka, která způsobuje nevratnou změnu v oku po aplikaci na přední plochu oka; b) látky, které jsou klasifikovány jako látky s dráždivými účinky na oči kategorie II nebo III EPA, kategorie R36 EU nebo kategorie 2A nebo 2B GHS (1) (2) (3).
Silně dráždivá látka: a) Látka, která způsobuje poškození tkání v oku po aplikaci na přední plochu oka, které není vratné do 21 dní od aplikace, nebo způsobuje vážné fyzické snížení vidění. b) Látky, které jsou klasifikovány jako látky s dráždivými účinky na oči kategorie 1 GHS, kategorie I EPA nebo kategorie R41 EU (1)(2)(3).
Pozitivní kontrola: Replika obsahující všechny složky zkušebního systému a zkoušená s látkou, o níž je známo, že způsobuje pozitivní reakci. Aby se zajistilo, že proměnlivost v reakci na pozitivní kontrolu bude možné časem vyhodnotit, rozsah silné reakce by neměl být nadměrný.
Spolehlivost: Měření rozsahu, v jakém se zkušební metoda může časem použít opakovaně v laboratořích a mezi laboratořemi, když se provádí s použitím stejného protokolu. Hodnotí se to výpočtem laboratorní a mezilaboratorní reprodukovatelnosti a laboratorní opakovatelnosti.
Mikroskop se štěrbinovou lampou: Přístroj používaný k přímému vyšetření oka se zvětšením pod binokulárním mikroskopem a vytvořením stereoskopického, přímého obrazu. Ve zkušební metodě ICE se tento přístroj používá k prohlížení předních struktur kuřecího oka a také k objektivnímu měření tloušťky rohovky s přídavným zařízením na měření hloubky.
Kontrola s rozpouštědlem/vehikulem: Neošetřený vzorek obsahující všechny složky zkušebního systému, včetně rozpouštědla nebo vehikulu, který se zpracovává s ošetřenou zkoušenou látkou a jinými kontrolními vzorky, aby se zjistila základní reakce vzorků zkoušených se zkoušenou látkou rozpuštěnou ve stejném rozpouštědle nebo vehikulu. Pokud se vzorek zkouší se souběžnou negativní kontrolou, ukazuje také, zda rozpouštědlo nebo vehikul vzájemně reaguje se zkušebním systémem.
Stupňovité zkoušení: Strategie postupného zkoušení, kde se všechny existující informace o zkoušené látce přezkoumávají ve stanoveném pořadí s použitím postupu váhy důkazů na každém stupni, aby se zjistilo, zda je k dispozici dost informací pro rozhodnutí o klasifikaci nebezpečnosti, než se postoupí do dalšího stupně. Pokud potenciál dráždivých účinků zkoušené látky lze určit na základě existujících informací, další zkoušení není nutné. Jestliže na základě existujících informací nelze určit potenciál dráždivých účinků zkoušené látky, použije se stupňovitý postupný postup zkoušení na zvířatech, dokud se neurčí jednoznačná klasifikace.
Validovaná zkušební metoda: Zkušební metoda, pro kterou byly zpracovány validační studie s cílem určit důležitost (včetně přesnosti) a spolehlivost pro specifický účel. Je nutné poznamenat, že validovaná zkušební metoda nemusí poskytnout postačující výsledek z hlediska přesnosti a spolehlivosti, aby byla shledána přijatelnou pro navržený účel.
Váha důkazů: Postup zvažování silných a slabých stránek různých informací v dosahování a podpoře závěru týkajícího se potenciálu nebezpečnosti látky.
Dodatek 2
VHODNÉ CHEMICKÉ LÁTKY PRO ZKUŠEBNÍ METODU ICE
Než laboratoře rutinně použijí zkušební metodu, která dodržuje tuto zkušební metodu, měly by prokázat svou odbornou způsobilost správným určením klasifikace 10 látek s dráždivými účinky na oči doporučených v tabulce 1. Tyto látky byly vybrány tak, aby představovaly rozsah reakcí pro místní podráždění/poleptání očí, který vychází z výsledků očních zkoušek in vivo na králících (TG 405) (tj. kategorie 1, 2A, 2B nebo neklasifikované či označené podle GHS OSN (3)(7). S přihlédnutím k validované účelnosti těchto analýz (tj. zjišťování pouze látek s leptavými/silně dráždivými účinky na oči) však existují pouze dva výsledky zkoušky pro klasifikační účely (leptavá/silně dráždivá látka nebo neleptavá/slabá dráždivá látka), aby byla prokázána odborná způsobilost. Dalším kritériem výběru bylo to, zda látka je komerčně dostupná, zda jsou k dispozici kvalitní referenční údaje in vivo a zda jsou k dispozici kvalitní údaje ze dvou metod in vitro, pro které byly zpracovány metodiky. Z tohoto důvodu byly dráždivé látky vybrány z doporučeného seznamu 122 referenčních látek ICCVAM pro ověření platnosti zkušebních metod oční toxicity in vitro (viz dodatek H: Seznam doporučených referenčních látek ICCVAM) (4). Referenční údaje jsou dostupné v základním dokumentu o přezkumu ICCVAM pro zkušební metodu pro zákal a propustnost rohovky u skotu (BCOP) a zkušební metodu odděleného kuřecího oka (ICE) (18) (19).
Tabulka 1
Doporučené látky k prokázání odborné způsobilosti pro ICE
|
Chemická látka |
CASRN |
Třída chemických látek (9) |
Fyzikální forma |
Klasifikace (10) in vivo |
Klasifikace (11) in vitro |
|
Benzalkoniumchlorid (5 %) |
8001-54-5 |
Oniová sloučenina |
Tekutá |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Chlorhexidin |
55-56-1 |
Amin, amidin |
Pevná |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Dibenzoyl-L–tartarová kyselina |
2743-38-6 |
Karboxylová kyselina, ester |
Pevná |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Imidazol |
288-32-4 |
Heterocyklická |
Pevná |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Kyselina trichloroctová (30 %) |
76-03-9 |
Karboxylová kyselina |
Tekutá |
Kategorie 1 |
Leptavá/silně dráždivá látka |
|
Dichlorobenzoylchlorid |
4659-45-4 |
Acylhalogenid |
Tekutá |
Kategorie 2A |
Neleptavá/slabá dráždivá látka |
|
Ethyl-2-metylaceto–acetát |
609-14-3 |
Keton, ester |
Tekutá |
Kategorie 2B |
Neleptavá/slabá dráždivá látka |
|
Dusičnan amonný |
6484-52-2 |
Anorganická sůl |
Pevná |
Kategorie 2A |
Neleptavá/slabá dráždivá látka |
|
Glycerol |
56-81-5 |
Alkohol |
Tekutá |
Neoznačená |
Neleptavá/slabá dráždivá látka |
|
n-hexan |
110-54-3 |
Uhlovodík (acyklický) |
Tekutá |
Neoznačená |
Neleptavá/slabá dráždivá látka |
|
Zkratky: CASRN = registrační číslo podle služby chemických abstrakt |
|||||
Dodatek 3
Schématický nákres chladícího přístroje a držáků očí ICE
Další obecně použitelné popisy chladícího přístroje a držáku očí viz Burton et al. (17)
(1) Třídy chemických látek byly přiděleny každé zkoušené látce s použitím standardního klasifikačního schématu na základě klasifikačního systému Národní knihovny názvů léků a léčivých látek (MeSH) (dostupné na http//www.nlm.nih.gov/mesh).
(2) Založena na oční zkoušce in vivo na králících (OECD TG 405) s použitím GHS OSN (3)(7).
(3) Založena na výsledcích v BCOP a ICE.
(4) Poskytnuté rozměry vycházejí z držáku rohovek, který se používá u krav ve věku od 12 do 60 měsíců. V případě, že se používají zvířata ve věku od 6 do 12 měsíců, držák by musel být zkonstruován tak, aby každá komora měla objem 4 ml a aby každá vnitřní komora měla průměr 1,5 cm a hloubku 2,2 cm. U každého nově zkonstruovaného držáku rohovek je velmi důležité, aby poměr exponované plochy povrchu rohovky k objemu zadní komory byl stejný jako poměr v tradičním držáku rohovek. Je to nutné k zajištění, že hodnoty propustnosti budou stanoveny správně pro výpočet IVIS za pomoci navrženého vzorce.
(5) Hodnoty otoku rohovky jsou použitelné pouze, měří-li se tloušťka pod mikroskopem se štěrbinovou lampou Haag-Streit BP900 s měřícím přístrojem na měření hloubky č. I a nastavením šířky štěrbiny na 9½, což se rovná 0,095 mm. Uživatelé by si měli být vědomi toho, že mikroskopy se štěrbinovou lampou by mohly ukazovat měření různé tloušťky rohovky, je-li rozdílné nastavení šířky štěrbiny.
(6) Viz tabulka 1.
(7) Viz tabulka 2.
(8) Výskyt těchto kombinací je méně pravděpodobný.
(9) Chemické třídy byly přiděleny každé zkoušené látce s použitím standardního klasifikačního schématu na základě klasifikačního systému Národní knihovny názvů léků a léčivých látek (MeSH) (dostupný na http//www.nlm.nih.gov/mesh).
(10) Založena na oční zkoušce in vivo na králících (OECD TG 405) a s použitím GHS OSN (3)(7).
(11) Založena na výsledcích v BCOP a ICE.