|
Kapitoly 1 až 3 (F) se nahrazují tímto:
„KAPITOLA 1
Veterinární osvědčení
pro zpracované živočišné bílkoviny jiné než získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny, a jsou určeny k odeslání do Evropské unie nebo k tranzitu přes její území (2)
 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17.
 Text obrazu
Text obrazu
I.18. Popis zboží
I.19. Kód zboží (kód HS)
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
I.25. Zboží osvědčené pro:
Krmivo Technické využití Výroba krmiva pro zvířata v zájmovém chovu
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Druh zboží
Výrobní závod
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny jiné než získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a), zejména pokud jde o článek 10 uvedeného nařízení, a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu X kapitolu II oddíl 1 a přílohu XIV kapitolu I uvedeného nařízení, a potvrzuji, že:
II.1. zpracované živočišné bílkoviny nebo produkt popsaný výše obsahují výhradně zpracované živočišné bílkoviny, které nejsou určeny k lidské spotřebě a které:
a) byly připraveny a skladovány v zařízení nebo podniku schváleném a dozorovaném příslušným orgánem v souladu s článkem 24 nařízení (ES) č. 1069/2009; a
b) byly připraveny výhradně z těchto vedlejších produktů živočišného původu:
(2) buď [- těla poražených zvířat a jejich části, nebo v případě zvěře těla usmrcených zvířat nebo jejich části, které jsou podle právních předpisů Unie vhodné k lidské spotřebě, avšak z obchodních důvodů nejsou k lidské spotřebě určeny;]
(2) a/nebo [- jatečně upravená těla a níže uvedené části pocházející buď ze zvířat, která byla poražena na jatkách a po prohlídce před porážkou byla shledána jako způsobilá k porážce k lidské spotřebě, nebo těla a níže uvedené části zvěře usmrcené k lidské spotřebě v souladu s právními předpisy Unie:
i) jatečně upravená těla nebo těla zvířat a jejich části, které byly v souladu s právními předpisy Unie prohlášeny za nevhodné k lidské spotřebě, avšak nevykazovaly žádné příznaky onemocnění přenosného na člověka nebo zvířata;
ii) hlavy drůbeže;
iii) kůže a kožky, včetně jejich odřezků a plátků, rohy a končetiny, včetně článků prstů, zápěstních a záprstních kůstek, nártů a zánártí;
iv) prasečí štětiny;
v) peří;]
(2) a/nebo [- krev zvířat, která nevykazovala žádné příznaky onemocnění přenosného krví na člověka nebo zvířata, která byla poražena na jatkách a která byla po prohlídce před porážkou shledána způsobilými k porážce k lidské spotřebě v souladu s právními předpisy Unie;]
(2) a/nebo [- vedlejší produkty živočišného původu, které vznikají při výrobě produktů určených k lidské spotřebě, včetně odtučněných kostí, škvarků nebo kalu z odstředivky nebo separátoru ze zpracování mléka;]
(2) a/nebo [- produkty živočišného původu nebo potraviny obsahující produkty živočišného původu, které z obchodních důvodů nebo z důvodů problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny k lidské spotřebě;]
(2) a/nebo [- krev, placenta, vlna, peří, srst, rohy, odřezky kopyt a paznehtů a syrové mléko pocházející ze živých zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto produktem na člověka nebo zvířata;]
(2) a/nebo [- vodní živočichové a jejich části, kromě mořských savců, kteří nevykazovali žádné příznaky onemocnění přenosných na člověka nebo zvířata;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních živočichů pocházející ze zařízení nebo podniků na výrobu produktů určených k lidské spotřebě;]
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny jiné než získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) a/nebo [- níže uvedený materiál pocházející ze zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto materiálem na člověka nebo zvířata:
i) ulity měkkýšů a korýšů s měkkými tkáněmi nebo masem;
ii) tento materiál pocházející ze suchozemských zvířat:
— vedlejší produkty z líhní,
— vejce,
— vedlejší produkty z vajec, včetně vaječných skořápek;
iii) jednodenní kuřata usmrcená z obchodních důvodů;]
(2) a/nebo [- vodní a suchozemští bezobratlí živočichové, kromě druhů patogenních pro člověka nebo zvířata a hmyzu;]
(2) a/nebo [- zvířata z řádů hlodavců (Rodentia) a zajícovců (Lagomorpha) a jejich části, kromě materiálu kategorie 1 uvedeného v čl. 8 písm. a) bodech iii), iv) a v) a materiálu kategorie 2 uvedeného v čl. 9 písm. a) až g) nařízení (ES) č. 1069/2009;]
a
c) byly podrobeny této metodě zpracování:
(2) buď [zahřátí na teplotu v jádře vyšší než 133 °C po dobu alespoň 20 minut bez přerušení a při tlaku (absolutním) alespoň 3 bary získaném nasycenou parou s velikostí částic před zpracováním maximálně 50 mm;]
(2) nebo [v případě živočišných bílkovin nepocházejících ze savců, s výjimkou rybí moučky, zpracovatelské metodě 1-2-3-4-5-7 (uveďte zpracovatelskou metodu) podle přílohy IV kapitoly III nařízení (EU) č. 142/2011;]
(2) nebo [v případě rybí moučky zpracovatelské metodě 1-2-3-4-5-6-7 (uveďte zpracovatelskou metodu) podle přílohy IV kapitoly III nařízení (EU) č. 142/2011;]
(2) nebo [v případě prasečí krve zpracovatelské metodě 1-2-3-4-5-7 … (uveďte zpracovatelskou metodu) podle přílohy IV kapitoly III nařízení (EU) č. 142/2011, přičemž v případě metody 7 se na celou hmotu použije tepelné ošetření při teplotě alespoň 80 °C;]
II.2. příslušný orgán bezprostředně před odesláním vyšetřil namátkově vybraný vzorek a shledal jej v souladu s těmito normami (3):
Salmonella: nepřítomnost v 25 g produktu: n = 5, c = 0, m = 0, M = 0
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 300 v 1 g;
II.3. produkt prošel všemi preventivními opatřeními k zabránění kontaminace patogenními původci po ošetření;
II.4. konečný produkt byl:
(2) buď [zabalen do nových nebo sterilizovaných pytlů,]
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny jiné než získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) nebo [přepravován volně ložený v kontejnerech nebo jiných dopravních prostředcích, které byly před použitím důkladně vyčištěny a vydezinfikovány,]
které jsou opatřeny etiketami s nápisem „NENÍ URČENO K LIDSKÉ SPOTŘEBĚ“;
II.5. konečný produkt byl uložen v uzavřeném skladišti;
(2) [II.6. zpracované živočišné bílkoviny nebo produkt popsaný výše obsahují vedlejší produkty živočišného původu z přežvýkavců nebo jsou z nich získány a:
(2) buď [pocházejí ze země nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE, a]]
(2) nebo [pocházejí ze země nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž byl zjištěn domácí případ BSE, a vedlejší produkt živočišného původu nebo získaný produkt byl získán ze zvířat narozených po datu, od kterého byl v uvedené zemi nebo oblasti účinně vymáhán zákaz krmení přežvýkavců masokostní moučkou a škvarky získanými z přežvýkavců, jak jsou definovány v Kodexu zdraví suchozemských živočichů OIE, a]
(2) buď [jsou získány z přežvýkavců jiných než skot, ovce nebo kozy;]
(2) nebo [jsou získány ze skotu, ovcí nebo koz a neobsahují dále uvedené složky ani z nich nebyly získány:
(2) buď [materiál pocházející ze skotu, ovcí a koz jiný než získaný ze zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE;]]
(2) nebo [a) specifikovaný rizikový materiál, jak je definován v bodě 1 přílohy V nařízení Evropského parlamentu a Rady (ES) č. 999/2001 (4);
b) strojně oddělené maso získané z kostí skotu, ovcí nebo koz s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím Komise 2007/453/ES (5) do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE;
c) vedlejší produkt živočišného původu nebo získaný produkt ze skotu, ovcí nebo koz, které byly po omráčení usmrceny lacerací centrální nervové tkáně pomocí podlouhlého tyčovitého nástroje zavedeného do dutiny lebeční nebo prostřednictvím plynové injekce do dutiny lebeční, s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE;]]]
II.7. zpracované živočišné bílkoviny nebo produkt popsaný výše:
(2) buď [neobsahují mléko nebo mléčné výrobky pocházející z ovcí nebo koz ani nejsou určeny pro krmení hospodářských zvířat jiných než kožešinových zvířat;]
(2) nebo [obsahují mléko nebo mléčné výrobky pocházející z ovcí nebo koz a jsou určeny pro krmení hospodářských zvířat jiných než kožešinových zvířat a mléko nebo mléčné výrobky:
a) jsou získány z ovcí a koz, které byly nepřetržitě od narození chovány v zemi, v níž jsou splněny tyto podmínky:
i) klasická klusavka je povinná hlášením;
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny jiné než získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
ii) funguje systém osvěty, sledování a dohledu;
iii) na hospodářství s chovem ovcí nebo koz se uplatňují úřední omezení v případě podezření na TSE nebo potvrzení klasické klusavky;
iv) ovce a kozy postižené klasickou klusavkou jsou usmrceny a zlikvidovány;
v) krmení ovcí a koz masokostní moučkou nebo škvarky z přežvýkavců, jak jsou definovány v Kodexu zdraví suchozemských živočichů Světové organizace pro zdraví zvířat (OIE), bylo zakázáno a zákaz byl účinně vymáhán v celé zemi přinejmenším po dobu předchozích sedmi let;
b) pocházejí z hospodářství, pro která neplatí žádné úřední omezení z důvodu podezření na výskyt TSE;
c) pocházejí z hospodářství, v nichž přinejmenším po dobu předchozích sedmi let nebyl diagnostikován žádný případ klasické klusavky, nebo po potvrzení případu klasické klusavky:
(2) buď [byly usmrceny a zlikvidovány nebo poraženy všechny ovce a kozy v hospodářství s výjimkou plemenných beranů genotypu ARR/ARR, chovných bahnic nesoucích alespoň jednu alelu ARR a žádnou alelu VRQ a dalších ovcí nesoucích alespoň jednu alelu ARR;]
(2) nebo [byla všechna zvířata, u nichž byla klasická klusavka potvrzena, usmrcena a zlikvidována a na hospodářství se alespoň po dva roky od potvrzení posledního případu klasické klusavky vztahuje intenzivnější sledování TSE, včetně vyšetření všech následujících zvířat starších 18 měsíců, s výjimkou ovcí genotypu ARR/ARR, na přítomnost TSE s negativním výsledkem v souladu s laboratorními metodami stanovenými v příloze X kapitole C bodě 3.2 nařízení (ES) č. 999/2001:
— zvířata, která byla poražena k lidské spotřebě, a
— zvířata, která uhynula nebo byla usmrcena v daném hospodářství, avšak nebyla usmrcena v rámci kampaně eradikace nákazy;]]
II.8. zpracované živočišné bílkoviny nebo produkt popsaný výše obsahují vedlejší produkty živočišného původu z nepřežvýkavců nebo jsou z nich získány a v souladu s prohlášením odesílatele v kolonce I.1.
(2) buď [nejsou určeny k výrobě krmiv pro hospodářská zvířata jiná než kožešinová zvířata.]
(2) (6) nebo [jsou určeny k výrobě krmiv pro nepřežvýkavá hospodářská zvířata jiná než kožešinová zvířata a odesílatel se zavázal zajistit, že vstupnímu stanovišti hraniční kontroly budou poskytnuty výsledky zkoušení podle metod stanovených v příloze VI nařízení Komise (ES) č. 152/2009 (7).]
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit přes Evropskou unii; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
— Kolonka I.12.: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit. Produkty smí být při tranzitu skladovány pouze ve svobodných pásmech, svobodných skladech a celních skladech.
— Kolonka I.15.: Registrační číslo (železničních vagonů nebo kontejneru a nákladních automobilů), číslo letu (letadla) nebo název (plavidla); informace je třeba poskytnout v případě vykládky a opětovného naložení.
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny jiné než získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
— Kolonka I.19.: Použijte příslušný kód HS: 05.05, 05.06, 05.07, 05.11, 23.01 nebo 23.09.
— Kolonka I.25.: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26. a I.27.: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
— Kolonka I.28.: Druh: vyberte: Aves, Ruminantia, Suidae, Mammalia kromě Ruminantia nebo Suidae, Pesca, Mollusca, Crustacea, bezobratlí kromě Mollusca a Crustacea. V případě ryb ve farmovém chovu uveďte vědecký název ryby.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
(2) Nehodící se škrtněte.
(3) Kde:
n = počet vzorků, které mají být vyšetřeny;
m = prahová hodnota počtu bakterií; výsledek je považován za uspokojivý, jestliže počet bakterií ve všech vzorcích nepřekročí m;
M = maximální hodnota počtu bakterií; výsledek je považován za neuspokojivý, pokud počet bakterií v jednom nebo více vzorcích je roven nebo vyšší než M; a
c = počet vzorků, jejichž bakteriální počet smí být v rozmezí mezi m a M, přičemž vzorek je ještě stále považován za přípustný, pokud je bakteriální počet ostatních vzorků roven m nebo nižší.
(4) Úř. věst. L 147, 31.5.2001, s. 1.
(5) Úř. věst. L 172, 30.6.2007, s. 84.
(6) Osoba zodpovědná za zásilku uvedená v kolonce I.6. musí zajistit, aby v případě, že zpracované živočišné bílkoviny nebo produkt popsaný v tomto veterinárním osvědčení mají být určeny k výrobě krmiva pro nepřežvýkavá hospodářská zvířata jiná než kožešinová zvířata, byla zásilka podrobena zkoušení podle metod stanovených v příloze VI nařízení (ES) č. 152/2009, aby se ověřila nepřítomnost nepovolených složek živočišného původu. Informace týkající se výsledku takového zkoušení musí být při předložení zásilky na stanovišti hraniční kontroly EU připojeny k tomuto veterinárnímu osvědčení.
(7) Úř. věst. L 54, 26.2.2009, s. 1.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro osobu zodpovědnou za zásilku v Evropské unii: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
KAPITOLA 1a
Veterinární osvědčení
pro zpracované živočišné bílkoviny získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny, a jsou určeny k odeslání do Evropské unie nebo k tranzitu přes její území (2)
 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17.
I.18. Popis zboží
I.19. Kód zboží (kód HS)
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
 Text obrazu
Text obrazu
I.25. Zboží osvědčené pro:
Krmivo Technické využití Výroba krmiva pro zvířata v zájmovém chovu
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Druh zboží
Výrobní závod
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a), zejména pokud jde o článek 10 uvedeného nařízení, a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu X kapitolu II oddíl 1 a přílohu XIV kapitolu I uvedeného nařízení, a potvrzuji, že:
II.1. zpracované živočišné bílkoviny získané z farmově chovaného hmyzu nebo produkt popsaný výše obsahují výhradně zpracované živočišné bílkoviny, které nejsou určeny k lidské spotřebě a které:
a) byly připraveny a skladovány v zařízení nebo podniku schváleném a dozorovaném příslušným orgánem v souladu s článkem 24 nařízení (ES) č. 1069/2009 a
b) byly připraveny výhradně z farmově chovaného hmyzu těchto druhů:
(2) buď [- bráněnka (Hermetia illucens);]
(2) a/nebo [- moucha domácí (Musca domestica);]
(2) a/nebo [- potemník moučný (Tenebrio molitor);]
(2) a/nebo [- potemník stájový (Alphitobius diaperinus);]
(2) a/nebo [- cvrček domácí (Acheta domesticus);]
(2) a/nebo [- cvrček krátkokřídlý (Gryllodes sigillatus);]
(2) a/nebo [- cvrček banánový (Gryllus assimilis)]
a
c) byly zpracovány v souladu s metodou [1]-[2]-[3]-[4]-[5]-[7] (2) stanovenou v příloze IV kapitole III nařízení (EU) č. 142/2011;
a
d) substrát ke krmení farmově chovaného hmyzu smí obsahovat pouze produkty, které nejsou živočišného původu, nebo tyto produkty živočišného původu materiálu kategorie 3:
— rybí moučka,
— krevní výrobky z nepřežvýkavců,
— hydrogenfosforečnan vápenatý a fosforečnan vápenatý živočišného původu,
— hydrolyzované bílkoviny z nepřežvýkavců,
— hydrolyzované bílkoviny z kůží a kožek přežvýkavců,
— želatina a kolagen z nepřežvýkavců,
— vejce a výrobky z vajec,
— mléko, mléčné výrobky, produkty získané z mléka a mlezivo,
— med,
— tavené/škvařené tuky
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
a
e) substrát ke krmení hmyzu a hmyz nebo jeho larvy nebyly ve styku s jinými materiály živočišného původu než materiály uvedenými v písmenu d) a substrát neobsahoval hnůj, odpad ze stravovacích zařízení nebo jiný odpad;
II.2. příslušný orgán bezprostředně před odesláním vyšetřil namátkově vybraný vzorek a shledal jej v souladu s těmito normami (3):
Salmonella: nepřítomnost v 25 g produktu: n = 5, c = 0, m = 0, M = 0
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 300 v 1 g;
II.3. produkt prošel všemi preventivními opatřeními k zabránění kontaminace patogenními původci po ošetření;
II.4. konečný produkt byl:
(2) buď [zabalen do nových nebo sterilizovaných pytlů,]
(2) nebo [přepravován volně ložený v kontejnerech nebo jiných dopravních prostředcích, které byly před použitím důkladně vyčištěny a vydezinfikovány,]
které jsou opatřeny etiketami s nápisem „NENÍ URČENO K LIDSKÉ SPOTŘEBĚ / ZPRACOVANÉ HMYZÍ BÍLKOVINY – NENÍ URČENO PRO POUŽITÍ V KRMIVECH PRO HOSPODÁŘSKÁ ZVÍŘATA KROMĚ ŽIVOČICHŮ POCHÁZEJÍCÍCH Z AKVAKULTURY A KOŽEŠINOVÝCH ZVÍŘAT“;
II.5. konečný produkt byl uložen v uzavřeném skladišti;
(2) [II.6. zpracované živočišné bílkoviny nebo produkt popsaný výše obsahují vedlejší produkty živočišného původu z přežvýkavců nebo jsou z nich získány a:
(2) buď [pocházejí ze země nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE, a]]
(2) nebo [pocházejí ze země nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž byl zjištěn domácí případ BSE, a vedlejší produkt živočišného původu nebo získaný produkt byl získán ze zvířat narozených po datu, od kterého byl v uvedené zemi nebo oblasti účinně vymáhán zákaz krmení přežvýkavců masokostní moučkou a škvarky získanými z přežvýkavců, jak jsou definovány v Kodexu zdraví suchozemských živočichů OIE, a]]
(2) buď [jsou získány z přežvýkavců jiných než skot, ovce nebo kozy;]]
(2) nebo [jsou získány ze skotu, ovcí nebo koz a neobsahují dále uvedené složky ani z nich nebyly získány:
(2) buď [materiál pocházející ze skotu, ovcí a koz jiný než získaný ze zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE;]]
(2) nebo [a) specifikovaný rizikový materiál, jak je definován v bodě 1 přílohy V nařízení Evropského parlamentu a Rady (ES) č. 999/2001 (4);
b) strojně oddělené maso získané z kostí skotu, ovcí nebo koz s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím Komise 2007/453/ES (5) do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
c) vedlejší produkt živočišného původu nebo získaný produkt ze skotu, ovcí nebo koz, které byly po omráčení usmrceny lacerací centrální nervové tkáně pomocí podlouhlého tyčovitého nástroje zavedeného do dutiny lebeční nebo prostřednictvím plynové injekce do dutiny lebeční, s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE;]]]
II.7. zpracované živočišné bílkoviny nebo produkt popsaný výše:
(2) buď [neobsahují mléko nebo mléčné výrobky pocházející z ovcí nebo koz ani nejsou určeny pro krmení hospodářských zvířat jiných než kožešinových zvířat;]
(2) nebo [obsahují mléko nebo mléčné výrobky pocházející z ovcí nebo koz a jsou určeny pro krmení hospodářských zvířat jiných než kožešinových zvířat a mléko nebo mléčné výrobky:
a) jsou získány z ovcí a koz, které byly nepřetržitě od narození chovány v zemi, v níž jsou splněny tyto podmínky:
i) klasická klusavka je povinná hlášením;
ii) funguje systém osvěty, sledování a dohledu, pokud jde o klasickou klusavku;
iii) na hospodářství s chovem ovcí nebo koz se uplatňují úřední omezení v případě podezření na TSE nebo potvrzení klasické klusavky;
iv) ovce a kozy postižené klasickou klusavkou jsou usmrceny a zlikvidovány;
v) krmení ovcí a koz masokostní moučkou nebo škvarky z přežvýkavců, jak jsou definovány v Kodexu zdraví suchozemských živočichů Světové organizace pro zdraví zvířat (OIE), bylo zakázáno a zákaz byl účinně vymáhán v celé zemi přinejmenším po dobu předchozích sedmi let;
b) pocházejí z hospodářství, pro která neplatí žádné úřední omezení z důvodu podezření na výskyt TSE;
c) pocházejí z hospodářství, v nichž přinejmenším po dobu předchozích sedmi let nebyl diagnostikován žádný případ klasické klusavky, nebo po potvrzení případu klasické klusavky:
(2) buď [byly usmrceny a zlikvidovány nebo poraženy všechny ovce a kozy v hospodářství s výjimkou plemenných beranů genotypu ARR/ARR, chovných bahnic nesoucích alespoň jednu alelu ARR a žádnou alelu VRQ a dalších ovcí nesoucích alespoň jednu alelu ARR;]
(2) nebo [byla všechna zvířata, u nichž byla klasická klusavka potvrzena, usmrcena a zlikvidována a na hospodářství se alespoň po dva roky od potvrzení posledního případu klasické klusavky vztahuje intenzivnější sledování TSE, včetně vyšetření všech následujících zvířat starších 18 měsíců, s výjimkou ovcí genotypu ARR/ARR, na přítomnost TSE s negativním výsledkem v souladu s laboratorními metodami stanovenými v příloze X kapitole C bodě 3.2 nařízení (ES) č. 999/2001:
— zvířata, která byla poražena k lidské spotřebě, a
— zvířata, která uhynula nebo byla usmrcena v daném hospodářství, avšak nebyla usmrcena v rámci kampaně eradikace nákazy;]]
II.8. [zpracované živočišné bílkoviny nebo produkt popsaný výše obsahují vedlejší produkty živočišného původu z nepřežvýkavců nebo jsou z nich získány a v souladu s prohlášením odesílatele v kolonce I.1.
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) buď [nejsou určeny k výrobě krmiv pro hospodářská zvířata jiná než kožešinová zvířata.]
(2) (6) nebo [jsou určeny k výrobě krmiv pro nepřežvýkavá hospodářská zvířata jiná než kožešinová zvířata a odesílatel se zavázal zajistit, že stanovišti hraniční kontroly v místě vstupu do Evropské unie budou poskytnuty výsledky zkoušení podle metod stanovených v příloze VI nařízení Komise (ES) č.152/2009 (7).]
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit přes Evropskou unii; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
— Kolonka I.12.: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit. Produkty smí být při tranzitu skladovány pouze ve svobodných pásmech, svobodných skladech a celních skladech.
— Kolonka I.15.: Registrační číslo (železničních vagonů nebo kontejneru a nákladních automobilů), číslo letu (letadla) nebo název (plavidla); informace je třeba poskytnout v případě vykládky a opětovného naložení.
— Kolonka I.19.: Použijte příslušný kód HS: 05.11, 23.01 nebo 23.09.
— Kolonka I.25.: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26. a I.27.: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
— Kolonka I.28.: Druh: hmyz, uveďte vědecký název.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
(2) Nehodící se škrtněte.
(3) Kde:
n = počet vzorků, které mají být vyšetřeny;
m = prahová hodnota počtu bakterií; výsledek je považován za uspokojivý, jestliže počet bakterií ve všech vzorcích nepřekročí m;
M = maximální hodnota počtu bakterií; výsledek je považován za neuspokojivý, pokud počet bakterií v jednom nebo více vzorcích je roven nebo vyšší než M; a
c = počet vzorků, jejichž bakteriální počet smí být v rozmezí mezi m a M, přičemž vzorek je ještě stále považován za přípustný, pokud je bakteriální počet ostatních vzorků roven m nebo nižší.
(4) Úř. věst. L 147, 31.5.2001, s. 1.
(5) Úř. věst. L 172, 30.6.2007, s. 84.
 Text obrazu
Text obrazu
ZEMĚ
Zpracované živočišné bílkoviny získané z farmově chovaného hmyzu, které nejsou určeny k lidské spotřebě, včetně směsí a produktů jiných než krmivo pro zvířata v zájmovém chovu obsahujících tyto bílkoviny
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(6) Osoba zodpovědná za zásilku uvedená v kolonce I.6. musí zajistit, aby v případě, že zpracované živočišné bílkoviny nebo produkt popsaný v tomto veterinárním osvědčení mají být určeny k výrobě krmiva pro nepřežvýkavá hospodářská zvířata jiná než kožešinová zvířata, byla zásilka podrobena zkoušení podle metod stanovených v příloze VI nařízení (ES) č. 152/2009, aby se ověřila nepřítomnost nepovolených složek živočišného původu. Informace týkající se výsledku takového zkoušení musí být při předložení zásilky na stanovišti hraniční kontroly EU připojeny k tomuto veterinárnímu osvědčení.
(7) Úř. věst. L 54, 26.2.2009, s. 1.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro osobu zodpovědnou za zásilku v Evropské unii: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
KAPITOLA 2 (A)
Veterinární osvědčení
pro mléko, mléčné výrobky a produkty získané z mléka, které nejsou určeny k lidské spotřebě, určené k odeslání do Evropské unie nebo k tranzitu přes její území (2)
 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17. Číslo/čísla CITES
I.18. Popis zboží
I.19. Kód zboží (kód HS)
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
 Text obrazu
Text obrazu
I.25. Zboží osvědčené pro:
Krmivo Další zpracování Výroba krmiva pro zvířata v zájmovém chovu
Technické využití
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Výrobní závod
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Mléko, mléčné výrobky a produkty získané z mléka, které nejsou určeny k lidské spotřebě
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a), zejména pokud jde o článek 10 uvedeného nařízení, a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu X kapitolu II oddíl 4 a přílohu XIV kapitolu I uvedeného nařízení, a potvrzuji, že mléko (2), mléčné výrobky (2) a produkty získané z mléka (2) uvedené v kolonce I.28. splňují následující podmínky:
II.1. byly vyrobeny a získány v (vložte název vyvážejícízemě) (3), (vložte název oblasti) (3), která je uvedena v příloze II části I nařízení Komise (EU) č. 605/2010 (4) a byla 12 měsíců bezprostředně před vývozem prostá slintavky a kulhavky a moru skotu a v průběhu uvedeného období zde neproběhlo očkování proti moru skotu;
II.2. byly vyrobeny ze syrového mléka získaného ze zvířat, která v době dojení nevykazovala žádné klinické příznaky onemocnění přenosného mlékem na člověka nebo zvířata a která byla po dobu nejméně 30 dnů před výrobou držena v hospodářstvích, která nebyla předmětem úředních omezení z důvodu slintavky a kulhavky nebo moru skotu;
II.3. jedná se o mléko nebo mléčné výrobky, které:
(2) buď [byly ošetřeny jedním ze způsobů uvedených v bodě II.4. nebo jejich kombinací;]
(2) nebo [obsahují syrovátku určenou ke krmení zvířat druhů vnímavých ke slintavce a kulhavce, přičemž tato syrovátka byla odebrána z mléka, které bylo ošetřeno jedním ze způsobů popsaných v bodě II.4., a:
(2) buď [byla odebrána nejdříve 16 hodin po sražení mléka a má pH nižší než 6;]
(2) (5) nebo [byla vyrobena nejméně 21 dní před odesláním a během této doby nebyl ve vyvážející zemi zjištěn žádný případ slintavky a kulhavky;]
(2) (5) nebo [byla vyrobena dne / / , přičemž toto datum, s ohledem na předpokládanou dobu přepravy, odpovídá době nejméně 21 dní před datem, kdy je zásilka předložena na stanovišti hraniční kontroly Evropské unie;]]
II.4. byly ošetřeny jedním z následujících způsobů:
(2) buď [krátkodobou vysokoteplotní pasterizací při teplotě 72 °C trvající nejméně 15 sekund nebo ošetřením s rovnocenným pasterizačním účinkem, kterým je dosaženo negativní reakce na fosfatázový test u kravského mléka, v kombinaci s:
(2) buď [následnou další krátkodobou vysokoteplotní pasterizací při teplotě 72 °C trvající nejméně 15 sekund nebo ošetřením s rovnocenným pasterizačním účinkem, kterým je samo o sobě dosaženo negativní reakce na fosfatázový test u kravského mléka;]
(2) nebo [následným procesem sušení, v případě mléka určeného ke krmení v kombinaci s doplňkovým zahřátím alespoň na 72 °C;]
(2) nebo [následným procesem, při kterém je pH sníženo a alespoň jednu hodinu udržováno pod hranicí 6;]
(2) (5) nebo [podmínkou, že mléko / mléčný výrobek byl(o) vyroben(o) nejméně 21 dní před datem odeslání a že během této doby nebyl ve vyvážející zemi zjištěn žádný případ slintavky a kulhavky;]
(2) (5) nebo [mléko / mléčný výrobek byl(o) vyroben(o) dne …/…/…(vložte datum), přičemž toto datum, s ohledem na předpokládanou dobu přepravy, odpovídá době nejméně 21 dnů před datem, kdy je zásilka předložena na stanovišti hraniční kontroly Evropské unie;]
(2) nebo [sterilizací přinejmenším na hodnotu F03;]]
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Mléko, mléčné výrobky a produkty získané z mléka, které nejsou určeny k lidské spotřebě
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) nebo [ošetřením ultravysokou teplotou při 132 °C trvajícím nejméně jednu sekundu v kombinaci s:
(2) buď [následným procesem sušení, v případě mléka určeného ke krmení v kombinaci s doplňkovým zahřátím alespoň na 72 °C;]
(2) nebo [následným procesem, při kterém je pH sníženo a alespoň jednu hodinu udržováno pod hranicí 6;]
(2) (5) nebo [podmínkou, že mléko / mléčný výrobek byl(o) vyroben(o) nejméně 21 dní před datem odeslání a že během této doby nebyl ve vyvážející zemi zjištěn žádný případ slintavky a kulhavky;]
(2) (5) nebo [mléko / mléčný výrobek byl(o) vyroben(o) dne …/…/…(vložte datum), přičemž toto datum, s ohledem na předpokládanou dobu přepravy, odpovídá době nejméně 21 dnů před datem, kdy je zásilka předložena na stanovišti hraniční kontroly Evropské unie;]]
II.5. byla uplatněna všechna preventivní opatření k zabránění kontaminace mléka / mléčného výrobku / produktu získaného z mléka po zpracování;
II.6. mléko / mléčný výrobek / produkt získaný z mléka byl(o) zabalen(o):
(2) buď [do nových nádob;]
(2) nebo [ve vozidlech nebo kontejnerech pro volně ložené látky, které byly před nakládkou vydezinfikovány dezinfekčním prostředkem schváleným příslušným orgánem;]
a nádoby a kontejnery jsou označeny způsobem, který označuje charakter mléka / mléčného výrobku / produktu získaného z mléka, a jsou opatřeny etiketami uvádějícími, že se jedná o materiál kategorie 3, který není určen k lidské spotřebě;
II.7. výše popsané mléko, mléčné výrobky a produkty získané z mléka:
(2) buď [neobsahují mléko nebo mléčné výrobky pocházející z ovcí nebo koz ani nejsou určeny pro krmení hospodářských zvířat jiných než kožešinových zvířat.]
(2) nebo [obsahují mléko nebo mléčné výrobky pocházející z ovcí nebo koz a jsou určeny pro krmení hospodářských zvířat jiných než kožešinových zvířat a mléko nebo mléčné výrobky:
a) jsou získány z ovcí a koz, které byly nepřetržitě od narození chovány v zemi, v níž jsou splněny tyto podmínky:
i) klasická klusavka je povinná hlášením;
ii) funguje systém osvěty, sledování a dohledu, pokud jde o klasickou klusavku;
iii) na hospodářství s chovem ovcí nebo koz se uplatňují úřední omezení v případě podezření na TSE nebo potvrzení klasické klusavky;
iv) ovce a kozy postižené klasickou klusavkou jsou usmrceny a zlikvidovány;
v) krmení ovcí a koz masokostní moučkou nebo škvarky z přežvýkavců, jak jsou definovány v Kodexu zdraví suchozemských živočichů Světové organizace pro zdraví zvířat (OIE), bylo zakázáno a zákaz byl účinně vymáhán v celé zemi přinejmenším po dobu předchozích sedmi let;
b) pocházejí z hospodářství, pro která neplatí žádné úřední omezení z důvodu podezření na výskyt TSE;
 Text obrazu
Text obrazu
ZEMĚ
Mléko, mléčné výrobky a produkty získané z mléka, které nejsou určeny k lidské spotřebě
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
c) pocházejí z hospodářství, v nichž přinejmenším po dobu předchozích sedmi let nebyl diagnostikován žádný případ klasické klusavky, nebo po potvrzení případu klasické klusavky:
(2) buď [byly usmrceny a zlikvidovány nebo poraženy všechny ovce a kozy v hospodářství s výjimkou plemenných beranů genotypu ARR/ARR, chovných bahnic nesoucích alespoň jednu alelu ARR a žádnou alelu VRQ a dalších ovcí nesoucích alespoň jednu alelu ARR;]
(2) nebo [byla všechna zvířata, u nichž byla klasická klusavka potvrzena, usmrcena a zlikvidována a na hospodářství se alespoň po dva roky od potvrzení posledního případu klasické klusavky vztahuje intenzivnější sledování TSE, včetně vyšetření všech následujících zvířat starších 18 měsíců, s výjimkou ovcí genotypu ARR/ARR, na přítomnost TSE s negativním výsledkem v souladu s laboratorními metodami stanovenými v příloze X kapitole C bodě 3.2 nařízení (ES) č.999/2001 (6):
— zvířata, která byla poražena k lidské spotřebě, a
— zvířata, která uhynula nebo byla usmrcena v daném hospodářství, avšak nebyla usmrcena v rámci kampaně eradikace nákazy.]]
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit přes Evropskou unii; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
— Kolonka I.12.: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit.
— Kolonka I.15.: Je třeba uvést registrační číslo (vagony nebo kontejnery a nákladní automobily), číslo letu (letadlo) nebo název (plavidlo). V případě vykládky a opětovného naložení musí odesílatel informovat stanoviště hraniční kontroly Evropské unie.
— Kolonka I.19.: použijte příslušný kód harmonizovaného systému (HS) Světové celní organizace: 04.01, 04.02, 04.03, 04.04, 23.09.10, 23.09.90, 35.01, 35.02 nebo 35.04.
— Kolonka I.23.: V případě kontejnerů pro volně ložené látky musí být uvedeno číslo kontejneru a (případně) číslo plomby.
— Kolonka I.25.: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26. a I.27.: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
— Kolonka I.28.: Výrobní závod: vyplňte číslo registrace zařízení, v němž proběhlo ošetření nebo zpracování.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
 Text obrazu
Text obrazu
ZEMĚ
Mléko, mléčné výrobky a produkty získané z mléka, které nejsou určeny k lidské spotřebě
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) Nehodící se škrtněte.
(3) Vyplňte, pokud je oprávnění k dovozu do Evropské unie nebo k tranzitu přes Evropskou unii omezeno na určité regiony dotčené třetí země.
(4) Úř. věst. L 175, 10.7.2010, s. 1.
(5) Tato podmínka platí pouze pro třetí země uvedené v příloze I sloupci A nařízení (EU) č. 605/2010.
(6) Úř. věst. L 147, 31.5.2001, s. 1.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro osobu zodpovědnou za zásilku v Evropské unii: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
KAPITOLA 2 (B)
Veterinární osvědčení
pro mlezivo a výrobky z mleziva skotu, které nejsou určeny k lidské spotřebě, určené k odeslání do Evropské unie nebo k tranzitu přes její území (2)
 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17. Číslo/čísla CITES
I.18. Popis zboží
I.19. Kód zboží (kód HS)
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
 Text obrazu
Text obrazu
I.25. Zboží osvědčené pro:
Krmivo Další zpracování Výroba krmiva pro zvířata v zájmovém chovu
Technické využití
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Výrobní závod
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Mlezivo a výrobky z mleziva skotu, které nejsou určeny k lidské spotřebě
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a), zejména pokud jde o článek 10 uvedeného nařízení, a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu X kapitolu II oddíl 4 a přílohu XIV kapitolu I uvedeného nařízení, a potvrzuji, že mlezivo (2) nebo výrobky z mleziva (2) uvedené v kolonce I.28. splňují následující podmínky:
II.1. byly vyrobeny a získány v (vložte název vyvážející země) (3), (vložte název oblasti) (3), která je uvedena v příloze I nařízení Komise (EU) č. 605/2010 (4) a byla 12 měsíců bezprostředně před vývozem prostá slintavky a kulhavky a moru skotu a v průběhu uvedeného období zde neproběhlo očkování proti moru skotu;
II.2. byly vyrobeny z mleziva získaného ze zvířat, která v době dojení nevykazovala žádné klinické příznaky onemocnění přenosného mlezivem na člověka nebo zvířata a která byla po dobu nejméně 30 dnů před datem výroby držena v hospodářstvích, která nebyla předmětem úředních omezení z důvodu slintavky a kulhavky nebo moru skotu;
II.3. jedná se o mlezivo nebo výrobky z mleziva skotu, které prošly krátkodobou vysokoteplotní pasterizací při teplotě 72 °C trvající nejméně 15 sekund nebo ošetřením s rovnocenným pasterizačním účinkem, kterým je dosaženo negativní reakce na fosfatázový test u mleziva skotu, v kombinaci s:
(2) (5) buď [podmínkou, že mlezivo nebo výrobky z mleziva byly vyrobeny během doby nejméně 21 dní před datem odeslání a že během této doby nebyl ve vyvážející zemi zjištěn žádný případ slintavky a kulhavky; ]
(2) (5) nebo [podmínkou, že mlezivo nebo výrobky z mleziva byly vyrobeny dne …/ /…(vložte datum), přičemž toto datum, s ohledem na předpokládanou dobu přepravy, odpovídá době nejméně 21 dní před datem, kdy je zásilka předložena na stanovišti hraniční kontroly Evropské unie;]
a byly získány od zvířat, u nichž se provádějí pravidelné veterinární kontroly, aby bylo zajištěno, že pocházejí z hospodářství, v nichž jsou všechna stáda skotu:
(2) (5) buď [uznána za úředně prostá tuberkulózy a brucelózy (6);]
(2) (5) nebo [nepodléhající podle vnitrostátních právních přepisů třetí země původu omezením v souvislosti s eradikací tuberkulózy a brucelózy;]
a (2) (5) buď [uznána za úředně prostá enzootické leukózy skotu (6);]
(2) (5) nebo [zahrnuta do úředního systému pro tlumení enzootické leukózy skotu a během doby předchozích dvou let u nich klinická a laboratorní vyšetření neprokázala výskyt této nákazy;]]
II.4. byla uplatněna všechna preventivní opatření k zabránění kontaminace mleziva / výrobku z mleziva po zpracování;
II.5. mlezivo / výrobek z mleziva byl(o) zabalen(o):
(2) buď [do nových nádob,]
(2) nebo [ve vozidlech nebo kontejnerech pro volně ložené látky, které byly před nakládkou vydezinfikovány dezinfekčním prostředkem schváleným příslušným orgánem]
a nádoby a kontejnery jsou označeny způsobem, který označuje charakter mleziva / výrobku z mleziva, a jsou opatřeny etiketami uvádějícími, že se jedná o materiál kategorie 3, který není určen k lidské spotřebě;
II.6. mlezivo nebo výrobek z mleziva neobsahuje mléko nebo mléčné výrobky pocházející z ovcí nebo koz.
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit přes Evropskou unii; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Mlezivo a výrobky z mleziva skotu, které nejsou určeny k lidské spotřebě
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
— Kolonka I.12.: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit.
— Kolonka I.15.: Je třeba uvést registrační číslo (vagony nebo kontejnery a nákladní automobily), číslo letu (letadlo) nebo název (plavidlo). V případě vykládky a opětovného naložení v Evropské unii musí odesílatel informovat stanoviště hraniční kontroly Evropské unie.
— Kolonka I.19.: použijte příslušný kód harmonizovaného systému (HS) Světové celní organizace: 04.04.90, 23.09.10, 23.09.90, 35.01, 35.02 nebo 35.04.
— Kolonka I.23.: V případě kontejnerů pro volně ložené látky musí být uvedeno číslo kontejneru a (případně) číslo plomby.
— Kolonka I.25.: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26. a I.27.: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
— Kolonka I.28.: Výrobní závod: vyplňte číslo registrace zařízení, v němž proběhlo ošetření nebo zpracování.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
(2) Nehodící se škrtněte.
(3) Vyplňte, pokud je oprávnění k dovozu do Evropské unie omezeno na určité regiony dotčené třetí země.
(4) Úř. věst. L 175, 10.7.2010, s. 1.
(5) Tato podmínka platí pouze pro třetí země uvedené v příloze I sloupci A nařízení Komise (EU) č. 605/2010 (Úř. věst. L 175, 10.7.2010, s. 1).
(6) Stádo úředně prosté tuberkulózy a brucelózy podle vymezení v příloze A směrnice Rady 64/432/EHS (Úř. věst. 121, 29.7.1964, s. 1977) a stádo úředně prosté enzootické leukózy skotu podle vymezení v příloze D kapitole I uvedené směrnice.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro dovozce: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly Evropské unie.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
KAPITOLA 3 (A)
Veterinární osvědčení
pro krmivo v konzervách pro zvířata v zájmovém chovu určené k odeslání do Evropské unie nebo k tranzitu přes její území (2)
 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17.
I.18. Popis zboží
I.19. Kód zboží (kód HS)
23.09
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
 Text obrazu
Text obrazu
I.25. Zboží osvědčené pro:
Krmivo pro zvířata v zájmovém chovu Technické využití
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Výrobní závod
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Krmivo v konzervách pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a), zejména pokud jde o články 8 a 10 uvedeného nařízení, a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu XIII kapitolu II a přílohu XIV kapitolu II uvedeného nařízení, a potvrzuji, že výše popsané krmivo pro zvířata v zájmovém chovu:
II.1. bylo připraveno a skladováno v zařízení nebo podniku schváleném a dozorovaném příslušným orgánem v souladu s článkem 24 nařízení (ES) č. 1069/2009;
II.2. bylo připraveno výhradně z těchto vedlejších produktů živočišného původu:
(2) buď [- těla poražených zvířat a jejich části, nebo v případě zvěře těla usmrcených zvířat nebo jejich části, které jsou podle právních předpisů Unie vhodné k lidské spotřebě, avšak z obchodních důvodů nejsou k lidské spotřebě určeny;]
(2) a/nebo [- jatečně upravená těla a níže uvedené části pocházející buď ze zvířat, která byla poražena na jatkách a po prohlídce před porážkou byla shledána jako způsobilá k porážce k lidské spotřebě, nebo těla a níže uvedené části zvěře usmrcené k lidské spotřebě v souladu s právními předpisy Unie:
i) jatečně upravená těla nebo těla zvířat a jejich části, které byly v souladu s právními předpisy Unie prohlášeny za nevhodné k lidské spotřebě, avšak nevykazovaly žádné příznaky onemocnění přenosného na člověka nebo zvířata;
ii) hlavy drůbeže;
iii) kůže a kožky, včetně jejich odřezků a plátků, rohy a končetiny, včetně článků prstů, zápěstních a záprstních kůstek, nártů a zánártí;
iv) prasečí štětiny;
v) peří;]
(2) a/nebo [- vedlejší produkty živočišného původu z drůbeže a ze zajícovců poražených na farmě, jak je uvedeno v čl. 1 odst. 3 písm. d) nařízení Evropského parlamentu a Rady (ES) č. 853/2004 (2a), kteří nevykazovali příznaky onemocnění přenosného na člověka nebo zvířata;]
(2) a/nebo [- krev zvířat, která nevykazovala žádné příznaky onemocnění přenosného krví na člověka nebo zvířata, která byla poražena na jatkách a která byla po prohlídce před porážkou shledána způsobilými k porážce k lidské spotřebě v souladu s právními předpisy Unie;]
(2) a/nebo [- vedlejší produkty živočišného původu, které vznikají při výrobě produktů určených k lidské spotřebě, včetně odtučněných kostí, škvarků nebo kalu z odstředivky nebo separátoru ze zpracování mléka;]
(2) a/nebo [- produkty živočišného původu nebo potraviny obsahující produkty živočišného původu, které z obchodních důvodů nebo z důvodů problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny k lidské spotřebě;]
(2) a/nebo [- krmivo pro zvířata v zájmovém chovu a krmivo živočišného původu nebo krmivo obsahující vedlejší produkty živočišného původu či získané produkty, které z obchodních důvodů nebo z důvodu problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny ke krmení;]
(2) a/nebo [- krev, placenta, vlna, peří, srst, rohy, odřezky kopyt a paznehtů a syrové mléko pocházející ze živých zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto produktem na člověka nebo zvířata;]
(2) a/nebo [- vodní živočichové a jejich části, kromě mořských savců, kteří nevykazovali žádné příznaky onemocnění přenosných na člověka nebo zvířata;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních živočichů pocházející z podniků nebo zařízení na výrobu produktů určených k lidské spotřebě;]
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Krmivo v konzervách pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) a/nebo [- níže uvedený materiál pocházející ze zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto materiálem na člověka nebo zvířata:
i) ulity měkkýšů a korýšů s měkkými tkáněmi nebo masem;
ii) tento materiál pocházející ze suchozemských zvířat:
— vedlejší produkty z líhní,
— vejce,
— vedlejší produkty z vajec, včetně vaječných skořápek;
iii) jednodenní kuřata usmrcená z obchodních důvodů;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních nebo suchozemských bezobratlých živočichů, kromě druhů patogenních pro člověka nebo zvířata;]
(2) a/nebo [- zvířata z řádů hlodavců (Rodentia) a zajícovců (Lagomorpha) a jejich části, kromě materiálu kategorie 1 uvedeného v čl. 8 písm. a) bodech iii), iv) a v) nařízení (ES) č. 1069/2009 a materiálu kategorie 2 uvedeného v čl. 9 písm. a) až g) uvedeného nařízení;]
(2) a/nebo [- materiál ze zvířat, která byla ošetřena některými látkami zakázanými podle směrnice Rady 96/22/ES (2b), přičemž dovoz tohoto materiálu byl povolen v souladu s čl. 35 písm. a) bodem ii) nařízení (ES) č. 1069/2009;]
II.3. bylo podrobeno tepelnému ošetření, při kterém je dosaženo hodnoty Fc rovné minimálně 3, v hermeticky uzavřených nádobách;
II.4. bylo analyzováno pomocí alespoň pěti namátkou odebraných vzorků z každé zpracované šarže laboratorní diagnostickou metodou tak, aby se ověřilo, zda bylo provedeno odpovídající tepelné ošetření celé zásilky, jak stanoví bod II.3.;
II.5. prošlo všemi preventivními opatřeními k zabránění kontaminace patogenními původci po ošetření;
(2) [II.6. výše popsané krmivo pro zvířata v zájmovém chovu
(2) buď [je získáno z přežvýkavců jiných než skot, ovce nebo kozy.]
(2) nebo [je získáno ze skotu, ovcí nebo koz a neobsahuje dále uvedené složky ani z nich nebylo získáno:
(2) buď [materiál pocházející ze skotu, ovcí a koz jiný než získaný ze zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]
(2) nebo [a) specifikovaný rizikový materiál, jak je definován v bodě 1 přílohy V nařízení Evropského parlamentu a Rady (ES) č. 999/2001 (3);
b) strojně oddělené maso získané z kostí skotu, ovcí nebo koz s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím Komise 2007/453/ES (4) do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE;
c) vedlejší produkt živočišného původu nebo získaný produkt ze skotu, ovcí nebo koz, které byly po omráčení usmrceny lacerací centrální nervové tkáně pomocí podlouhlého tyčovitého nástroje zavedeného do dutiny lebeční nebo prostřednictvím plynové injekce do dutiny lebeční, s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]]
 Text obrazu
Text obrazu
ZEMĚ
Krmivo v konzervách pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit přes Evropskou unii; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
— Kolonka I.12.: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit. Produkty smí být při tranzitu skladovány pouze ve svobodných pásmech, svobodných skladech a celních skladech.
— Kolonka I.15.: Registrační číslo (železničních vagonů nebo kontejneru a nákladních automobilů), číslo letu (letadla) nebo název (plavidla); informace je třeba poskytnout v případě vykládky a opětovného naložení v Evropské unii.
— Kolonka I.23.: V případě kontejnerů pro volně ložené látky musí být uvedeno číslo kontejneru a (případně) číslo plomby.
— Kolonka I.25.: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26. a I.27.: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
— Kolonka I.28.: Druh: vyberte: Aves, Ruminantia, Suidae, Mammalia kromě Ruminantia nebo Suidae, Pesca, Mollusca, Crustacea, bezobratlí kromě Mollusca a Crustacea.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
(2) Nehodící se škrtněte.
(2a) Úř. věst. L 139, 30.4.2004, s. 55.
(2b) Úř. věst. L 125, 23.5.1996, s. 3.
(3) Úř. věst. L 147, 31.5.2001, s. 1.
(4) Úř. věst. L 172, 30.6.2007, s. 84.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro osobu zodpovědnou za zásilku v Evropské unii: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
KAPITOLA 3 (B)
Veterinární osvědčení
pro zpracované krmivo pro zvířata v zájmovém chovu jiné než v konzervách určené k odeslání do Evropské unie nebo k tranzitu přes její území (2)
 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17.
I.18. Popis zboží
I.19. Kód zboží (kód HS)
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
 Text obrazu
Text obrazu
I.25. Zboží osvědčené pro:
Krmivo pro zvířata v zájmovém chovu Technické využití
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Výrobní závod
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Zpracované krmivo pro zvířata v zájmovém chovu jiné než v konzervách
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a), zejména pokud jde o články 8 a 10 uvedeného nařízení, a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu XIII kapitolu II a přílohu XIV kapitolu II uvedeného nařízení, a potvrzuji, že výše popsané krmivo pro zvířata v zájmovém chovu:
II.1. bylo připraveno a skladováno v podniku schváleném a dozorovaném příslušným orgánem v souladu s článkem 24 nařízení (ES) č. 1069/2009;
II.2. bylo připraveno výhradně z těchto vedlejších produktů živočišného původu:
(2) buď [- těla poražených zvířat a jejich části, nebo v případě zvěře těla usmrcených zvířat nebo jejich části, které jsou podle právních předpisů Unie vhodné k lidské spotřebě, avšak z obchodních důvodů nejsou k lidské spotřebě určeny;]
(2) a/nebo [- jatečně upravená těla a níže uvedené části pocházející buď ze zvířat, která byla poražena na jatkách a po prohlídce před porážkou byla shledána jako způsobilá k porážce k lidské spotřebě, nebo těla a níže uvedené části zvěře usmrcené k lidské spotřebě v souladu s právními předpisy Unie:
i) jatečně upravená těla nebo těla zvířat a jejich části, které byly v souladu s právními předpisy Unie prohlášeny za nevhodné k lidské spotřebě, avšak nevykazovaly žádné příznaky onemocnění přenosného na člověka nebo zvířata;
ii) hlavy drůbeže;
iii) kůže a kožky, včetně jejich odřezků a plátků, rohy a končetiny, včetně článků prstů, zápěstních a záprstních kůstek, nártů a zánártí;
iv) prasečí štětiny;
v) peří;]
(2) a/nebo [- vedlejší produkty živočišného původu z drůbeže a ze zajícovců poražených na farmě, jak je uvedeno v čl. 1 odst. 3 písm. d) nařízení Evropského parlamentu a Rady (ES) č. 853/2004 (2a), kteří nevykazovali příznaky onemocnění přenosného na člověka nebo zvířata;]
(2) a/nebo [- krev zvířat, která nevykazovala žádné příznaky onemocnění přenosného krví na člověka nebo zvířata, která byla poražena na jatkách a která byla po prohlídce před porážkou shledána způsobilými k porážce k lidské spotřebě v souladu s právními předpisy Unie;]
(2) a/nebo [- vedlejší produkty živočišného původu, které vznikají při výrobě produktů určených k lidské spotřebě, včetně odtučněných kostí, škvarků nebo kalu z odstředivky nebo separátoru ze zpracování mléka;]
(2) a/nebo [- produkty živočišného původu nebo potraviny obsahující produkty živočišného původu, které z obchodních důvodů nebo z důvodů problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny k lidské spotřebě;]
(2) a/nebo [- krmivo pro zvířata v zájmovém chovu a krmivo živočišného původu nebo krmivo obsahující vedlejší produkty živočišného původu či získané produkty, které z obchodních důvodů nebo z důvodu problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny ke krmení;]
(2) a/nebo [- krev, placenta, vlna, peří, srst, rohy, odřezky kopyt a paznehtů a syrové mléko pocházející ze živých zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto produktem na člověka nebo zvířata;]
(2) a/nebo [- vodní živočichové a jejich části, kromě mořských savců, kteří nevykazovali žádné příznaky onemocnění přenosných na člověka nebo zvířata;]
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Zpracované krmivo pro zvířata v zájmovém chovu jiné než v konzervách
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) a/nebo [- vedlejší produkty živočišného původu z vodních živočichů pocházející z podniků nebo zařízení na výrobu produktů určených k lidské spotřebě;]
(2) a/nebo [- níže uvedený materiál pocházející ze zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto materiálem na člověka nebo zvířata:
i) ulity měkkýšů a korýšů s měkkými tkáněmi nebo masem;
ii) tento materiál pocházející ze suchozemských zvířat:
— vedlejší produkty z líhní,
— vejce,
— vedlejší produkty z vajec, včetně vaječných skořápek;
iii) jednodenní kuřata usmrcená z obchodních důvodů;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních nebo suchozemských bezobratlých živočichů, kromě druhů patogenních pro člověka nebo zvířata;]
(2) a/nebo [- zvířata z řádů hlodavců (Rodentia) a zajícovců (Lagomorpha) a jejich části, kromě materiálu kategorie 1 uvedeného v čl. 8 písm. a) bodech iii), iv) a v) nařízení (ES) č. 1069/2009 a materiálu kategorie 2 uvedeného v čl. 9 písm. a) až g) uvedeného nařízení;]
(2) a/nebo [- materiál ze zvířat, která byla ošetřena některými látkami zakázanými podle směrnice Rady 96/22/ES (2b), přičemž dovoz tohoto materiálu byl povolen v souladu s čl. 35 písm. a) bodem ii) nařízení (ES) č. 1069/2009;]
II.3.
(2) buď [bylo podrobeno tepelnému ošetření dosahujícímu alespoň 90 °C v celé hmotě;]
(2) nebo [bylo vyrobeno, pokud jde o složky živočišného původu, výhradně za použití produktů, které:
a) v případě vedlejších produktů živočišného původu nebo produktů získaných z masa nebo masných výrobků byly podrobeny tepelnému ošetření při teplotě alespoň 90 °C v celé hmotě;
b) v případě mléka a mléčných výrobků,
i) pokud pocházejí ze třetích zemí nebo částí třetích zemí uvedených v příloze I sloupci B nařízení Komise (EU) č. 605/2010 (3), prošly pasterizačním ošetřením dostatečným k dosažení negativního fosfatázového testu;
ii) s pH sníženým na méně než 6, pokud pocházejí ze třetích zemí nebo částí třetích zemí uvedených v příloze I sloupci C nařízení (EU) č. 605/2010, prošly nejprve pasterizačním ošetřením dostatečným k dosažení negativního fosfatázového testu;
iii) pokud pocházejí ze třetích zemí nebo částí třetích zemí uvedených v příloze I sloupci C nařízení (EU) č. 605/2010, prošly sterilizačním procesem nebo dvojím tepelným ošetřením, přičemž každé z těchto ošetření bylo samo o sobě dostatečné k dosažení negativního fosfatázového testu;
iv) pokud pocházejí ze třetích zemí nebo částí třetích zemí uvedených v příloze I sloupci C nařízení (EU) č. 605/2010, ve kterých se v předchozích 12 měsících vyskytlo ohnisko slintavky a kulhavky, nebo kde v předchozích 12 měsících proběhlo očkování proti slintavce a kulhavce, byly podrobeny:
buď
— sterilizačnímu procesu, při kterém je dosaženo hodnoty Fc rovné nebo vyšší než 3,
nebo
— počátečnímu tepelnému ošetření s tepelným účinkem alespoň rovnocenným účinku dosaženému pasterizačním procesem o teplotě alespoň 72 °C po dobu nejméně 15 sekund a dostatečným k dosažení negativní reakce na fosfatázový test, následovaným:
 Text obrazu
Text obrazu
ZEMĚ
Zpracované krmivo pro zvířata v zájmovém chovu jiné než v konzervách
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
buď
— druhým tepelným ošetřením s tepelným účinkem alespoň rovnocenným účinku počátečního tepelného ošetření a dostatečným k dosažení negativní reakce na fosfatázový test, následovaným v případě sušeného mléka nebo sušených mléčných výrobků procesem sušení,
nebo
— acidifikačním procesem, při kterém bylo pH udržováno na hodnotě nižší než 6 po dobu nejméně jedné hodiny;
c) v případě želatiny byly vyrobeny postupem, který zajišťuje, že nezpracovaný materiál kategorie 3 je podroben ošetření kyselinou či zásadou následovanému jedním nebo několikerým propláchnutím, dále úpravou pH a extrakcí zahřátím (podle potřeby opakovaně), po níž následuje pročištění prostřednictvím filtrace a sterilizace;
d) v případě hydrolyzovaných bílkovin byly vyrobeny výrobním postupem, který zahrnuje vhodná opatření k co největšímu omezení kontaminace surového materiálu kategorie 3, a v případě hydrolyzovaných bílkovin zcela nebo zčásti získaných z kůží a kožek přežvýkavců byly vyrobeny ve zpracovatelském zařízení určeném výhradně k výrobě hydrolyzovaných bílkovin, výhradně za použití materiálu, jehož molekulární hmotnost je nižší než 10 000 daltonů, a za použití postupu zahrnujícího přípravu surového materiálu kategorie 3 nakládáním do solného láku, loužením a intenzivním praním, po němž následuje:
i) vystavení materiálu pH o hodnotě vyšší než 11 po dobu delší než tři hodiny při teplotě vyšší než 80 °C a následně tepelné ošetření při teplotě vyšší než 140 °C po dobu 30 minut při tlaku vyšším než 3,6 baru; nebo
ii) vystavení materiálu pH v rozmezí hodnot 1 až 2 následované vystavením pH o hodnotě vyšší než 11 a následně tepelné ošetření při teplotě 140 °C po dobu 30 minut při tlaku 3 bary;
e) v případě vaječných výrobků byly podrobeny jakékoli ze zpracovatelských metod 1 až 5 nebo 7 uvedených v příloze IV kapitole III nařízení (EU) č. 142/2011, nebo byly ošetřeny v souladu s kapitolou II oddílu X přílohy III nařízení (ES) č. 853/2004;
f) v případě kolagenu byly podrobeny postupu, který zajišťuje, že nezpracovaný materiál kategorie 3 je podroben ošetření, které zahrnuje promytí, úpravu pH pomocí kyseliny či zásady s následným jedním či několikerým propláchnutím, filtrací a extruzí, přičemž se zakazuje používání konzervačních prostředků jiných než prostředků povolených právními předpisy Unie;
g) v případě krevních výrobků byly podrobeny jakékoli ze zpracovatelských metod 1 až 5 nebo 7 uvedených v příloze IV kapitole III nařízení (EU) č. 142/2011;
h) v případě zpracovaných živočišných bílkovin pocházejících ze savců byly podrobeny jakékoli ze zpracovatelských metod 1 až 5 nebo 7, a v případě prasečí krve byly podrobeny jakékoli ze zpracovatelských metod 1 až 5 nebo 7, pokud se v případě zpracovatelské metody 7 použilo na celou hmotu tepelné ošetření při minimální teplotě 80 °C;
i) v případě zpracovaných živočišných bílkovin nepocházejících ze savců s výjimkou rybí moučky byly podrobeny jakékoli ze zpracovatelských metod 1 až 5 nebo 7 uvedených v příloze IV kapitole III nařízení (EU) č. 142/2011;
j) v případě rybí moučky byly podrobeny jakékoli ze zpracovatelských metod 1 až 7 uvedených v příloze IV kapitole III nařízení (EU) č. 142/2011 nebo metodě a parametrům, které zajišťují soulad výrobku s mikrobiologickými normami pro získané produkty stanovenými v příloze X kapitole I nařízení (EU) č. 142/2011;
k) v případě taveného/škvařeného tuku, včetně rybího tuku, byly podrobeny některé ze zpracovatelských metod 1 až 5 nebo 7 (a metodě 6 v případě rybího tuku) uvedených v příloze IV kapitole III nařízení (EU) č. 142/2011, nebo byly vyrobeny v souladu s přílohou III oddílem XII kapitolou II nařízení (ES) č. 853/2004; tavené/škvařené tuky z přežvýkavců musí být pročištěny tak, aby maximální úroveň zbývajících nerozpustných nečistot nepřesahovala 0,15 % hmotnostních;
 Text obrazu
Text obrazu
ZEMĚ
Zpracované krmivo pro zvířata v zájmovém chovu jiné než v konzervách
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
l) v případě hydrogenfosforečnanu vápenatého byly vyrobeny postupem, jenž
i) zajišťuje, že všechen kostní materiál kategorie 3 je najemno nadrcen a pomocí horké vody odtučněn a ošetřen zředěnou kyselinou chlorovodíkovou (při minimální koncentraci 4 % a pH nižším než 1,5) po dobu alespoň dvou dnů;
ii) po skončení postupu uvedeného v bodě i) pokračuje ošetřením získaného fosforečného výluhu vápnem, což vede k získání výsledné sraženiny hydrogenfosforečnanu vápenatého při pH 4 až 7; a
iii) tuto sraženinu hydrogenfosforečnanu vápenatého nakonec vysuší vzduchem při vstupní teplotě v rozmezí od 65 °C do 325 °C a konečné teplotě v rozmezí od 30 °C do 65 °C;
m) v případě fosforečnanu vápenatého byly vyrobeny postupem, jenž zajišťuje
i) že všechen kostní materiál kategorie 3 je najemno nadrcen a pomocí protiproudu horké vody odtučněn (úlomky kostí menší než 14 mm);
ii) nepřetržité vaření v páře při teplotě 145 °C po dobu 30 minut při tlaku 4 bary;
iii) že vývar z bílkovin se odstředěním oddělí od hydroxyapatitu (fosforečnanu vápenatého); a
iv) že ke granulaci fosforečnanu vápenatého dojde po sušení ve fluidní vrstvě vzduchem o teplotě 200 °C;
n) v případě dochucovacích masových výtažků byly vyrobeny podle zpracovatelské metody a parametrů, které zajišťují soulad výrobku s mikrobiologickými normami uvedenými v bodě II.4.;]
(2) nebo [bylo podrobeno ošetření sušením nebo kvašením, které bylo schváleno příslušným orgánem;]
(2) nebo [v případě vodních a suchozemských bezobratlých živočichů, kromě druhů patogenních pro člověka nebo zvířata, bylo podrobeno ošetření, které bylo schváleno příslušným orgánem a které zajišťuje, že toto krmivo pro zvířata v zájmovém chovu nepředstavuje žádné nepřípustné riziko pro zdraví lidí a zvířat;]
II.4. bylo analyzováno pomocí alespoň pěti vzorků z každé zpracované šarže namátkově odebraných během skladování nebo při vyskladnění ve zpracovatelském zařízení a vyhovuje těmto normám (4):
Salmonella: nepřítomnost v 25 g produktu: n = 5, c = 0, m = 0, M = 0
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 300 v 1 g;
II.5. prošlo všemi preventivními opatřeními k zabránění kontaminace patogenními původci po ošetření;
II.6. bylo zabaleno do nového obalu opatřeného etiketami s nápisem „NENÍ URČENO K LIDSKÉ SPOTŘEBĚ“, není-li krmivo pro zvířata v zájmovém chovu odesíláno v balení připraveném k prodeji, na němž je jasně uvedeno, že obsah je určen výhradně ke krmení zvířat v zájmovém chovu;
(2) [II.7. výše popsané krmivo pro zvířata v zájmovém chovu
(2) buď [je získáno z přežvýkavců jiných než skot, ovce nebo kozy.]
(2) nebo [je získáno ze skotu, ovcí nebo koz a neobsahuje dále uvedené složky ani z nich nebylo získáno:
(2) buď [materiál pocházející ze skotu, ovcí a koz jiný než získaný ze zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]
(2) nebo [a) specifikovaný rizikový materiál, jak je definován v bodě 1 přílohy V nařízení Evropského parlamentu a Rady (ES) č. 999/2001 (5);
 Text obrazu
Text obrazu
ZEMĚ
Zpracované krmivo pro zvířata v zájmovém chovu jiné než v konzervách
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
b) strojně oddělené maso získané z kostí skotu, ovcí nebo koz s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím Komise 2007/453/ES (6) do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE;
c) vedlejší produkt živočišného původu nebo získaný produkt ze skotu, ovcí nebo koz, které byly po omráčení usmrceny lacerací centrální nervové tkáně pomocí podlouhlého tyčovitého nástroje zavedeného do dutiny lebeční nebo prostřednictvím plynové injekce do dutiny lebeční, s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]]
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit přes Evropskou unii; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
— Kolonka I.12.: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit. Produkty smí být při tranzitu skladovány pouze ve svobodných pásmech, svobodných skladech a celních skladech.
— Kolonka I.15.: Je třeba uvést registrační číslo (vagony nebo kontejnery a nákladní automobily), číslo letu (letadlo) nebo název (plavidlo). V případě vykládky a opětovného naložení musí odesílatel informovat stanoviště hraniční kontroly v místě vstupu do Evropské unie.
— Kolonka I.19.: Použijte příslušný kód harmonizovaného systému (HS) následujících čísel: 04.01, 04.02, 04.03, 04.04, 04.08, 05.04, 05.05, 05.06, 05.11, 15.01, 15.02, 15.03, 15.04, 23.01, 23.09, 28.35.25, 28.35.26, 35.01, 35.02, 35.03 nebo 35.04.
— Kolonka I.23.: V případě kontejnerů pro volně ložené látky musí být uvedeno číslo kontejneru a (případně) číslo plomby.
— Kolonka I.25.: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26. a I.27.: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
— Kolonka I.28.: Druh: vyberte: Aves, Ruminantia, Suidae, Mammalia kromě Ruminantia nebo Suidae, Pesca, Mollusca, Crustacea, bezobratlí kromě Mollusca a Crustacea.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
(2) Nehodící se škrtněte.
(2a) Úř. věst. L 139, 30.4.2004, s. 55.
(2b) Úř. věst. L 125, 23.5.1996, s. 3.
(3) Úř. věst. L 175, 10.7.2010, s. 1.
 Text obrazu
Text obrazu
ZEMĚ
Zpracované krmivo pro zvířata v zájmovém chovu jiné než v konzervách
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(4) Kde:
n = počet vzorků, které mají být vyšetřeny;
m = prahová hodnota počtu bakterií; výsledek je považován za uspokojivý, jestliže počet bakterií ve všech vzorcích nepřekročí m;
M = maximální hodnota počtu bakterií; výsledek je považován za neuspokojivý, pokud počet bakterií v jednom nebo více vzorcích je roven nebo vyšší než M; a
c = počet vzorků, jejichž bakteriální počet smí být v rozmezí mezi m a M, přičemž vzorek je ještě stále považován za přípustný, pokud je bakteriální počet ostatních vzorků roven m nebo nižší.
(5) Úř. věst. L 147, 31.5.2001, s. 1.
(6) Úř. věst. L 172, 30.6.2007, s. 84.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro osobu zodpovědnou za zásilku v Evropské unii: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly v místě vstupu do Evropské unie.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
KAPITOLA 3 (C)
Veterinární osvědčení
pro žvýkací pamlsky pro psy, které jsou určeny k odeslání do Evropské unie nebo k tranzitu přes její území (2)
 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17.
I.18. Popis zboží
I.19. Kód zboží (kód HS)
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
 Text obrazu
Text obrazu
I.25. Zboží osvědčené pro:
Krmivo pro zvířata v zájmovém chovu Technické využití
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Výrobní závod
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Žvýkací pamlsky pro psy
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a), zejména pokud jde o článek 10 uvedeného nařízení, a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu XIII kapitolu II a přílohu XIV kapitolu II uvedeného nařízení, a potvrzuji, že výše popsané žvýkací pamlsky pro psy:
II.1. byly připraveny výhradně z těchto vedlejších produktů živočišného původu:
(2) buď [- těla poražených zvířat a jejich části, nebo v případě zvěře těla usmrcených zvířat nebo jejich části, které jsou podle právních předpisů Unie vhodné k lidské spotřebě, avšak z obchodních důvodů nejsou k lidské spotřebě určeny;]
(2) a/nebo [- jatečně upravená těla a níže uvedené části pocházející buď ze zvířat, která byla poražena na jatkách a po prohlídce před porážkou byla shledána jako způsobilá k porážce k lidské spotřebě, nebo těla a níže uvedené části zvěře usmrcené k lidské spotřebě v souladu s právními předpisy Unie:
i) jatečně upravená těla nebo těla zvířat a jejich části, které byly v souladu s právními předpisy Unie prohlášeny za nevhodné k lidské spotřebě, avšak nevykazovaly žádné příznaky onemocnění přenosného na člověka nebo zvířata;
ii) hlavy drůbeže;
iii) kůže a kožky, včetně jejich odřezků a plátků, rohy a končetiny, včetně článků prstů, zápěstních a záprstních kůstek, nártů a zánártí;
iv) prasečí štětiny;
v) peří;]
(2) a/nebo [- krev zvířat, která nevykazovala žádné příznaky onemocnění přenosného krví na člověka nebo zvířata, která byla poražena na jatkách a která byla po prohlídce před porážkou shledána způsobilými k porážce k lidské spotřebě v souladu s právními předpisy Unie;]
(2) a/nebo [- vedlejší produkty živočišného původu, které vznikají při výrobě produktů určených k lidské spotřebě, včetně odtučněných kostí, škvarků nebo kalu z odstředivky nebo separátoru ze zpracování mléka;]
(2) a/nebo [- vodní živočichové a jejich části, kromě mořských savců, kteří nevykazovali žádné příznaky onemocnění přenosných na člověka nebo zvířata;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních živočichů pocházející z podniků nebo zařízení na výrobu produktů určených k lidské spotřebě;]
(2) a/nebo [- materiál ze zvířat, která byla ošetřena některými látkami zakázanými podle směrnice Rady 96/22/ES (2b), přičemž dovoz tohoto materiálu byl povolen v souladu s čl. 35 písm. a) bodem ii) nařízení (ES) č. 1069/2009;]
II.2. byly podrobeny
(2) buď [v případě žvýkacích pamlsků pro psy vyrobených z kůží a kožek kopytníků nebo z ryb ošetření dostatečnému ke zničení patogenních původců (včetně salmonel); a žvýkací pamlsky pro psy jsou vysušené;]
(2) a/nebo [v případě žvýkacích pamlsků pro psy vyrobených z vedlejších produktů živočišného původu jiných než kůží a kožek kopytníků a ryb tepelnému ošetření při teplotě minimálně 90 °C v celé hmotě;]
II.3. byly analyzovány pomocí alespoň pěti vzorků z každé zpracované šarže namátkově odebraných během skladování nebo při vyskladnění ve zpracovatelském zařízení a vyhovují těmto normám (3):
Salmonella: nepřítomnost v 25 g produktu: n = 5, c = 0, m = 0, M = 0
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 300 v 1 g;
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Žvýkací pamlsky pro psy
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
II.4. prošly všemi preventivními opatřeními k zabránění kontaminace patogenními původci po ošetření;
II.5. byly zabaleny do nového obalu;
(2) [II.6. výše popsané žvýkací pamlsky pro psy
(2) buď [jsou získány z přežvýkavců jiných než skot, ovce nebo kozy.]]
(2) nebo [jsou získány ze skotu, ovcí nebo koz a neobsahují dále uvedené složky ani z nich nebyly získány:
(2) buď [materiál pocházející ze skotu, ovcí a koz jiný než získaný ze zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]
(2) nebo [a) specifikovaný rizikový materiál, jak je definován v bodě 1 přílohy V nařízení Evropského parlamentu a Rady (ES) č. 999/2001 (4);
b) strojně oddělené maso získané z kostí skotu, ovcí nebo koz s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím Komise 2007/453/ES (5) do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE;
c) vedlejší produkt živočišného původu nebo získaný produkt ze skotu, ovcí nebo koz, které byly po omráčení usmrceny lacerací centrální nervové tkáně pomocí podlouhlého tyčovitého nástroje zavedeného do dutiny lebeční nebo prostřednictvím plynové injekce do dutiny lebeční, s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]]
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
— Kolonka I.12.: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit. Produkty smí být při tranzitu skladovány pouze ve svobodných pásmech, svobodných skladech a celních skladech.
— Kolonka I.15.: Registrační číslo (železničních vagonů nebo kontejneru a nákladních automobilů), číslo letu (letadla) nebo název (plavidla); informace je třeba poskytnout v případě vykládky a opětovného naložení v Evropské unii.
— Kolonka I.19.: 05.11, 23.09, 41.01 nebo 42.05.
— Kolonka I.23.: V případě kontejnerů pro volně ložené látky musí být uvedeno číslo kontejneru a (případně) číslo plomby.
— Kolonka I.25.: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26. a I.27.: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
— Kolonka I.28.: Druh: vyberte: Aves, Ruminantia, Suidae, Mammalia kromě Ruminantia nebo Suidae, Pesca, Mollusca, Crustacea, bezobratlí kromě Mollusca a Crustacea.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
 Text obrazu
Text obrazu
ZEMĚ
Žvýkací pamlsky pro psy
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) Nehodící se škrtněte.
(2a) Úř. věst. L 125, 23.5.1996, s. 3.
(3) Kde:
— n = počet vzorků, které mají být vyšetřeny;
— m = prahová hodnota počtu bakterií; výsledek je považován za uspokojivý, jestliže počet bakterií ve všech vzorcích nepřekročí m;
— M = maximální hodnota počtu bakterií; výsledek je považován za neuspokojivý, pokud počet bakterií v jednom nebo více vzorcích je roven nebo vyšší než M; a
— c = počet vzorků, jejichž bakteriální počet smí být v rozmezí mezi m a M, přičemž vzorek je ještě stále považován za přípustný, pokud je bakteriální počet ostatních vzorků roven m nebo nižší.
(4) Úř. věst. L 147, 31.5.2001, s. 1.
(5) Úř. věst. L 172, 30.6.2007, s. 84.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro osobu zodpovědnou za zásilku v Evropské unii: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly v místě vstupu do Evropské unie.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
KAPITOLA 3 (D)
Veterinární osvědčení
pro syrové krmivo pro zvířata v zájmovém chovu k přímému prodeji nebo pro vedlejší produkty živočišného původu určené ke krmení kožešinových zvířat, určené k odeslání do Evropské unie nebo k tranzitu přes její území (2)
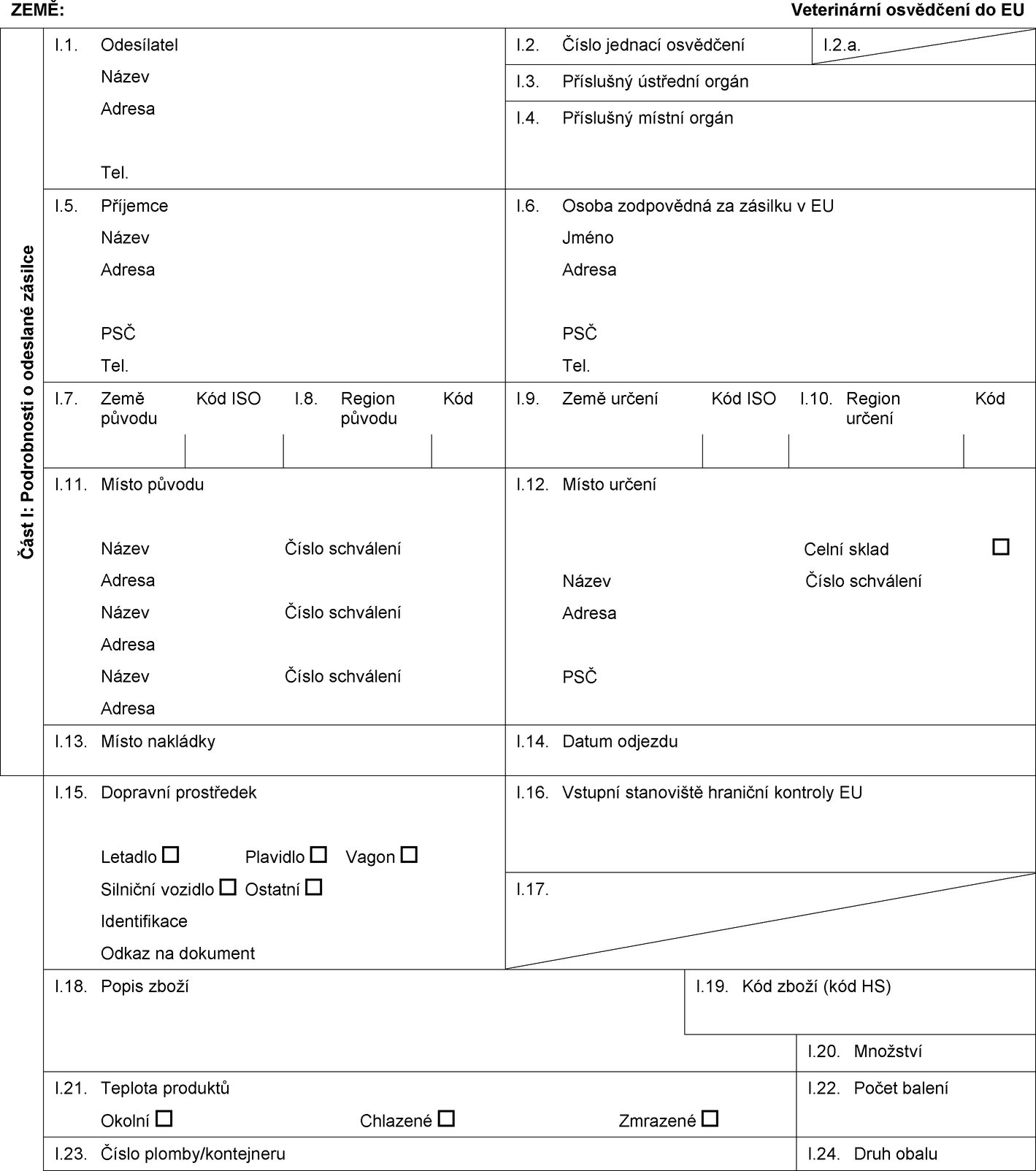 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17.
I.18. Popis zboží
I.19. Kód zboží (kód HS)
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
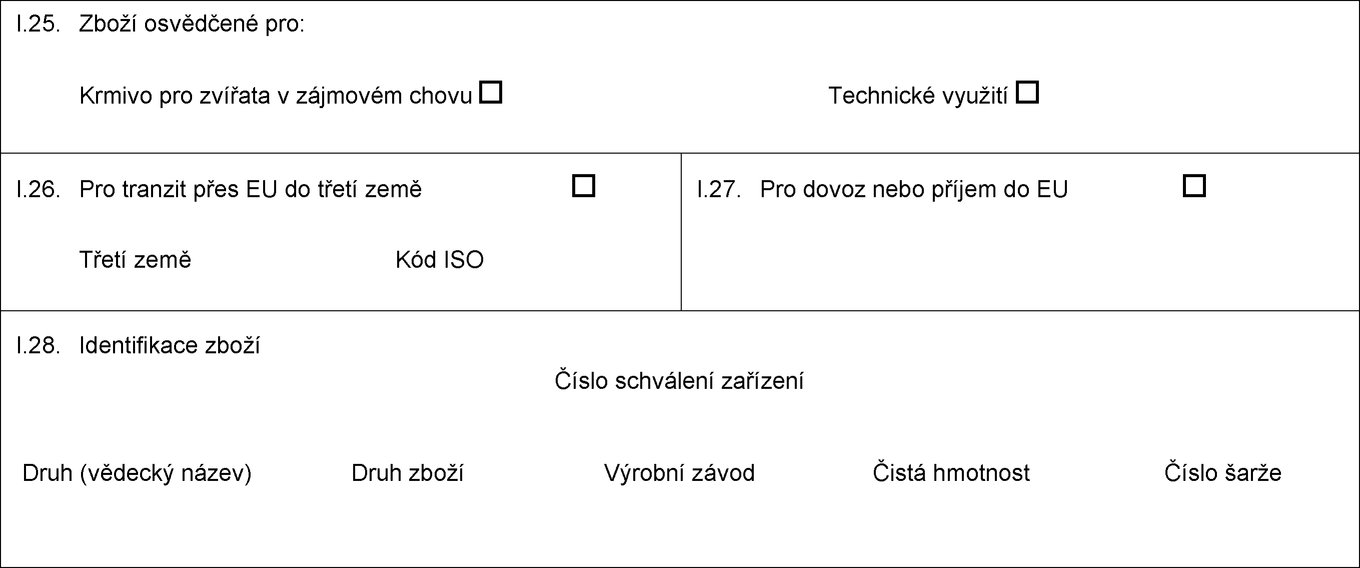 Text obrazu
Text obrazu
I.25. Zboží osvědčené pro:
Krmivo pro zvířata v zájmovém chovu Technické využití
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Druh zboží
Výrobní závod
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Syrové krmivo pro zvířata v zájmovém chovu určené k přímému prodeji nebo vedlejší produkty živočišného původu určené ke krmení kožešinových zvířat
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a), zejména pokud jde o článek 10 uvedeného nařízení, a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu XIII kapitolu II a přílohu XIV kapitolu II uvedeného nařízení, a potvrzuji, že výše popsané syrové krmivo pro zvířata v zájmovém chovu nebo vedlejší produkty živočišného původu:
II.1. sestávají z vedlejších produktů živočišného původu, které splňují veterinární požadavky uvedené níže;
II.2. sestávají z vedlejších produktů živočišného původu:
a) získaných z masa, které splňuje příslušné veterinární a hygienické požadavky stanovené:
— v nařízení Komise (EU) č. 206/2010 (3), a pokud zvířata, z nichž bylo maso získáno, pocházejí ze třetích zemí, území nebo jejich částí … (kód ISO v případě země nebo kódy území nebo jejich částí),
— a/nebo v nařízení Komise (ES) č. 798/2008 (4), a pokud zvířata, z nichž bylo maso získáno, pocházejí z třetích zemí, území nebo jejich částí … (kód ISO v případě země nebo kódy území nebo jejich částí) vyjmenovaných v uvedeném nařízení, které byly posledních 12 měsíců prosté newcastleské choroby a influenzy ptáků,
— a/nebo v nařízení Komise (ES) č. 119/2009 (5), a pokud zvířata, z nichž bylo maso získáno, pocházejí třetích zemí, území nebo jejich částí … (kód ISO v případě země nebo kódy území nebo jejich částí) vyjmenovaných v uvedeném nařízení, které byly předchozích 12 měsíců prosté slintavky a kulhavky, moru skotu, klasického moru prasat, afrického moru prasat, vezikulární choroby prasat, newcastleské choroby a influenzy ptáků a kde během uvedeného období neproběhlo očkování (pouze u vnímavých druhů);
b) získaných ze zvířat, která na jatkách prošla prohlídkou během doby 24 hodin před porážkou a která nevykazovala žádné příznaky nákaz zmíněných v nařízeních uvedených v písmeni a), vůči nimž jsou tato zvířata vnímavá; a
c) získaných ze zvířat, s nimiž bylo na jatkách před porážkou či usmrcením a v době porážky či usmrcení zacházeno v souladu s příslušnými ustanoveními právních předpisů Unie a byly dodrženy požadavky alespoň rovnocenné těm, které jsou stanoveny v kapitolách II a III nařízení Rady (ES) č. 1099/2009 (6); nebo
d) získaných v případě krmiva pro kožešinová zvířata z vodních živočichů, kteří splňují příslušné veterinární a hygienické požadavky stanovené v rozhodnutí Komise 2006/766/ES (7) a pocházejí ze zemí nebo jejich území … (kód ISO země) vyjmenovaných v příloze II uvedeného rozhodnutí;
II.3.1. sestávají pouze z těchto vedlejších produktů živočišného původu:
a) těla poražených zvířat a jejich části, nebo v případě zvěře těla usmrcených zvířat nebo jejich části, které byly podle právních předpisů Unie až do okamžiku, kdy byly z obchodních důvodů nevratně prohlášeny za vedlejší produkty živočišného původu, považovány za vhodné k lidské spotřebě;]
b) části poražených zvířat, které byly prohlášeny za nevhodné k lidské spotřebě, ale které nevykazují žádné příznaky onemocnění přenosných na člověka nebo zvířata a pochází z jatečně upravených těl vhodných k lidské spotřebě v souladu s právními předpisy Unie;
II.3.2. v případě krmiva pro kožešinová zvířata sestávají kromě vedlejších produktů živočišného původu uvedených v bodě II.3.1. i z těchto vedlejších produktů živočišného původu:
(2) buď [- vedlejší produkty živočišného původu z drůbeže a ze zajícovců poražených na farmě, jak je uvedeno v čl. 1 odst. 3 písm. d) nařízení Evropského parlamentu a Rady (ES) č. 853/2004 (2a), kteří nevykazovali příznaky onemocnění přenosného na člověka nebo zvířata;]
(2) a/nebo [- krev zvířat, která nevykazovala žádné příznaky onemocnění přenosného krví na člověka nebo zvířata, která byla poražena na jatkách a která byla po prohlídce před porážkou shledána způsobilými k porážce k lidské spotřebě v souladu s právními předpisy Unie;]
(2) a/nebo [- vedlejší produkty živočišného původu, které vznikají při výrobě produktů určených k lidské spotřebě, včetně odtučněných kostí, škvarků nebo kalu z odstředivky nebo separátoru ze zpracování mléka;]
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Syrové krmivo pro zvířata v zájmovém chovu určené k přímému prodeji nebo vedlejší produkty živočišného původu určené ke krmení kožešinových zvířat
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) a/nebo [- produkty živočišného původu nebo potraviny obsahující produkty živočišného původu, které z obchodních důvodů nebo z důvodů problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny k lidské spotřebě;]
(2) a/nebo [- krmivo pro zvířata v zájmovém chovu a krmivo živočišného původu nebo krmivo obsahující vedlejší produkty živočišného původu či získané produkty, které z obchodních důvodů nebo z důvodu problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny ke krmení;]
(2) a/nebo [- krev, placenta, vlna, peří, srst, rohy, odřezky kopyt a paznehtů a syrové mléko pocházející ze živých zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto produktem na člověka nebo zvířata;]
(2) a/nebo [- vodní živočichové a jejich části, kromě mořských savců, kteří nevykazovali žádné příznaky onemocnění přenosných na člověka nebo zvířata;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních živočichů pocházející z podniků nebo zařízení na výrobu produktů určených k lidské spotřebě;]
(2) a/nebo [- níže uvedený materiál pocházející ze zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto materiálem na člověka nebo zvířata:
i) ulity měkkýšů a korýšů s měkkými tkáněmi nebo masem;
ii) tento materiál pocházející ze suchozemských zvířat:
— vedlejší produkty z líhní,
— vejce,
— vedlejší produkty z vajec, včetně vaječných skořápek;
iii) jednodenní kuřata usmrcená z obchodních důvodů;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních nebo suchozemských bezobratlých živočichů, kromě druhů patogenních pro člověka nebo zvířata;]
(2) a/nebo [- zvířata z řádů hlodavců (Rodentia) a zajícovců (Lagomorpha) a jejich části, kromě materiálu kategorie 1 uvedeného v čl. 8 písm. a) bodech iii), iv) a v) nařízení (ES) č. 1069/2009 a materiálu kategorie 2 uvedeného v čl. 9 písm. a) až g) uvedeného nařízení;]
II.4. byly získány a připraveny, aniž se dostaly do kontaktu s jiným materiálem, který nesplňuje podmínky stanovené v nařízení (ES) č. 1069/2009, a při manipulaci byla učiněna taková opatření, aby nedošlo ke kontaminaci patogenními původci;
II.5. byly zabaleny v konečném balení opatřeném etiketami s nápisem „SYROVÉ KRMIVO PRO ZVÍŘATA V ZÁJMOVÉM CHOVU – NENÍ URČENO K LIDSKÉ SPOTŘEBĚ“ nebo „VEDLEJŠÍ PRODUKTY ŽIVOČIŠNÉHO PŮVODU URČENÉ KE KRMENÍ KOŽEŠINOVÝCH ZVÍŘAT – NENÍ URČENO K LIDSKÉ SPOTŘEBĚ“ a poté uloženy do nepropustných a úředně zaplombovaných krabic/nádob nebo do nepropustného nového obalu a úředně zaplombovaných krabic/nádob opatřených etiketami s nápisem „SYROVÉ KRMIVO PRO ZVÍŘATA V ZÁJMOVÉM CHOVU – NENÍ URČENO K LIDSKÉ SPOTŘEBĚ“ nebo „VEDLEJŠÍ PRODUKTY ŽIVOČIŠNÉHO PŮVODU URČENÉ KE KRMENÍ KOŽEŠINOVÝCH ZVÍŘAT – NENÍ URČENO K LIDSKÉ SPOTŘEBĚ“ a názvem a adresou zařízení určení;
II.6. v případě syrového krmiva pro zvířata v zájmovém chovu:
a) bylo připraveno a skladováno v podniku schváleném a dozorovaném příslušným orgánem v souladu s článkem 24 nařízení (ES) č. 1069/2009 a
b) bylo analyzováno pomocí alespoň pěti vzorků z každé šarže namátkově odebraných během skladování (před odesláním) a vyhovuje těmto normám (8):
 Text obrazu
Text obrazu
ZEMĚ
Syrové krmivo pro zvířata v zájmovém chovu určené k přímému prodeji nebo vedlejší produkty živočišného původu určené ke krmení kožešinových zvířat
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Salmonella: nepřítomnost v 25 g produktu: n = 5, c = 0, m =0, M = 0
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 5 000 v 1 g;
(2) [II.7. [výše popsané krmivo pro zvířata v zájmovém chovu nebo vedlejší produkty živočišného původu určené ke krmení kožešinových zvířat obsahují vedlejší produkty živočišného původu z přežvýkavců nebo jsou z nich získány a:
(2) buď [pocházejí ze země nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE, a]]
(2) nebo [pocházejí ze země nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž byl zjištěn domácí případ BSE, a vedlejší produkt živočišného původu nebo získaný produkt byl získán ze zvířat narozených po datu, od kterého byl v uvedené zemi nebo oblasti účinně vymáhán zákaz krmení přežvýkavců masokostní moučkou a škvarky získanými z přežvýkavců, jak jsou definovány v Kodexu zdraví suchozemských živočichů OIE, a]]
(2) buď [jsou získány z přežvýkavců jiných než skot, ovce nebo kozy.]]
(2) nebo [jsou získány ze skotu, ovcí nebo koz a neobsahují dále uvedené složky ani z nich nebyly získány:
(2) buď [materiál pocházející ze skotu, ovcí a koz jiný než získaný ze zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]
(2) nebo [a) specifikovaný rizikový materiál, jak je definován v bodě 1 přílohy V nařízení Evropského parlamentu a Rady (ES) č. 999/2001 (9);
b) strojně oddělené maso získané z kostí skotu, ovcí nebo koz s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím Komise 2007/453/ES (10) do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE;
c) vedlejší produkt živočišného původu nebo získaný produkt ze skotu, ovcí nebo koz, které byly po omráčení usmrceny lacerací centrální nervové tkáně pomocí podlouhlého tyčovitého nástroje zavedeného do dutiny lebeční nebo prostřednictvím plynové injekce do dutiny lebeční, s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]]
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit přes Evropskou unii; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
— Kolonka I.12.: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit. Produkty smí být při tranzitu skladovány pouze ve svobodných pásmech, svobodných skladech a celních skladech.
— Kolonka I.15.: Je třeba uvést registrační číslo (vagony nebo kontejnery a nákladní automobily), číslo letu (letadlo) nebo název (plavidlo). V případě vykládky a opětovného naložení musí odesílatel informovat stanoviště hraniční kontroly v místě vstupu do Evropské unie.
— Kolonka I.19.: Použijte příslušný kód harmonizovaného systému (HS) následujícího čísla: 04.08, 05.06, 05.08, 05.11, 23.01 nebo 23.09.
— Kolonka I.23.: V případě kontejnerů pro volně ložené látky musí být uvedeno číslo kontejneru a (případně) číslo plomby.
— Kolonka I.25.: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26. a I.27.: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
 Text obrazu
Text obrazu
ZEMĚ
Syrové krmivo pro zvířata v zájmovém chovu určené k přímému prodeji nebo vedlejší produkty živočišného původu určené ke krmení kožešinových zvířat
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
— Kolonka I.28.:
Druh zboží: uveďte syrové krmivo pro zvířata v zájmovém chovu nebo vedlejší produkt živočišného původu.
V případě syrového materiálu pro výrobu syrového krmiva pro zvířata v zájmovém chovu uveďte vědecký název druhu.
V případě syrového materiálu pro výrobu krmiva pro kožešinová zvířata vyberte: Aves, Ruminantia, Suidae, Mammalia kromě Ruminantia nebo Suidae, Pesca, Mollusca, Crustacea, bezobratlí kromě Mollusca a Crustacea.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
(2) Nehodící se škrtněte.
(2a) Úř. věst. L 139, 30.4.2004, s. 55.
(3) Úř. věst. L 73, 20.3.2010, s. 1.
(4) Úř. věst. L 226, 23.8.2008, s. 1.
(5) Úř. věst. L 39, 10.2.2009, s. 12.
(6) Úř. věst. L 303, 18.11.2009, s. 1.
(7) Úř. věst. L 320, 18.11.2006, s. 53.
(8) Kde:
n = počet vzorků, které mají být vyšetřeny;
m = prahová hodnota počtu bakterií; výsledek je považován za uspokojivý, jestliže počet bakterií ve všech vzorcích nepřekročí m;
M = maximální hodnota počtu bakterií; výsledek je považován za neuspokojivý, pokud počet bakterií v jednom nebo více vzorcích je roven nebo vyšší než M; a
c = počet vzorků, jejichž bakteriální počet smí být v rozmezí mezi m a M, přičemž vzorek je ještě stále považován za přípustný, pokud je bakteriální počet ostatních vzorků roven m nebo nižší.
(9) Úř. věst. L 147, 31.5.2001, s. 1.
(10) Úř. věst. L 172, 30.6.2007, s. 84.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro osobu zodpovědnou za zásilku v Evropské unii: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly Evropské unie.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
KAPITOLA 3 (E)
Veterinární osvědčení
pro dochucovací masové výtažky pro výrobu krmiva pro zvířata v zájmovém chovu, určené k odeslání do Evropské unie nebo k tranzitu přes její území (2)
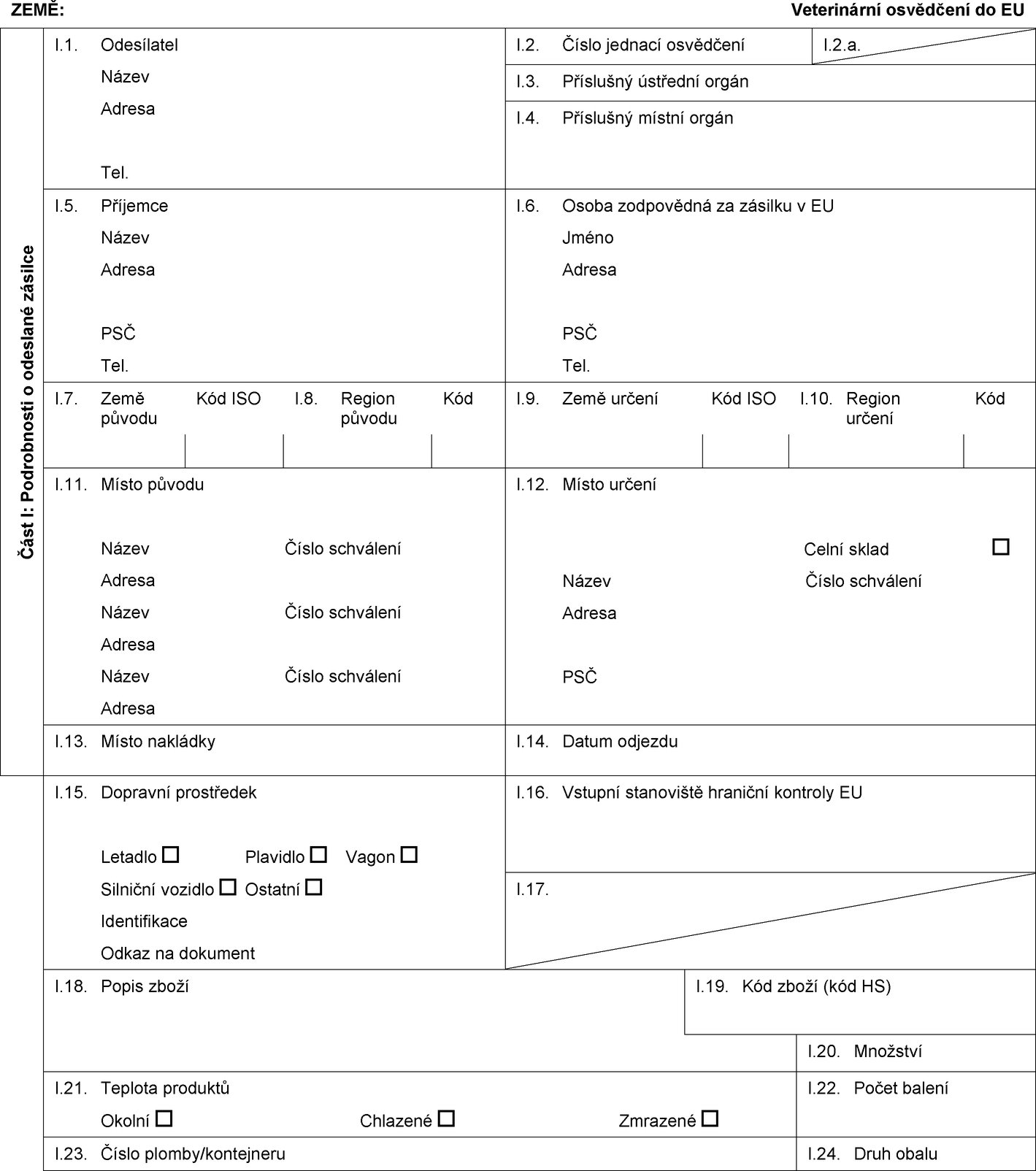 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17.
I.18. Popis zboží
I.19. Kód zboží (kód HS)
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
 Text obrazu
Text obrazu
I.25. Zboží osvědčené pro:
Krmivo pro zvířata v zájmovém chovu Technické využití
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Druh zboží
Výrobní závod
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Dochucovací masové výtažky pro výrobu krmiva pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a), zejména pokud jde o články 8 a 10 uvedeného nařízení, a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu XIII kapitolu III a přílohu XIV kapitolu II uvedeného nařízení, a potvrzuji, že výše popsané dochucovací masové výtažky:
II.1. sestávají z vedlejších produktů živočišného původu, které splňují veterinární požadavky uvedené níže;
II.2. byly připraveny výhradně z těchto vedlejších produktů živočišného původu a obsahují výhradně tyto vedlejší produkty živočišného původu:
(2) buď [- těla poražených zvířat a jejich části, nebo v případě zvěře těla usmrcených zvířat nebo jejich části, které jsou podle právních předpisů Unie vhodné k lidské spotřebě, avšak z obchodních důvodů nejsou k lidské spotřebě určeny;]
(2) a/nebo [- jatečně upravená těla a níže uvedené části pocházející buď ze zvířat, která byla poražena na jatkách a po prohlídce před porážkou byla shledána jako způsobilá k porážce k lidské spotřebě, nebo těla a níže uvedené části zvěře usmrcené k lidské spotřebě v souladu s právními předpisy Unie:
i) jatečně upravená těla nebo těla zvířat a jejich části, které byly v souladu s právními předpisy Unie prohlášeny za nevhodné k lidské spotřebě, avšak nevykazovaly žádné příznaky onemocnění přenosného na člověka nebo zvířata;
ii) hlavy drůbeže;
iii) kůže a kožky, včetně jejich odřezků a plátků, rohy a končetiny, včetně článků prstů, zápěstních a záprstních kůstek, nártů a zánártí;
iv) prasečí štětiny;
v) peří;]
(2) a/nebo [- krev zvířat, která nevykazovala žádné příznaky onemocnění přenosného krví na člověka nebo zvířata, která byla poražena na jatkách a která byla po prohlídce před porážkou shledána způsobilými k porážce k lidské spotřebě v souladu s právními předpisy Unie;]
(2) a/nebo [- vedlejší produkty živočišného původu, které vznikají při výrobě produktů určených k lidské spotřebě, včetně odtučněných kostí, škvarků nebo kalu z odstředivky nebo separátoru ze zpracování mléka; ]
(2) a/nebo [- produkty živočišného původu nebo potraviny obsahující produkty živočišného původu, které z obchodních důvodů nebo z důvodů problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny k lidské spotřebě;]
(2) a/nebo [- krmivo pro zvířata v zájmovém chovu a krmivo živočišného původu nebo krmivo obsahující vedlejší produkty živočišného původu či získané produkty, které z obchodních důvodů nebo z důvodu problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny ke krmení;]
(2) a/nebo [- krev, placenta, vlna, peří, srst, rohy, odřezky kopyt a paznehtů a syrové mléko pocházející ze živých zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto produktem na člověka nebo zvířata;]
(2) a/nebo [- vodní živočichové a jejich části, kromě mořských savců, kteří nevykazovali žádné příznaky onemocnění přenosných na člověka nebo zvířata;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních živočichů pocházející z podniků nebo zařízení na výrobu produktů určených k lidské spotřebě;]
(2) a/nebo [- níže uvedený materiál pocházející ze zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto materiálem na člověka nebo zvířata:
i) ulity měkkýšů a korýšů s měkkými tkáněmi nebo masem;
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Dochucovací masové výtažky pro výrobu krmiva pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
ii) tento materiál pocházející ze suchozemských zvířat:
– vedlejší produkty z líhní,
– vejce,
– vedlejší produkty z vajec, včetně vaječných skořápek;
iii) jednodenní kuřata usmrcená z obchodních důvodů;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních nebo suchozemských bezobratlých živočichů, kromě druhů patogenních pro člověka nebo zvířata;]
(2) a/nebo [- zvířata z řádů hlodavců (Rodentia) a zajícovců (Lagomorpha) a jejich části, kromě materiálu kategorie 1 uvedeného v čl. 8 písm. a) bodech iii), iv) a v) nařízení (ES) č. 1069/2009 a materiálu kategorie 2 uvedeného v čl. 9 písm. a) až g) uvedeného nařízení;]
(2) a/nebo [- materiál ze zvířat, která byla ošetřena některými látkami zakázanými podle směrnice Rady 96/22/ES (2b), přičemž dovoz tohoto materiálu byl povolen v souladu s čl. 35 písm. a) bodem ii) nařízení (ES) č. 1069/2009;]
II.3. byly podrobeny zpracování v souladu s přílohou XIII kapitolou III nařízení (EU) č. 142/2011 za účelem zničení patogenních původců;
II.4. byly analyzovány pomocí alespoň pěti vzorků z každé zpracované šarže namátkově odebraných během skladování nebo při vyskladnění ve zpracovatelském zařízení a vyhovují těmto normám (3):
Salmonella: nepřítomnost v 25 g produktu: n = 5, c = 0, m = 0, M = 0
Enterobacteriaceae: n = 5, c = 2, m = 10, M = 300 v 1 g;
II.5. konečný produkt byl:
(2) buď [zabalen do nových nebo sterilizovaných pytlů, ]
(2) nebo [přepravován volně ložený v kontejnerech nebo jiných dopravních prostředcích, které byly před použitím důkladně vyčištěny a vydezinfikovány dezinfekčním přípravkem schváleným příslušným orgánem]
a které jsou opatřeny etiketami s nápisem „NENÍ URČENO K LIDSKÉ SPOTŘEBĚ“;
II.6. konečný produkt byl uložen v uzavřeném skladišti;
II.7. produkt prošel všemi preventivními opatřeními k zabránění kontaminace patogenními původci po ošetření;
(2) [II.8. výše popsané dochucovací masové výtažky
(2) buď [jsou získány z přežvýkavců jiných než skot, ovce nebo kozy.]]
(2) nebo [jsou získány ze skotu, ovcí nebo koz a neobsahují dále uvedené složky ani z nich nebyly získány:
(2) buď [materiál pocházející ze skotu, ovcí a koz jiný než získaný ze zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]
(2) nebo [a) specifikovaný rizikový materiál, jak je definován v bodě 1 přílohy V nařízení Evropského parlamentu a Rady (ES) č. 999/2001 (4);
b) strojně oddělené maso získané z kostí skotu, ovcí nebo koz s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím Komise 2007/453/ES (5) do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE;
c) vedlejší produkt živočišného původu nebo získaný produkt ze skotu, ovcí nebo koz, které byly po omráčení usmrceny lacerací centrální nervové tkáně pomocí podlouhlého tyčovitého nástroje zavedeného do dutiny lebeční nebo prostřednictvím plynové injekce do dutiny lebeční, s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]]
 Text obrazu
Text obrazu
ZEMĚ
Dochucovací masové výtažky pro výrobu krmiva pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit přes Evropskou unii; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
— Kolonka I.12.: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit. Produkty smí být při tranzitu skladovány pouze ve svobodných pásmech, svobodných skladech a celních skladech.
— Kolonka I.15.: Registrační číslo (železničních vagonů nebo kontejneru a nákladních automobilů), číslo letu (letadla) nebo název (plavidla); informace je třeba poskytnout v případě vykládky a opětovného naložení v Evropské unii.
— Kolonka I.19.: Použijte příslušný kód HS: 05.04, 05.06, 05.11 nebo 23.09.
— Kolonka I.23.: V případě kontejnerů pro volně ložené látky by mělo být uvedeno číslo kontejneru a číslo plomby (v příslušných případech).
— Kolonka I.25.: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26. a I.27.: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
— Kolonka I.28.:
— Druh: vyberte: Aves, Ruminantia, Suidae, Mammalia kromě Ruminantia nebo Suidae, Pesca, Mollusca, Crustacea, bezobratlí kromě Mollusca a Crustacea.
— Specifikujte masový výtažek.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
(2) Nehodící se škrtněte.
(2a) Úř. věst. L 125, 23.5.1996, s. 3.
(3) Kde:
n = počet vzorků, které mají být vyšetřeny;
m = prahová hodnota počtu bakterií; výsledek je považován za uspokojivý, jestliže počet bakterií ve všech vzorcích nepřekročí m;
M = maximální hodnota počtu bakterií; výsledek je považován za neuspokojivý, pokud počet bakterií v jednom nebo více vzorcích je roven nebo vyšší než M; a
c = počet vzorků, jejichž bakteriální počet smí být v rozmezí mezi m a M, přičemž vzorek je ještě stále považován za přípustný, pokud je bakteriální počet ostatních vzorků roven m nebo nižší.
(4) Úř. věst. L 147, 31.5.2001, s. 1.
(5) Úř. věst. L 172, 30.6.2007, s. 84.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro osobu zodpovědnou za zásilku v Evropské unii: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
KAPITOLA 3 (F)
Veterinární osvědčení
pro vedlejší produkty živočišného původu (3) pro výrobu krmiva pro zvířata v zájmovém chovu, určené k odeslání do Evropské unie nebo k tranzitu přes její území (2)
 Text obrazu
Text obrazu
ZEMĚ:
Veterinární osvědčení do EU
Část I: Podrobnosti o odeslané zásilce
I.1. Odesílatel
Název
Adresa
Tel.
I.2. Číslo jednací osvědčení
I.2.a.
I.3. Příslušný ústřední orgán
I.4. Příslušný místní orgán
I.5. Příjemce
Název
Adresa
PSČ
Tel.
I.6. Osoba zodpovědná za zásilku v EU
Jméno
Adresa
PSČ
Tel.
I.7. Země původu
Kód ISO
I.8. Region původu
Kód
I.9. Země určení
Kód ISO
I.10. Region určení
Kód
I.11. Místo původu
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
Název Číslo schválení
Adresa
I.12. Místo určení
Celní sklad
Název Číslo schválení
Adresa
PSČ
I.13. Místo nakládky
I.14. Datum odjezdu
I.15. Dopravní prostředek
Letadlo Plavidlo Vagon
Silniční vozidlo Ostatní
Identifikace
Odkaz na dokument
I.16. Vstupní stanoviště hraniční kontroly EU
I.17.
I.18. Popis zboží
I.19. Kód zboží (kód HS)
I.20. Množství
I.21. Teplota produktů
Okolní Chlazené Zmrazené
I.22. Počet balení
I.23. Číslo plomby/kontejneru
I.24. Druh obalu
 Text obrazu
Text obrazu
I.25. Zboží osvědčené pro:
Výroba krmiva pro zvířata v zájmovém chovu Další zpracování Technické využití
I.26. Pro tranzit přes EU do třetí země
Třetí země Kód ISO
I.27. Pro dovoz nebo příjem do EU
I.28. Identifikace zboží
Číslo schválení zařízení
Druh (vědecký název)
Druh zboží
Výrobní závod
Počet balení
Čistá hmotnost
Číslo šarže
 Text obrazu
Text obrazu
ZEMĚ
Vedlejší produkty živočišného původu pro výrobu krmiva pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
Já, níže podepsaný úřední veterinární lékař, prohlašuji, že jsem přečetl a porozuměl nařízení Evropského parlamentu a Rady (ES) č. 1069/2009 (1a) a nařízení Komise (EU) č. 142/2011 (1b), zejména pokud jde o přílohu XIV kapitolu II uvedeného nařízení, a potvrzuji, že výše popsané vedlejší produkty živočišného původu:
II.1.1. sestávají z vedlejších produktů živočišného původu, které splňují veterinární požadavky uvedené níže;
II.1.2. byly získány na území: (1c) ze zvířat:
(2) buď [a) která pobývala na tomto území od narození nebo alespoň po dobu tří měsíců před datem porážky;]
(2) nebo [b) která byla usmrcena v přírodě na tomto území (1d);]
(2) nebo [c) byly získány z hlodavců, zajícovitých, vodních živočichů nebo suchozemských nebo vodních bezobratlých živočichů;]
II.1.3. byly získány nebo vyrobeny ze zvířat:
(2) buď [a) pocházejících z hospodářství:
i) kde nebyl zaznamenán žádný případ / žádné ohnisko následujících nákaz, vůči nimž jsou tato zvířata vnímavá: po dobu předchozích 30 dnů mor skotu, vezikulární choroba prasat, newcastleská choroba nebo vysoce patogenní influenza ptáků, po dobu předchozích 40 dnů klasický mor prasat nebo africký mor prasat, ani nebyl po dobu předchozích 30 dnů žádný takový případ / žádné takové ohnisko zaznamenán/o v hospodářstvích v okruhu 10 km; a
ii) kde nebyl po dobu předchozích 60 dnů zaznamenán žádný případ / žádné ohnisko slintavky a kulhavky, ani nebyl po dobu předchozích 30 dnů žádný takový případ / žádné takové ohnisko zaznamenán/o v hospodářstvích v okruhu 25 km; a
b) která:
i) nebyla usmrcena za účelem eradikace epizootické nákazy;
ii) zůstala v hospodářství původu po dobu alespoň 40 dnů před datem odjezdu a byla přepravena přímo na jatka, aniž se dostala do kontaktu s jinými zvířaty, která nesplňují stejné veterinární podmínky;
iii) prošla na jatkách veterinární prohlídkou v průběhu 24 hodin před porážkou a nevykazovala žádné příznaky výše uvedených nákaz, vůči nimž jsou tato zvířata vnímavá; a
iv) bylo s nimi na jatkách před porážkou či usmrcením a v době porážky či usmrcení zacházeno v souladu s příslušnými ustanoveními právních předpisů Unie a byly dodrženy požadavky alespoň rovnocenné těm, které jsou stanoveny v kapitolách II a III nařízení Rady (ES) č. 1099/2009 (4);]
(2) nebo [a) která byla chycena a usmrcena v přírodě v oblasti:
i) kde v okruhu 25 km nebyl zaznamenán žádný případ / žádné ohnisko následujících nákaz, vůči nimž jsou tato zvířata vnímavá: po dobu předchozích 30 dnů slintavka a kulhavka, mor skotu, newcastleská choroba nebo vysoce patogenní influenza ptáků a po dobu předchozích 40 dnů klasický mor prasat nebo africký mor prasat; a
ii) nacházející se nejméně 20 km od země nebo části území země, která nebyla oprávněna vyvážet materiál z drůbeže do Evropské unie během předchozích 30 dnů nebo materiál z prasat během předchozích 40 dnů; a
b) která byla do 12 hodin po usmrcení převezena za účelem chlazení buď do sběrného střediska a bezprostředně poté do zařízení na zpracování zvěře, nebo přímo do zařízení na zpracování zvěře;]
Část II: Osvědčení
 Text obrazu
Text obrazu
ZEMĚ
Vedlejší produkty živočišného původu pro výrobu krmiva pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
II.1.4. byly získány v zařízení, kde v okruhu 10 km nebyl po dobu předchozích 30 dnů zaznamenán žádný případ/ohnisko nákaz uvedených v bodě II.1.3., vůči nimž jsou tato zvířata vnímavá, nebo pokud byl zaznamenán případ nákazy, byla příprava suroviny pro vývoz do Evropské unie povolena pouze po odstranění veškerého masa a po celkovém vyčištění a dezinfekci zařízení pod dohledem úředního veterinárního lékaře;
II.1.5. byly získány a připraveny, aniž se dostaly do kontaktu s jinými materiály, které nesplňují podmínky uvedené výše, a manipulace s nimi probíhala tak, aby nedošlo ke kontaminaci patogenními původci;
II.1.6. byly zabaleny v nepropustném novém obalu a úředně zaplombovaných nádobách opatřených etiketou s nápisem „SYROVÝ MATERIÁL POUZE PRO VÝROBU KRMIVA PRO ZVÍŘATA V ZÁJMOVÉM CHOVU“ a názvem a adresou zařízení určení v Evropské unii;
II.1.7. sestávají pouze z těchto vedlejších produktů živočišného původu:
(2) buď [- těla poražených zvířat a jejich části, nebo v případě zvěře těla usmrcených zvířat nebo jejich části, které byly podle právních předpisů Unie až do okamžiku, kdy byly z obchodních důvodů nevratně prohlášeny za vedlejší produkty živočišného původu, považovány za vhodné k lidské spotřebě;]
(2) a/nebo [- jatečně upravená těla a níže uvedené části pocházející buď ze zvířat, která byla poražena na jatkách a po prohlídce před porážkou byla shledána jako způsobilá k porážce k lidské spotřebě, nebo těla a níže uvedené části zvěře usmrcené k lidské spotřebě v souladu s právními předpisy Unie:
i) jatečně upravená těla nebo těla zvířat a jejich části, které byly v souladu s právními předpisy Unie prohlášeny za nevhodné k lidské spotřebě, avšak nevykazovaly žádné příznaky onemocnění přenosného na člověka nebo zvířata;
ii) hlavy drůbeže;
iii) kůže a kožky, včetně jejich odřezků a plátků, rohy a končetiny, včetně článků prstů, zápěstních a záprstních kůstek, nártů a zánártí;
iv) prasečí štětiny;
v) peří;]
(2) a/nebo [- vedlejší produkty živočišného původu, které vznikají při výrobě produktů určených k lidské spotřebě, včetně odtučněných kostí, škvarků nebo kalu z odstředivky nebo separátoru ze zpracování mléka;]
(2) a/nebo [- produkty živočišného původu nebo potraviny obsahující produkty živočišného původu, které z obchodních důvodů nebo z důvodů problémů způsobených výrobními vadami, vadami balení nebo jinými závadami, z nichž nevzniká žádné riziko pro zdraví lidí ani zvířat, již nejsou určeny k lidské spotřebě;]
(2) a/nebo [- vodní živočichové a jejich části, kromě mořských savců, kteří nevykazovali žádné příznaky onemocnění přenosných na člověka nebo zvířata;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních živočichů pocházející z podniků nebo zařízení na výrobu produktů určených k lidské spotřebě;]
(2) a/nebo [- níže uvedený materiál pocházející ze zvířat, která nevykazovala žádné příznaky onemocnění přenosného tímto materiálem na člověka nebo zvířata:
i) ulity měkkýšů a korýšů s měkkými tkáněmi nebo masem;
ii) tento materiál pocházející ze suchozemských zvířat:
— vedlejší produkty z líhní,
— vejce,
— vedlejší produkty z vajec, včetně vaječných skořápek;
 Text obrazu
Text obrazu
ZEMĚ
Vedlejší produkty živočišného původu pro výrobu krmiva pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
iii) jednodenní kuřata usmrcená z obchodních důvodů;]
(2) a/nebo [- vedlejší produkty živočišného původu z vodních nebo suchozemských bezobratlých živočichů, kromě druhů patogenních pro člověka nebo zvířata;]
(2) a/nebo [- zvířata z řádů hlodavců (Rodentia) a zajícovců (Lagomorpha) a jejich části, kromě materiálu kategorie 1 uvedeného v čl. 8 písm. a) bodech iii), iv) a v) nařízení (ES) č. 1069/2009 a materiálu kategorie 2 uvedeného v čl. 9 písm. a) až g) uvedeného nařízení;]
(2) a/nebo [- materiál ze zvířat, která byla ošetřena některými látkami zakázanými podle směrnice Rady 96/22/ES (4a), přičemž dovoz tohoto materiálu byl povolen v souladu s čl. 35 písm. a) bodem ii) nařízení (ES) č. 1069/2009;]
II.1.8. byly hluboce zmrazeny v podniku původu nebo konzervovány v souladu s právními předpisy Evropské unie takovým způsobem, aby se v době mezi odesláním a dodáním do podniku určení v Evropské unii nebo během tranzitu přes Evropskou unii nezkazily;
II.1.9. v případě surovin získaných ze zvířat, která byla ošetřena některými látkami zakázanými směrnicí 96/22/ES pro výrobu krmiva pro zvířata v zájmovém chovu, jejichž dovoz je povolen v souladu s čl. 35 písm. a) bodem ii) nařízení (ES) č. 1069/2009:
a) byla tato surovina ve třetí zemi před vstupem na území Evropské unie označena křížem z tekutého dřevěného uhlí nebo aktivního uhlí na každé vnější straně každého zmrazeného bloku, nebo pokud je surovina přepravována na paletách, které nejsou během přepravy do zařízení určení na výrobu krmiva pro zvířata v zájmovém chovu v Evropské unii nebo během tranzitu přes Evropskou unii rozděleny do jednotlivých zásilek, na každé vnější straně každé palety, a to takovým způsobem, že označení pokrývá nejméně 70 % úhlopříčné délky zmrazeného bloku a má šířku nejméně 10 cm;
b) v případě materiálu, který není zmrazený, byla surovina ve třetí zemi před vstupem na území Evropské unie označena nastříkáním tekutého dřevěného uhlí nebo nanesením práškového dřevěného uhlí tak, aby bylo dřevěné uhlí na materiálu jasně patrné; a
c) v případě, že jsou vedlejší produkty živočišného původu vyrobeny ze suroviny, která byla ošetřena výše uvedeným způsobem, a z jiné neošetřené suroviny, byly všechny tyto suroviny označeny způsobem uvedeným výše v písmenech a) a b).
(2) (5) [II.2. Zvláštní požadavky
(2) (6) [II.2.1. Vedlejší produkty v této zásilce pocházejí ze zvířat, která byla držena na území uvedeném v bodě II.1.2., kde se u domácího skotu pravidelně provádějí programy očkování proti slintavce a kulhavce a kde je tato nákaza úředně kontrolována.]
(2) (7) [II.2.2. Vedlejší produkty v této zásilce sestávají pouze z vedlejších produktů živočišného původu získaných z opracovaných drobů domácích přežvýkavců, které zrály při okolní teplotě vyšší než + 2 °C po dobu nejméně tří hodin nebo, v případě žvýkacích svalů skotu a vykostěného masa domácích zvířat, nejméně 24 hodin.]]
(2) [II.3. Vedlejší produkty živočišného původu pro výrobu krmiva pro zvířata v zájmovém chovu obsahují vedlejší produkty živočišného původu z přežvýkavců nebo jsou z nich získány a:
(2) buď [pocházejí ze země nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE, a]]
(2) nebo [pocházejí ze země nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž byl zjištěn domácí případ BSE, a vedlejší produkt živočišného původu nebo získaný produkt byl získán ze zvířat narozených po datu, od kterého byl v uvedené zemi nebo oblasti účinně vymáhán zákaz krmení přežvýkavců masokostní moučkou a škvarky získanými z přežvýkavců, jak jsou definovány v Kodexu zdraví suchozemských živočichů OIE, a]]
(2) buď [jsou získány z přežvýkavců jiných než skot, ovce nebo kozy.]
 Text obrazu
Text obrazu
ZEMĚ
Vedlejší produkty živočišného původu pro výrobu krmiva pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(2) nebo [jsou získány ze skotu, ovcí nebo koz a neobsahují dále uvedené složky ani z nich nebyly získány:
(2) buď [materiál pocházející ze skotu, ovcí a koz jiný než získaný ze zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]]
(2) nebo [a) specifikovaný rizikový materiál, jak je definován v bodě 1 přílohy V nařízení Evropského parlamentu a Rady (ES) č. 999/2001 (8);
b) strojně oddělené maso získané z kostí skotu, ovcí nebo koz s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím Komise 2007/453/ES (9) do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE, v nichž nebyl zjištěn žádný domácí případ BSE;
c) vedlejší produkt živočišného původu nebo získaný produkt ze skotu, ovcí nebo koz, které byly po omráčení usmrceny lacerací centrální nervové tkáně pomocí podlouhlého tyčovitého nástroje zavedeného do dutiny lebeční nebo prostřednictvím plynové injekce do dutiny lebeční, s výjimkou zvířat narozených, nepřetržitě chovaných a poražených v zemi nebo oblasti zařazené v souladu s rozhodnutím 2007/453/ES do kategorie země nebo oblasti se zanedbatelným rizikem výskytu BSE.]]]]
Poznámky
Část I:
— Kolonka I.6.: Osoba zodpovědná za zásilku v Evropské unii: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit; může se vyplnit, jedná-li se o osvědčení pro zboží dovážené do Evropské unie.
— Kolonka I.12: Místo určení: tuto kolonku je třeba vyplnit pouze tehdy, jedná-li se o osvědčení pro zboží určené pro tranzit. Produkty smí být při tranzitu skladovány pouze ve svobodných pásmech, svobodných skladech a celních skladech.
— Kolonka I.15: Registrační číslo (železničních vagonů nebo kontejneru a nákladních automobilů), číslo letu (letadla) nebo název (plavidla); informace je třeba poskytnout v případě vykládky a opětovného naložení v Evropské unii.
— Kolonka I.19: Použijte příslušný kód HS: 05.04, 05.06, 05.07, 05.11.91 nebo 05.11.99; 23.01 a 41.01.
— Kolonka I.23: V případě kontejnerů pro volně ložené látky by mělo být uvedeno číslo kontejneru a (případně) číslo plomby.
— Kolonka I.25: Technické využití: jakékoli jiné využití kromě krmení hospodářských zvířat jiných než kožešinových zvířat a výroba nebo zpracování krmiv pro zvířata v zájmovém chovu.
— Kolonky I.26 a I.27: Vyplňte podle toho, jedná-li se o osvědčení pro tranzit nebo pro dovoz.
— Kolonka I.28:
— Druh: vyberte: Aves, Ruminantia, Suidae, Mammalia kromě Ruminantia nebo Suidae, Pesca, Mollusca, Crustacea, bezobratlí kromě Mollusca a Crustacea.
— Výrobní závod: uveďte číslo veterinární kontroly schváleného zařízení.
Část II:
(1a) Úř. věst. L 300, 14.11.2009, s. 1.
(1b) Úř. věst. L 54, 26.2.2011, s. 1.
 Text obrazu
Text obrazu
ZEMĚ
Vedlejší produkty živočišného původu pro výrobu krmiva pro zvířata v zájmovém chovu
II. Zdravotní informace
II.a. Číslo jednací osvědčení
II.b.
(1c) Název a kód ISO vyvážející země v souladu s:
— s přílohou II částí 1 nařízení (EU) č. 206/2010,
— s přílohou I částí 1 nařízení (ES) č. 798/2008 a
— s přílohou I částí 1 nařízení (ES) č. 119/2009.
Navíc musí být uveden i kód ISO pro regionalizaci ve výše zmíněných přílohách (pokud jde o dotčené vnímavé druhy).
(1d) Pouze pro země, z nichž je povolen dovoz masa zvěře týchž živočišných druhů určeného k lidské spotřebě do Evropské unie.
(2) Nehodící se škrtněte.
(3) S výjimkou syrové krve, syrového mléka, kůží a kožek, kopyt a paznehtů, rohů, prasečích štětin a peří (viz příslušná specifická osvědčení pro dovoz těchto produktů v uvedené příloze).
(4) Úř. věst. L 303, 18.11.2009, s. 1.
(4a) Úř. věst. L 125, 23.5.1996, s. 3.
(5) Doplňkové záruky je nutno poskytnout v případě, že materiál z domácích přežvýkavců pochází z území jihoamerické nebo jihoafrické země nebo její části, odkud je do Evropské unie povolen pouze vývoz vyzrálého a vykostěného čerstvého masa domácích přežvýkavců k lidské spotřebě. Celé žvýkací svaly skotu naříznuté v souladu s přílohou I oddílem IV kapitolou I částí B bodem 1 nařízení Evropského parlamentu a Rady (ES) č. 854/2004 (Úř. věst. L 139, 30.4.2004, s. 206) jsou rovněž povoleny.
(6) Pouze pro některé jihoamerické země.
(7) Pouze pro některé jihoamerické a jihoafrické země.
(8) Úř. věst. L 147, 31.5.2001, s. 1.
(9) Úř. věst. L 172, 30.6.2007, s. 84.
— Barva podpisu a razítka se musí lišit od barvy tisku.
— Poznámka pro osobu zodpovědnou za zásilku v Evropské unii: toto osvědčení slouží pouze k veterinárním účelům a musí zásilku provázet až do okamžiku, kdy dosáhne stanoviště hraniční kontroly Evropské unie.
Úřední veterinární lékař / úřední inspektor
Jméno (hůlkovým písmem): Kvalifikace a titul:
Datum: Podpis:
Razítko:
“ |
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
“
Text obrazu
“ Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
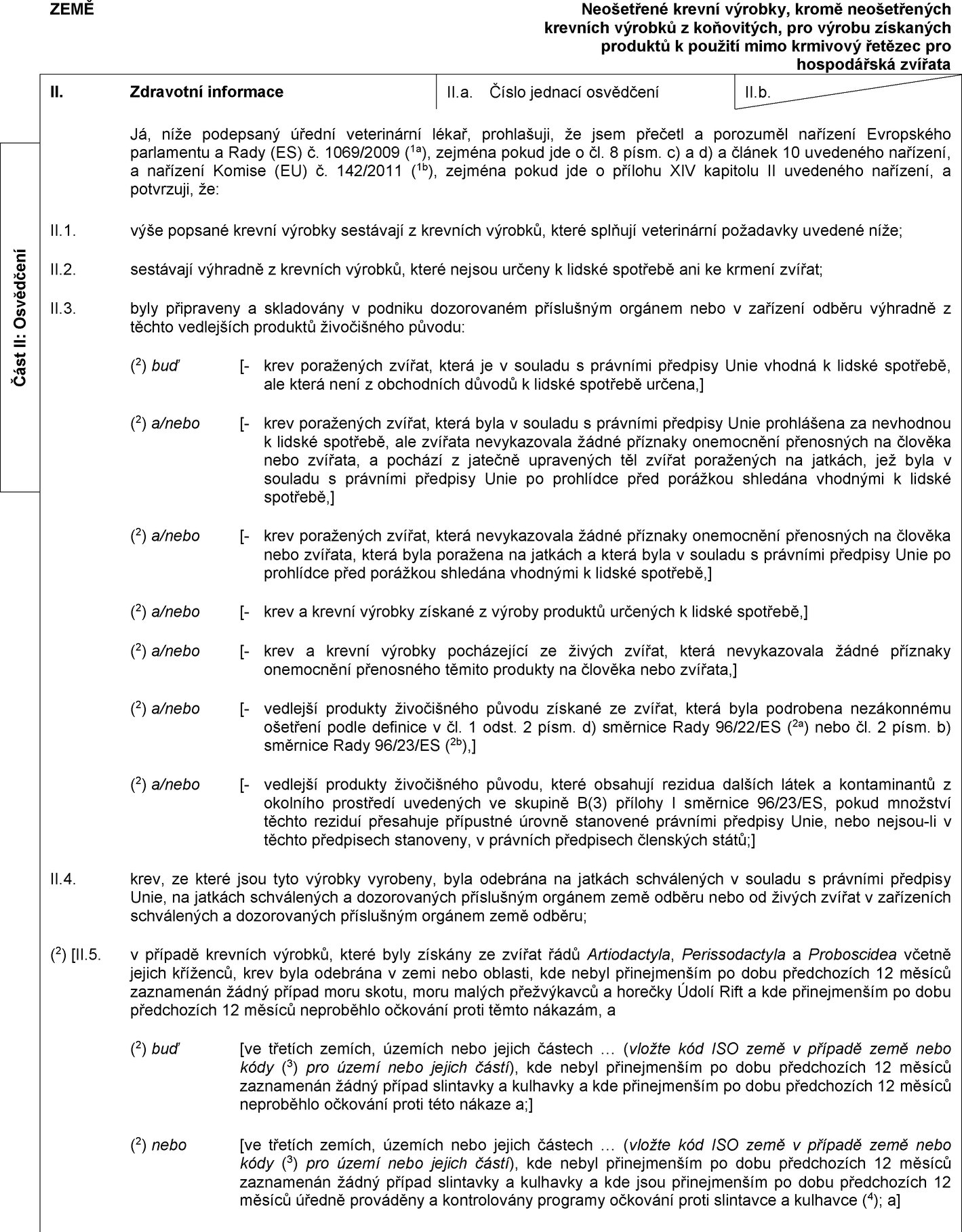 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
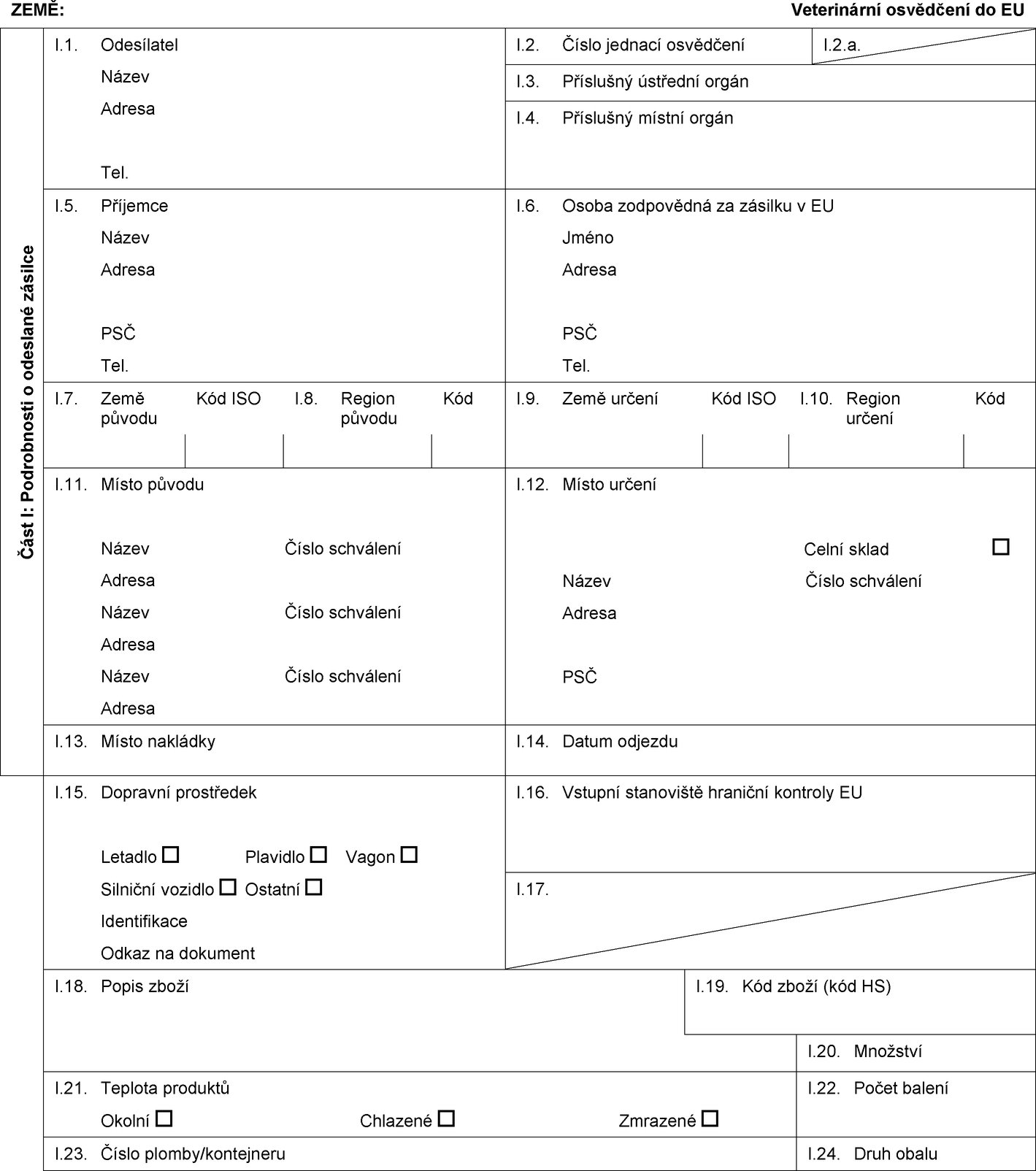 Text obrazu
Text obrazu
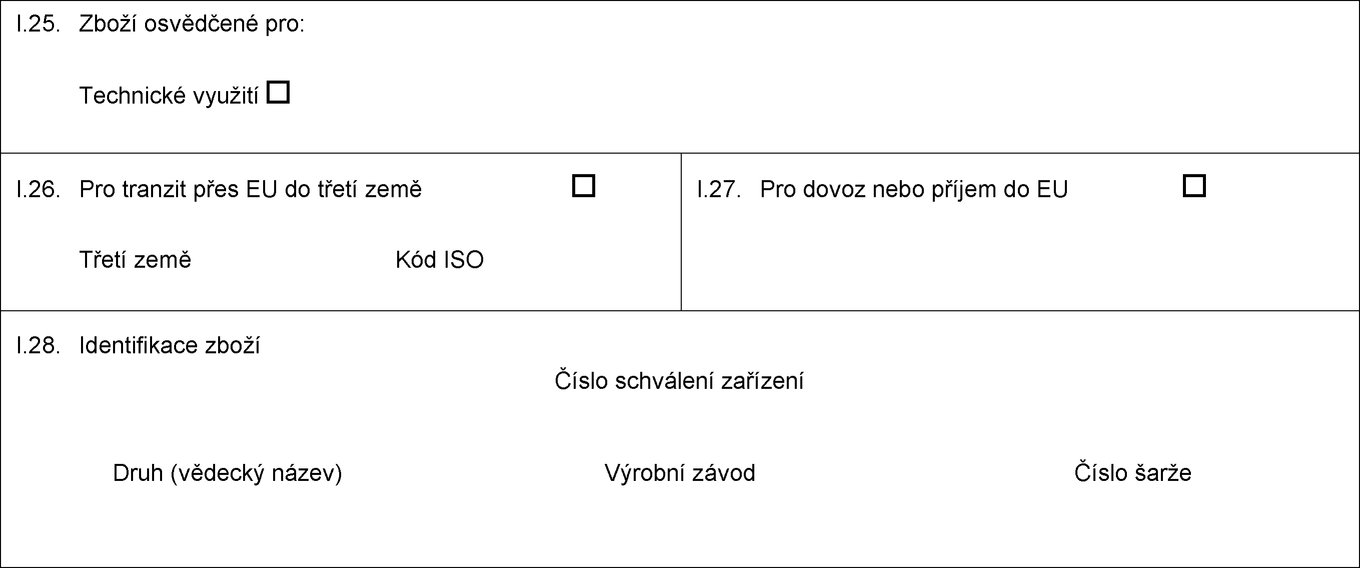 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
“
Text obrazu
“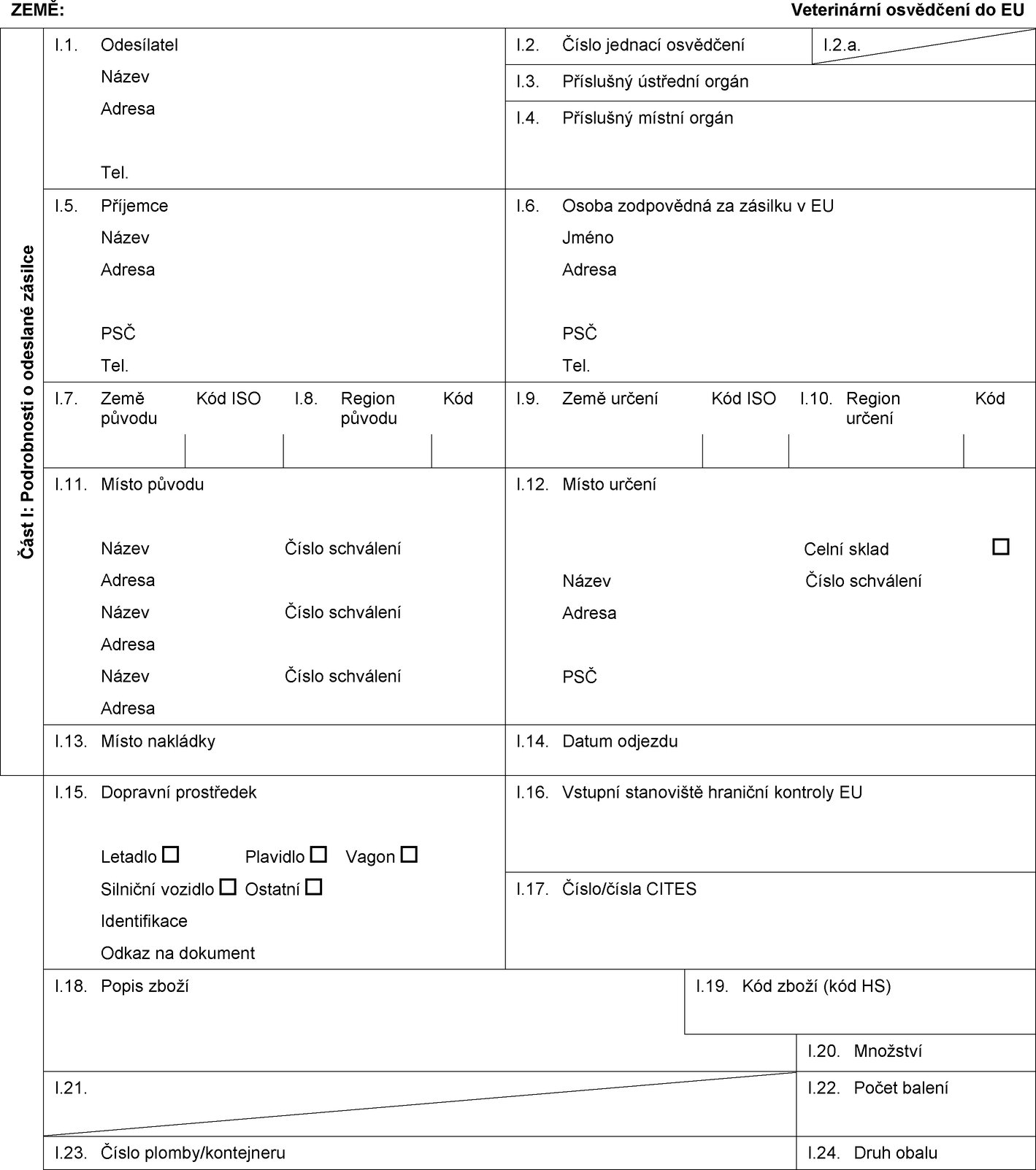 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
“
Text obrazu
“ Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
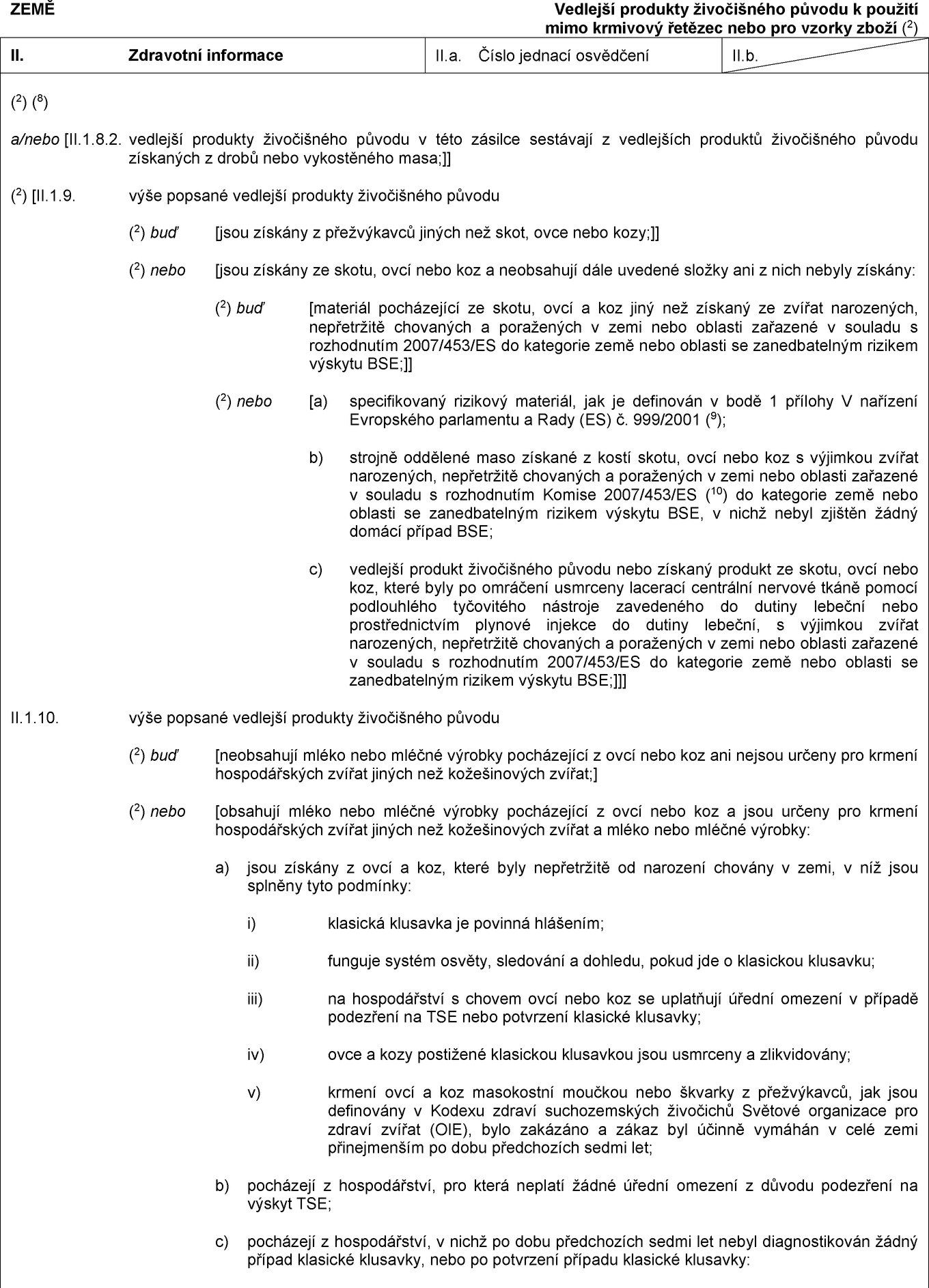 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
“
Text obrazu
“ Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
“
Text obrazu
“ Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
“
Text obrazu
“ Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
Text obrazu
 Text obrazu
“
Text obrazu
“