(EU) 2019/417Prováděcí rozhodnutí Komise (EU) 2019/417 ze dne 8. listopadu 2018, kterým se stanoví pokyny pro řízení systému Evropské unie pro rychlou výměnu informací „RAPEX“ zřízeného podle článku 12 směrnice 2001/95/ES o obecné bezpečnosti výrobků a jeho systému oznamování (oznámeno pod číslem C(2018) 7334)
| Publikováno: | Úř. věst. L 73, 15.3.2019, s. 121-187 | Druh předpisu: | Rozhodnutí |
| Přijato: | 8. listopadu 2018 | Autor předpisu: | Evropská komise |
| Platnost od: | 12. listopadu 2018 | Nabývá účinnosti: | 12. listopadu 2018 |
| Platnost předpisu: | Ano | Pozbývá platnosti: | |
Text předpisu s celou hlavičkou je dostupný pouze pro registrované uživatele.
PROVÁDĚCÍ ROZHODNUTÍ KOMISE (EU) 2019/417
ze dne 8. listopadu 2018,
kterým se stanoví pokyny pro řízení systému Evropské unie pro rychlou výměnu informací „RAPEX“ zřízeného podle článku 12 směrnice 2001/95/ES o obecné bezpečnosti výrobků a jeho systému oznamování
(oznámeno pod číslem C(2018) 7334)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na směrnici Evropského parlamentu a Rady 2001/95/ES ze dne 3. prosince 2001 o obecné bezpečnosti výrobků (1), a zejména na čl. 11 odst. 1 třetí pododstavec a bod 8 přílohy II uvedené směrnice,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 765/2008 ze dne 9. července 2008, kterým se stanoví požadavky na akreditaci a dozor nad trhem týkající se uvádění výrobků na trh a kterým se zrušuje nařízení (EHS) č. 339/93 (2),
po konzultaci s poradním výborem zřízeným článkem 15 směrnice 2001/95/ES,
vzhledem k těmto důvodům:
|
(1) |
Článkem 12 směrnice 2001/95/ES se zřizuje systém Evropské unie pro rychlou výměnu informací (dále jen „RAPEX“) mezi členskými státy a Komisí o opatřeních a akcích přijatých v souvislosti s výrobky, které představují vážné riziko pro zdraví a bezpečnost spotřebitelů. |
|
(2) |
V bodě 8 přílohy II směrnice 2001/95/ES se požaduje, aby byly pokyny pravidelně aktualizovány na základě nového vývoje a zkušeností. První a jedinou aktualizací pokynů bylo rozhodnutí Komise 2010/15/EU (3). |
|
(3) |
Vzhledem k novému vývoji a s cílem zajistit účinnější a efektivnější postupy oznamování v souladu s osvědčenými postupy je nutné tyto pokyny dále aktualizovat. |
|
(4) |
Terminologie a odkazy zastaraly, stejně jako způsoby komunikace mezi Komisí a orgány členských států i mezi samotnými orgány. |
|
(5) |
V pokynech se musí zohlednit nové nástroje, které byly v posledních letech vyvinuty pro řádné fungování systému RAPEX (wiki, rozhraní mezi systémem RAPEX a jinými systémy dozoru nad trhem). |
|
(6) |
Vzhledem k nejnovějšímu vývoji se kritéria oznamování v systému RAPEX stala nejasnými a je třeba je vyjasnit. |
|
(7) |
Přeshraniční prodej zboží on-line se zvýšil. Tento vývoj je třeba zohlednit v technikách oznamování i v nástrojích pro přijímání následných opatření. |
|
(8) |
Nařízením (ES) č. 765/2008 se používání systému RAPEX stanovené v článku 12 směrnice 2001/95/ES rozšiřuje také na výrobky, na které se vztahuje uvedený právní předpis. S rozšířením používání systému RAPEX vyvstaly určité otázky, které musí být v pokynech vyjasněny. |
|
(9) |
Nařízení (ES) č. 765/2008 se uplatňuje na spotřební výrobky a na profesionální výrobky, například určité zdravotnické prostředky. Uvedené nařízení se vztahuje také na širší oblast rizik, jiných než jsou rizika pro zdraví a bezpečnost spotřebitelů, například na bezpečnostní a environmentální rizika. Riziko se proto může týkat nejen spotřebitelů, ale také neurčité skupiny lidí označovaných jako „koneční uživatelé“. |
|
(10) |
Článek 22 nařízení (ES) č. 765/2008 stanoví, že opatření přijatá v souvislosti s výrobky, které představují vážné riziko pro zdraví a bezpečnost nebo jiné relevantní veřejné zájmy, by se měla oznamovat prostřednictvím systému RAPEX. |
|
(11) |
Směrnice 2001/95/ES a nařízení (ES) č. 765/2008 se vzájemně doplňují a vytvářejí systém pro zvýšení bezpečnosti nepotravinářských výrobků. |
|
(12) |
Systém RAPEX pomáhá zamezit a omezit dodávky výrobků představujících vážné riziko pro zdraví a bezpečnost, nebo v případě výrobků, na které se vztahuje nařízení (ES) č. 765/2008, také riziko pro jiné relevantní veřejné zájmy. Umožňuje Komisi sledovat účinnost a soudržnost dozoru nad trhem a kontrolních činností v členských státech. |
|
(13) |
Systém RAPEX je základem pro určování potřebných akcí na úrovni EU, zajišťuje důsledné vynucování požadavků EU na bezpečnost výrobků, a tím přispívá k řádnému fungování jednotného trhu. |
|
(14) |
Postup oznamování stanovený podle článku 11 směrnice 2001/95/ES stanoví výměnu informací mezi členskými státy a Komisí o opatřeních přijatých v souvislosti s výrobky, které představují nižší než vážné riziko pro zdraví a bezpečnost spotřebitelů. Pomáhá zajistit jednotnou a vysokou úroveň zdraví spotřebitelů a zachovat jednotný trh. |
|
(15) |
Článek 23 nařízení (ES) č. 765/2008 stanoví systém informační podpory, v jehož rámci členské státy poskytují Komisi informace požadované podle téhož článku o výrobcích, které představují nižší než vážné riziko. |
|
(16) |
Podle platných právních předpisů nejsou členské státy povinny tyto informace v systému RAPEX poskytovat. |
|
(17) |
Podle článku 16 směrnice o obecné bezpečnosti výrobků jsou členské státy a Komise povinny zpřístupnit veřejnosti informace o rizicích pro zdraví a bezpečnost spotřebitelů představovaných výrobky. |
|
(18) |
V zájmu zajištění soudržného systému informací o výrobcích představujících riziko pro zdraví a bezpečnost spotřebitelů, nebo v případě výrobků, na které se vztahuje nařízení (ES) č. 765/2008, také pro jiné relevantní veřejné zájmy by bylo žádoucí, aby byly dostupné informace týkající se nebezpečných výrobků, na které se vztahuje článek 23 nařízení (ES) č. 765/2008, zpřístupněny v systému RAPEX. |
|
(19) |
S cílem umožnit fungování systému RAPEX by se měly vypracovat pokyny k různým aspektům těchto postupů oznamování, a zejména by se měl stanovit obsah oznámení. Pokyny by měly zahrnovat informace, které by oznámení měla obsahovat, kritéria pro oznamování rizik, která nepřesahují nebo nemohou přesáhnout hranice daného členského státu, a kritéria pro klasifikaci oznámení podle stupně naléhavosti. V pokynech by se měly rovněž stanovit pracovní postupy, včetně lhůt pro jednotlivé kroky postupů oznamování a následných oznámení, jakož i pravidla týkající se důvěrnosti. |
|
(20) |
Aby se zajistilo řádné uplatňování postupů oznamování, měly by pokyny stanovit také metody posuzování rizik s kritérii pro určení rizik, přičemž by se mělo přihlédnout také k řízení rizik. |
|
(21) |
Vzhledem k bodu 2 přílohy II směrnice 2001/95/ES obsahují nové pokyny soubor pokynů týkajících se posuzování rizik spojených se spotřebitelskými výrobky a týkají se rovněž profesionálních výrobků, přičemž stanoví kritéria pro identifikaci vážných rizik. |
|
(22) |
Tyto pokyny by měly být určeny všem orgánům členských států, které jsou podle směrnice 2001/95/ES a nařízení (ES) č. 765/2008 zapojeny do sítě RAPEX, včetně orgánů dozoru nad trhem odpovědných za sledování souladu těchto výrobků s příslušnými požadavky na bezpečnost a orgánů provádějících kontroly na vnějších hranicích, |
PŘIJALA TOTO ROZHODNUTÍ:
Článek 1
Pokyny pro řízení systému Evropské unie pro rychlou výměnu informací „RAPEX“ zřízeného podle článku 12 směrnice 2001/95/ES a jeho systému oznamování jsou stanoveny v příloze tohoto rozhodnutí.
Článek 2
Rozhodnutí 2010/15/EU se zrušuje.
Článek 3
Toto rozhodnutí je určeno členským státům.
V Bruselu dne 8. listopadu 2018.
Za Komisi
Věra JOUROVÁ
členka Komise
(1) Úř. věst. L 11, 15.1.2002, s. 4.
(2) Úř. věst. L 218, 13.8.2008, s. 30.
(3) Rozhodnutí Komise 2010/15/EU ze dne 16. prosince 2009, kterým se stanoví pokyny pro řízení systému Společenství pro rychlou výměnu informací RAPEX zřízeného podle článku 12 a pro postup oznamování stanovený podle článku 11 směrnice 2001/95/ES (směrnice o obecné bezpečnosti výrobků) (Úř. věst. L 22, 26.1.2010, s. 1)
PŘÍLOHA
POKYNY PRO ŘÍZENÍ SYSTÉMU EVROPSKÉ UNIE PRO RYCHLOU VÝMĚNU INFORMACÍ „RAPEX“ ZŘÍZENÉHO PODLE ČLÁNKU 12 SMĚRNICE 2001/95/ES (SMĚRNICE O OBECNÉ BEZPEČNOSTI VÝROBKŮ) A JEHO SYSTÉMU OZNAMOVÁNÍ
ČÁST I
OBLAST PŮSOBNOSTI A URČENÍ POKYNŮ
1 Oblast působnosti, cíle a aktualizace
1.1 Oblast působnosti
Komise (1) na základě čl. 11 odst. 1 a bodu 8 přílohy II směrnice 2001/95/ES přijímá Pokyny pro řízení systému Evropské unie pro rychlou výměnu informací „RAPEX“ zřízeného podle článku 12 směrnice 2001/95/ES o obecné bezpečnosti výrobků (dále jen „pokyny“). Komisi je nápomocen poradní výbor složený ze zástupců členských států EU a zřízený podle čl. 15 odst. 3 uvedené směrnice.
Bod 8 přílohy II směrnice o obecné bezpečnosti výrobků zní takto: „V souladu s postupem stanoveným v čl. 15 odst. 3 Komise vypracuje a pravidelně aktualizuje pokyny pro řízení systému RAPEX Komisí a členskými státy.“
Článek 11 směrnice o obecné bezpečnosti výrobků stanoví, že členské státy informují Komisi o přijatých opatřeních, kterými omezí uvádění výrobků na trh nebo nařídí jejich stažení nebo odvolání, pokud tyto informace nesplňují požadavky na typ oznámení podle článku 12 směrnice o obecné bezpečnosti výrobků nebo na jiné oznámení podle jiných specifických právních předpisů Společenství.
Článek 22 nařízení (ES) č. 765/2008, stanoví, že pokud členský stát přijme nebo se chystá přijmout opatření, která brání, omezují nebo stanoví zvláštní podmínky pro uvádění na trh a používání výrobků, které představují vážné riziko pro zdraví, bezpečnost nebo jiné relevantní veřejné zájmy konečných uživatelů, okamžitě musí tato opatření oznámit Komisi za použití systému RAPEX.
Článek 23 nařízení (ES) č. 765/2008 stanoví, že členské státy musí Komisi poskytnout informace, které mají k dispozici a které dosud neposkytly podle článku 22, o výrobcích, které představují (nižší než vážné) riziko.
Podle článku 16 směrnice o obecné bezpečnosti výrobků jsou členské státy a Komise povinny zpřístupnit veřejnosti informace o rizicích pro zdraví a bezpečnost spotřebitelů představovaných výrobky. Bylo by proto vhodné, aby byly všechny informace o opatřeních přijatých proti výrobkům představujícím riziko, pokud jde o bezpečnost výrobků, obsaženy v systému, který slouží tomuto účelu. Členské státy se tudíž vyzývají, aby v systému RAPEX předložily všechna opatření přijatá proti výrobkům představujícím riziko a spadajícím do oblasti působnosti směrnice o obecné bezpečnosti výrobků nebo nařízení (ES) č. 765/2008. Tyto informace se mohou vkládat přímo do systému RAPEX. V případě, že musí být informace oznámeny do jiného systému pro výměnu informací podle nařízení (ES) č. 765/2008 (2), mohou členské státy vygenerovat oznámení v systému RAPEX v rámci uvedeného systému (viz část II kapitoly 1.2 písm. h) a 2.2 těchto pokynů).
Zatímco směrnice o obecné bezpečnosti výrobků se vztahuje pouze na spotřební výrobky představující riziko pro zdraví a bezpečnost spotřebitelů, nařízení (ES) č. 765/2008 se uplatňuje na spotřební výrobky, ale také na profesionální výrobky, na které se vztahují harmonizační právní předpisy EU (např. určité zdravotnické prostředky a lodní výstroj). Vztahuje se také na širší oblast rizik, jiných než jsou rizika pro zdraví a bezpečnost spotřebitelů, například na bezpečnostní a environmentální rizika. Riziko se proto může týkat nejen spotřebitelů, ale také – pokud se použije nařízení (ES) č. 765/2008 – jiných „konečných uživatelů“.
Pokyny pro posuzování rizik uvedené v části III dodatku 6 jsou nedílnou součástí pokynů k systému RAPEX. Jsou nástrojem, který umožňuje určit úroveň rizika výrobku, a proto pomáhá identifikovat opatření, která mají být přijata.
Pokyny pro posuzování rizik uvádějí úroveň rizika i zranění, která může daný výrobek způsobit. Posouzení rizik u jednotlivých výrobků musí být provázeno řádným řízením rizik. Například úroveň rizika u závadného elektrického spotřebiče pro domácnost, který představuje riziko požáru, může být jen „nízká“, což znamená, že pravděpodobnost, že jediný spotřebič způsobí během své životnosti smrtelný požár, je menší než jedna ku milionu. Pokud však byly na trh uvedeny miliony závadných spotřebičů, téměř nevyhnutelně dojde ke smrtelným požárům, pokud nebudou přijata vhodná opatření.
Do systému jsou podle pravidel stanovených ve směrnici o obecné bezpečnosti výrobků a v těchto pokynech (3) zapojeny členské státy (4), kandidátské země, země, které jsou stranami Evropského hospodářského prostoru (EHP), jakož i další třetí země a mezinárodní organizace, které mají přístup k systému RAPEX (za podmínek stanovených v čl. 12 odst. 4 směrnice o obecné bezpečnosti výrobků).
1.2 Cíle
Pokyny mají tyto cíle:
|
a) |
zjednodušit průběh oznamovacích postupů; |
|
b) |
stanovit kritéria oznamování u oznamovacích postupů; |
|
c) |
definovat obsah oznámení a následných oznámení zaslaných v rámci oznamovacího postupu, zejména jaké údaje se požadují a jaké formuláře se mají použít; |
|
d) |
stanovit následné činnosti, které mají členské státy po obdržení oznámení provést, a druh informací, které mají poskytnout; |
|
e) |
popsat, jakým způsobem Komise nakládá s oznámeními a následnými oznámeními; |
|
f) |
stanovit lhůty pro různé druhy akcí prováděných v rámci oznamovacích postupů; |
|
g) |
stanovit praktická a technická opatření, která Komise a členské státy potřebují k účinnému a efektivnímu používání oznamovacích postupů, a |
|
h) |
stanovit metody posuzování rizik a zejména kritéria pro určování vážných rizik. |
1.3 Aktualizace
V souladu s poradním postupem bude Komise pokyny pravidelně aktualizovat na základě nového vývoje a zkušeností v oblasti bezpečnosti výrobků.
2 Určení pokynů
Tyto pokyny jsou určeny všem orgánům členských států, které jsou činné v oblasti bezpečnosti výrobků a které jsou zapojené do sítě RAPEX, včetně orgánů dozoru nad trhem odpovědných za sledování souladu těchto výrobků s příslušnými požadavky na bezpečnost a orgánů provádějících kontroly na vnějších hranicích.
3 Výrobky
3.1 Výrobky, na které se vztahují tyto pokyny
Tyto pokyny se vztahují na dva soubory výrobků: na výrobky, na které se vztahuje směrnice o obecné bezpečnosti výrobků, a výrobky, na které se vztahuje nařízení (ES) č. 765/2008.
3.1.1 Výrobky, na které se vztahuje směrnice o obecné bezpečnosti výrobků
Podle čl. 2 písm. a) směrnice o obecné bezpečnosti výrobků jsou spotřebními výrobky pro účely těchto pokynů:
a) „výrobky určené pro spotřebitele“– tedy výrobky, které jsou vyvinuté a vyráběné pro spotřebitele a které jim jsou dány k dispozici,
b) „migrující výrobky“ (5) – tedy výrobky, které jsou vyvinuté a vyráběné pro odborníky, nicméně za rozumně předvídatelných podmínek budou pravděpodobně používány také spotřebiteli. Jedná se o výrobky vyráběné pro odborníky, jež jsou dány k dispozici spotřebitelům, kteří je mohou zakoupit a používat, aniž by k tomu potřebovali nějaké zvláštní znalosti nebo školení, např. elektrická vrtačka, úhlová bruska nebo stolní okružní pila, jež byly vyvinuté a vyráběné pro odborníky, nicméně se rovněž dodávají na spotřební trh (tj. spotřebitelé si je mohou zakoupit v obchodech a používat je bez zvláštního školení).
Výrobky určené pro spotřebitele i migrující výrobky lze spotřebitelům poskytnout zdarma, prodat jim je nebo poskytnout v souvislosti se službou. Systém RAPEX se vztahuje na všechny tyto tři možnosti.
Podle čl. 2 písm. a) směrnice o obecné bezpečnosti výrobků se za výrobky poskytované v souvislosti s určitou službou považují např.:
|
a) |
výrobky dodávané spotřebitelům, které si spotřebitelé odnesou a používají mimo provozovnu poskytovatele služeb, jako jsou automobily a stroje na sečení trávy pronajaté v půjčovnách a tetovací inkousty a implantáty (které nejsou klasifikovány jako zdravotnické prostředky), jež poskytovatel služby implantoval spotřebiteli pod kůži, |
|
b) |
výrobky používané v provozovně poskytovatele služeb, pokud je spotřebitelé sami aktivně obsluhují (např. zapnou stroj, mají možnost ho vypnout a ovlivnit jeho chod změnou polohy nebo intenzity během jeho používání). Příkladem takových výrobků jsou solární lehátka v soláriích a posilovnách. Spotřebitelé musejí výrobky používat aktivním způsobem a musejí je do značné míry ovládat. Pouhé pasivní používání, jako je použití šamponu osobou, jíž umývá vlasy kadeřník, nebo používání autobusu cestujícími, se nepovažuje za používání výrobků spotřebiteli. |
3.1.2 Výrobky, na které se vztahuje nařízení (ES) č. 765/2008
Podle nařízení (ES) č. 765/2008 se za výrobky pro účely systému RAPEX považují výrobky, které spadají do oblasti působnosti článku 15 uvedeného nařízení a pro které platí definice v něm obsažené bez ohledu na to, zda jsou určeny spotřebitelům nebo profesionálním uživatelům.
3.2 Výrobky, na které se tyto pokyny nevztahují
Tyto pokyny se nevztahují na:
|
a) |
výrobky, na něž se vztahují zvláštní rovnocenné oznamovací postupy stanovené jinými právními předpisy EU, zejména:
|
|
b) |
Výrobky, na které se nevztahuje definice „výrobku“ uvedená v čl. 2 písm. a) směrnice o obecné bezpečnosti výrobků, zejména:
|
|
c) |
výrobky, které nespadají pod definici výrobku podle čl. 15 odst. 4 nařízení (ES) č. 765/2008. |
4 Opatření
4.1 Druhy opatření
Preventivní a omezující opatření lze v souvislosti s výrobky představujícími riziko přijmout buď z podnětu hospodářského subjektu, který výrobek umístil na trh a/nebo ho na trhu distribuoval (dále jen „dobrovolná opatření“), nebo z příkazu orgánu členského státu, který je příslušný ke sledování souladu výrobků s požadavky na bezpečnost (dále jen „povinná opatření“).
Pro účely těchto pokynů se povinná a dobrovolná opatření definují takto:
a) povinná opatření: opatření, která orgány členských států přijaly nebo se rozhodly přijmout, často ve formě správního rozhodnutí, a která hospodářské subjekty zavazují k provedení preventivní, nápravné nebo omezující akce v souvislosti s konkrétním výrobkem, který dodaly na trh;
b) dobrovolná opatření:
|
i) |
preventivní a omezující opatření, která hospodářský subjekt přijal dobrovolně, tj. aniž by některý orgán členského státu musel zasáhnout, |
|
ii) |
doporučení a dohody s hospodářskými subjekty, které při své činnosti uzavřely orgány členských států. Patří mezi ně dohody, které nemají písemnou podobu a jejichž výsledkem je preventivní nebo omezující akce, kterou při své činnosti hospodářské subjekty provedou v souvislosti s výrobky představujícími vážné riziko, jež dodaly na trh. |
4.2 Kategorie opatření
Ustanovení čl. 8 odst. 1 písm. b) až f) směrnice o obecné bezpečnosti výrobků uvádí seznam různých kategorií opatření, která podléhají oznamovací povinnosti v systému RAPEX, pokud jsou splněny podmínky pro oznámení, včetně těchto opatření:
|
a) |
označit výrobek příslušným upozorněním na riziko, které může přestavovat; |
|
b) |
podmínit uvedení výrobku na trh stanovením předchozích podmínek; |
|
c) |
upozornit spotřebitele a konečné uživatele na riziko, které může výrobek představovat; |
|
d) |
dočasný zákaz dodávání, nabízení k dodání a vystavování výrobku; |
|
e) |
zákaz uvádění výrobku na trh a další doprovodná opatření, tj. opatření požadovaná k zajištění souladu se zákazem; |
|
f) |
stažení výrobku z trhu; |
|
g) |
zpětné převzetí výrobku od spotřebitelů; |
|
h) |
zničení výrobku, který byl stažen z trhu nebo převzat zpět od zákazníka. |
Pro účely systému RAPEX se výraz „stažení“ používá výhradně pro opatření k zabránění distribuce, vystavování nebo nabízení výrobku, který představuje riziko pro spotřebitele nebo jiné konečné uživatele, zatímco výraz „zpětné převzetí“ se používá pouze pro opatření k dosažení vrácení takového výrobku, který výrobce nebo distributor již dodal nebo poskytnul spotřebitelům nebo jiným konečným uživatelům.
4.3 Požadavky ohledně opatření
Podle čl. 12 odst. 1 směrnice o obecné bezpečnosti výrobků a článku 22 nařízení (ES) č. 765/2008 se u vážných rizik v systému RAPEX oznamují povinná i dobrovolná opatření.
Preventivní a omezující opatření, která hospodářský subjekt přijal dobrovolně, tj. aniž by některý orgán členského státu musel zasáhnout, která se týkají výrobku představujícího vážné riziko a související preventivní nebo omezující opatření přijatá z podnětu hospodářského subjektu je třeba neprodleně oznámit příslušným orgánům členského státu, jak je uvedeno v čl. 5 odst. 3 směrnice o obecné bezpečnosti výrobků a v čl. 22 odst. 2 a 3 nařízení (ES) č. 765/2008.
Všechny kategorie preventivních a omezujících opatření přijatých v souvislosti s uváděním na trh a používáním spotřebních výrobků, které představují vážné riziko pro zdraví a bezpečnost spotřebitelů, nebo v případě výrobků, které představují vážné riziko pro zdraví, bezpečnost nebo jiné relevantní veřejné zájmy konečných uživatelů a na které se vztahuje nařízení (ES) č. 765/2008, podléhají oznamovací povinnosti v systému RAPEX.
4.4 Vyloučení obecně platných povinných opatření
Komisi by se prostřednictvím aplikace RAPEX neměly oznamovat obecně platné zákony přijaté na vnitrostátní úrovni s cílem zabránit nebo omezit uvádění na trh a používání obecně popsaných kategorií spotřebních výrobků z toho důvodu, že představují vážné riziko pro zdraví a bezpečnost spotřebitelů. Všechna taková vnitrostátní opatření, která platí pouze pro obecně definované kategorie výrobků, např. pro všechny výrobky obecně nebo pro všechny výrobky, které slouží stejnému účelu, nikoli však pro výrobky či kategorie výrobků konkrétně identifikovatelné podle značky, zvláštního vzhledu, výrobce, obchodníka, názvu modelu nebo čísla atd., se Komisi oznamují podle směrnice Evropského parlamentu a Rady 2015/1535/EU (11).
5 Úrovně rizika
5.1 Vážné riziko
Než se orgán členského státu rozhodne předložit oznámení v systému RAPEX, vždy provede příslušné posouzení rizik (viz část III dodatek 6 těchto pokynů nebo doplňková obecná metodika EU pro posuzování rizik u výrobků, na které se vztahuje nařízení (ES) č. 765/2008 (12)) a stanoví, zda oznamovaný výrobek představuje vážné riziko pro zdraví a bezpečnost spotřebitelů, nebo v případě výrobků, na které se vztahuje nařízení (ES) č. 765/2008, vážné riziko pro zdraví, bezpečnost nebo jiné relevantní veřejné zájmy (např. bezpečnost nebo životní prostředí) konečných uživatelů, a zda je tudíž splněno jedno z kritérií oznamování v systému RAPEX.
5.2 Nižší než vážné riziko
Oznámení zasílaná v souladu s článkem 11 směrnice o obecné bezpečnosti výrobků nebo článkem 23 nařízení (ES) č. 765/2008 se obecně považují za oznámení výrobků představujících nižší než vážné riziko. Oznámení těchto výrobků, na rozdíl od oznámení výrobků představujících vážné riziko, nemusí nutně znamenat povinnost pro další členské státy provést následné činnosti, ledaže si to vyžádá povaha výrobku nebo riziko (viz část II kapitola 3.4.6.1).
5.3 Metoda posuzování rizika
V části III dodatku 6 těchto pokynů se stanoví metoda posuzování rizika, kterou mohou orgány členských států používat k posouzení výše rizika, jež představují spotřební výrobky pro zdraví a bezpečnost spotřebitelů, a k rozhodnutí, zda je nutné předložit oznámení v systému RAPEX. Stejně tak může být nutné prostudovat obecnou metodiku EU pro doplňkové posuzování rizik, jak je uvedeno v kapitole 5.1, v případě, kdy se na dotčený výrobek vztahuje nařízení (ES) č. 765/2008.
Pro provedení posouzení rizik je na internetové stránce RAPEX a v aplikaci RAPEX k dispozici zvláštní nástroj („RAG“ čili Pokyny pro posuzování rizik (13)), který zohledňuje zásady stanovené v dodatku 6.
5.4 Orgán posuzující riziko
Posuzování rizik vždy provádí nebo kontroluje orgán členského státu, který provedl šetření a přijal příslušná opatření nebo který sledoval dobrovolné akce, jež v souvislosti s nebezpečným výrobkem provedl hospodářský subjekt.
Všechny nejasnosti pak kontaktní místo RAPEX (viz část II kapitola 5.1) řeší s odpovědným orgánem před předáním oznámení prostřednictvím aplikace RAPEX.
6 Přeshraniční účinky
6.1 Mezinárodní událost
Podle článku 12 směrnice o obecné bezpečnosti výrobků a článku 22 nařízení (ES) č. 765/2008 předkládá členský stát oznámení v systému RAPEX pouze v případě, kdy usoudí, že účinky rizik, která představuje výrobek, přesahují nebo mohou přesáhnout jeho území (dále jen „přeshraniční účinky“ nebo „mezinárodní událost“).
Vzhledem k volnému pohybu výrobků na vnitřním trhu a ke skutečnosti, že se výrobky do EU dovážejí různými distribučními kanály a že spotřebitelé kupují výrobky při pobytu v zahraničí a prostřednictvím internetu, se vnitrostátním orgánům doporučuje, aby si kritérium přeshraničních účinků vykládaly poměrně široce. Oznámení podle článku 12 směrnice o obecné bezpečnosti výrobků nebo článku 22 nařízení (ES) č. 765/2008 se proto předkládá v případě, že:
|
a) |
nelze vyloučit, že nebezpečný výrobek byl prodán ve více než jednom členském státě EU, nebo |
|
b) |
nelze vyloučit, že nebezpečný výrobek byl prodán prostřednictvím internetu, nebo |
|
c) |
výrobek pochází ze třetí země a je pravděpodobné, že byl do EU dovezen několika distribučními kanály. |
6.2 Místní událost
Opatření přijatá v souvislosti s výrobkem představujícím vážné riziko, která mohou mít pouze místní účinky (dále jen „místní událost“), se podle článku 12 směrnice o obecné bezpečnosti výrobků neoznamují. To platí v situacích, kdy orgán členského státu má konkrétní a silný důvod vyloučit možnost, že dotčený výrobek byl nebo bude dán (jakýmikoli prostředky) k dispozici v jiných členských státech, např. opatření přijatá v souvislosti s místním výrobkem, který se vyrábí a distribuuje pouze v jednom členském státě. Orgány členského státu musí ve svém posouzení pečlivě zohlednit možnost, že by výrobek mohl být prodáván on-line nebo prostřednictvím nově vznikajících distribučních kanálů.
Oznámení týkající se výrobku představujícího vážné riziko v případě místní události se Komisi předkládá pouze v těch případech, že obsahuje informace, které by z hlediska bezpečnosti výrobku mohly zajímat i ostatní členské státy, a zejména pokud je reakcí na nový druh rizika, který zatím nebyl oznámen, nový druh rizika vyplývající z kombinace výrobků nebo nový druh nebo novou kategorii výrobků.
Takové oznámení se předkládá podle článku 11 s odkazem na čl. 11 odst. 1 druhý pododstavec směrnice o obecné bezpečnosti výrobků.
ČÁST II
SYSTÉM EU PRO RYCHLOU VÝMĚNU INFORMACÍ „RAPEX“ ZŘÍZENÝ PODLE ČLÁNKU 12 SMĚRNICE O OBECNÉ BEZPEČNOSTI VÝROBKŮ
1 Úvod
1.1 Cíle systému RAPEX
Článkem 12 směrnice o obecné bezpečnosti výrobků se zřizuje systém EU pro rychlou výměnu informací („RAPEX“).
RAPEX hraje významnou úlohu v oblasti bezpečnosti výrobků. Doplňuje jiné akce provedené na vnitrostátní i unijní úrovni s cílem zajistit vysokou úroveň bezpečnosti výrobků v EU.
Údaje systému RAPEX pomáhají:
|
a) |
zamezit a omezit dodávky nebezpečných výrobků; |
|
b) |
sledovat účinnost a soudržnost dozoru nad trhem a kontrolních činností, které provádějí orgány členských států; |
|
c) |
určovat potřeby a vytvářet základ pro akce na úrovni EU a |
|
d) |
důsledně vynucovat požadavky EU na bezpečnost výrobků, a tím přispívat k řádnému fungování jednotného trhu. |
1.2 Součásti systému RAPEX
Systém RAPEX se skládá z několika vzájemně se doplňujících součástí, které mají klíčový význam pro jeho efektivní a účinné fungování. K nejdůležitějším součástem patří:
|
a) |
právní rámec, který reguluje fungování systému (tj. směrnice o obecné bezpečnosti výrobků a pokyny); |
|
b) |
on-line aplikace (dále jen „aplikace RAPEX“), která členským státům a Komisi umožňuje rychlou výměnu informací prostřednictvím internetové platformy; |
|
c) |
síť kontaktních míst systému RAPEX, kterou tvoří jednotná kontaktní místa RAPEX odpovědná za provozování systému RAPEX ve všech členských státech (viz část II kapitola 5.1); |
|
d) |
vnitrostátní sítě systému RAPEX zřízené ve všech členských státech, které zahrnují kontaktní místo systému RAPEX (viz část II kapitola 5.1) a všechny příslušné orgány, jež se zabývají bezpečností výrobků; |
|
e) |
tým odpovědný za systém RAPEX zřízený v rámci útvaru Komise odpovědného za provádění směrnice o obecné bezpečnosti výrobků, který zkoumá a potvrzuje dokumenty předkládané prostřednictvím aplikace RAPEX a udržuje a zajišťuje jeho správné fungování; |
|
f) |
internetové stránky systému RAPEX (14), kde jsou zveřejněny souhrny oznámení v systému RAPEX i týdenní aktualizace; |
|
g) |
publikace související se systémem RAPEX, jako jsou statistiky, výroční zprávy a další propagační materiály, a |
|
h) |
rozhraní mezi systémem RAPEX a systémem ICSMS, které spočívá v propojení obou systémů, které usnadňuje kódování oznámení v systému RAPEX na základě údajů z šetření, které jsou již k dispozici v systému ICSMS. Vyplněním příslušných kolonek v systému ICSMS může být automaticky podáno oznámení v systému RAPEX. |
2 Kritéria oznamování
Systém RAPEX se týká opatření, která brání, omezují nebo stanoví zvláštní podmínky pro uvádění na trh a používání výrobků, které představují vážné riziko pro zdraví a bezpečnost spotřebitelů, nebo v případě výrobků, na které se vztahuje nařízení (ES) č. 765/2008, opatření, která brání, omezují nebo stanoví zvláštní podmínky pro uvádění na trh a používání výrobků, které představují vážné riziko pro zdraví, bezpečnost nebo jiné relevantní veřejné zájmy (např. bezpečnost nebo životní prostředí) konečných uživatelů.
2.1 Povinná účast v systému RAPEX: článek 12 směrnice o obecné bezpečnosti výrobků a článek 22 nařízení (ES) č. 765/2008
Podle směrnice o obecné bezpečnosti výrobků a nařízení (ES) č. 765/2008 je účast členských států v systému RAPEX povinná. Podle článku 12 směrnice o obecné bezpečnosti výrobků a článku 22 nařízení (ES) č. 765/2008 mají členské státy zákonnou povinnost oznámit Komisi povinná i dobrovolná opatření, pokud jsou splněna tato čtyři kritéria oznamování:
|
a) |
výrobek spadá do oblasti působnosti směrnice o obecné bezpečnosti výrobků nebo nařízení (ES) č. 765/2008; |
|
b) |
na výrobek se vztahují opatření, která jeho uvádění na trh nebo používání brání, omezují nebo pro ně stanoví zvláštní podmínky (dále jen „preventivní a omezující opatření“); |
|
c) |
výrobek představuje vážné riziko pro zdraví a bezpečnost spotřebitelů, nebo v případě výrobků, na které se vztahuje nařízení (ES) č. 765/2008, také pro jiné relevantní veřejné zájmy konečných uživatelů; |
|
d) |
nelze vyloučit, že účinek vážného rizika pro zdraví a bezpečnost spotřebitelů, nebo v případě výrobků, na které se vztahuje nařízení (ES) č. 765/2008, také pro jiné relevantní veřejné zájmy konečných uživatelů, přesahuje hranice oznamujícího členského státu. |
2.2 Nepovinná účast v systému RAPEX: článek 11 směrnice o obecné bezpečnosti výrobků a článek 23 nařízení (ES) č. 765/2008
Článek 11 směrnice o obecné bezpečnosti výrobků stanoví, že členské státy uvědomí Komisi o přijatých opatřeních, kterými omezí uvádění výrobků na trh nebo nařídí jejich stažení nebo odvolání, pokud tyto informace nesplňují požadavky na oznámení podle článku 12 nebo na jiné oznámení podle jiných specifických právních předpisů Společenství.
V zájmu zjednodušení a efektivnosti mohou členské státy využívat aplikaci RAPEX také k oznamování opatření přijatých v souvislosti s výrobky, na které se nevztahuje podávání oznámení podle článku 12 za podmínek v něm uvedených.
Členské státy mají zákonnou povinnost zaslat Komisi oznámení podle článku 11 směrnice o obecné bezpečnosti výrobků, pokud jsou splněna tato čtyři kritéria oznamování:
|
a) |
dotčený výrobek je určený spotřebitelům; |
|
b) |
platí pro něj omezující opatření přijatá vnitrostátními orgány (povinná opatření); |
|
c) |
představuje nižší než vážné riziko pro zdraví a bezpečnost spotřebitelů, jehož účinky mohou přesáhnout či přesahují území jednoho členského státu, nebo představuje vážné riziko pro zdraví a bezpečnost spotřebitelů, jehož účinky nepřesahují či nemohou přesáhnout jeho území, ale přijatá opatření obsahují informace, které pravděpodobně budou z hlediska bezpečnosti výrobku ostatní členské státy zajímat (15); |
|
d) |
Přijatá opatření se neoznamují žádným jiným postupem oznamování stanoveným právními předpisy EU. |
Bez ohledu na skutečnost, že článek 11 směrnice o obecné bezpečnosti výrobků neobsahuje výslovnou povinnost oznamovat dobrovolná opatření přijatá v souvislosti s výrobky, které představují nižší než vážné riziko, podle článku 16 směrnice o obecné bezpečnosti výrobků jsou členské státy a Komise povinny zpřístupnit veřejnosti informace o rizicích pro zdraví a bezpečnost spotřebitelů. V zájmu soudržnosti systému oznamování a účinného plnění povinností, které podle článku 16 směrnice o obecné bezpečnosti výrobků mají členské státy a Komise, se proto členským státům doporučuje, aby v systému RAPEX oznamovaly také dobrovolná opatření přijatá výrobci a distributory v souvislosti s výrobky, které představují nižší než vážné riziko.
Podle článku 23 nařízení (ES) č. 765/2008 členské státy poskytnou Komisi informace, které mají k dispozici a které dosud neposkytly podle článku 22, o výrobcích, které představují (nižší než vážné) riziko. Na rozdíl od článku 22 tohoto nařízení neukládá článek 23 členským státům povinnost předkládat oznámení s těmito informacemi v systému RAPEX. Podle článku 16 směrnice o obecné bezpečnosti výrobků však Komise a členské státy musí informace o rizicích, která může výrobek představovat pro zdraví a bezpečnost spotřebitelů, zveřejnit. V zájmu soudržnosti a s cílem účinně splnit povinnosti obsažené v článku 16 směrnice o obecné bezpečnosti výrobků by nejpragmatičtějším řešením bylo, aby systém RAPEX obsahoval všechna opatření přijatá v souvislosti s výrobky, které představují vážné a nižší než vážné riziko pro zdraví a bezpečnost spotřebitelů, a to jak u výrobků, na které se vztahuje směrnice o obecné bezpečnosti výrobků, tak u výrobků, na které se vztahuje nařízení (ES) č. 765/2008, přičemž v druhém případě by se jednalo také o rizika pro jiné relevantní veřejné zájmy konečných uživatelů. Proto se doporučuje, aby členské státy, když přijmou opatření a předloží je prostřednictvím systém ICSMS podle článku 23 nařízení (ES) č. 765/2008, oznámily tyto informace také v systému RAPEX. To lze učinit buď předložením samostatného oznámení v systému RAPEX nebo prostřednictvím systému ICSMS.
Propojení obou systémů usnadňuje kódování oznámení na základě údajů z šetření, které jsou již k dispozici v systému ICSMS. (Viz část II kapitola 1.2 písm. h)).
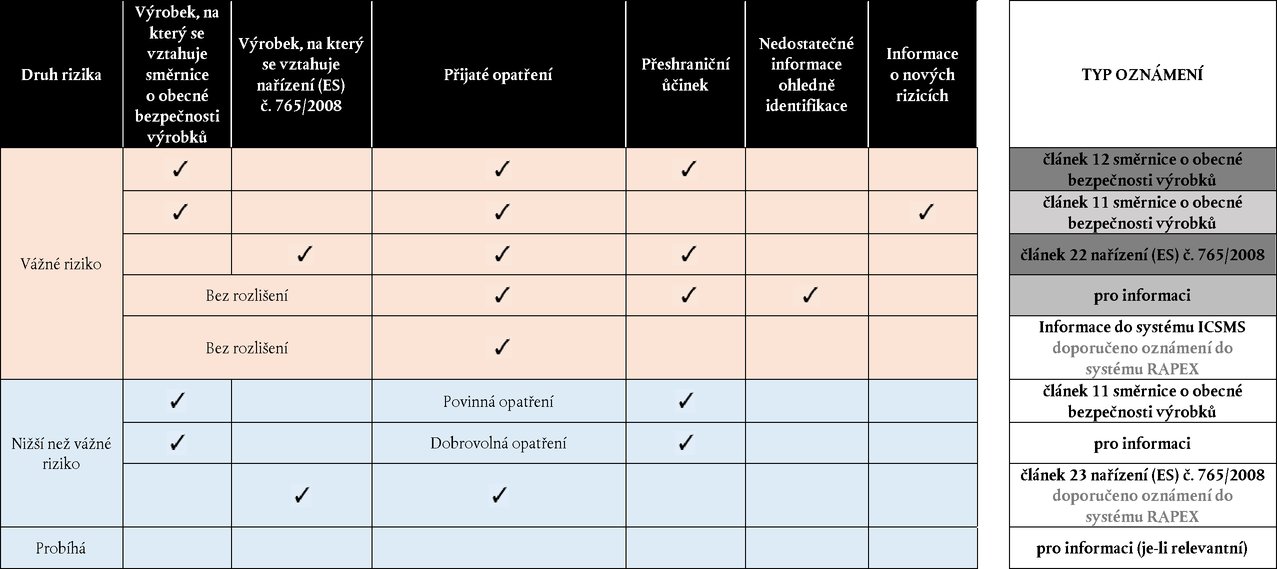
Druh rizika
Výrobek, na který se vztahuje směrnice o obecné bezpečnosti výrobků
Výrobek, na který se vztahuje nařízení (ES) č. 765/2008
Přijaté opatření
Přeshraniční ůčinek
Nedostatečné informace ohledně identifikace
Informace o nových rizicích
TYP OZNÁMENÍ
Vážné riziko
článek 12 směrnice o obecné bezpečnosti výrobků
článek 11 směrnice o obecné bezpečnosti výrobků
článek 22 nařízení (ES) č. 765/2008
Bez rozlišení
pro informaci
Bez rozlišení
Informace do systému ICSMS
doporučeno oznámení do systému RAPEX
Nižší než vážné riziko
Povinná opatření
článek 11 směrnice o obecné bezpečnosti výrobků
Dobrovolná opatření
pro informaci
článek 23 nařízení (ES) č. 765/2008
doporučeno oznámení do systému RAPEX
Probíhá
pro informaci (je-li relevantní)
V části III dodatku 3 těchto pokynů je zahrnut systém oznamovaní, který dále objasňuje kritéria oznamování uvedená v části II kapitole 2 těchto pokynů.
3 Oznámení
3.1 Typy oznámení
3.1.1 Oznámení
Orgány členských států jsou povinny předložit oznámení v systému RAPEX v těchto případech:
|
a) |
pokud jsou splněna všechna kritéria oznamování v systému RAPEX stanovená v článku 12 směrnice o obecné bezpečnosti výrobků (16), členský stát vypracuje a Komisi předloží oznámení v systému RAPEX, které je v aplikaci RAPEX klasifikováno jako „oznámení podle článku 12“; |
|
b) |
pokud jsou splněna všechna kritéria oznamování v systému RAPEX, a výrobek navíc představuje život ohrožující riziko a/nebo došlo k nehodám se smrtelnými následky, a v jiných případech, kdy oznámení v systému RAPEX vyžaduje okamžitou akci ze strany všech členských států, oznamující členský stát vypracuje a Komisi předloží oznámení v systému RAPEX, které je v aplikaci RAPEX klasifikováno jako „oznámení vyžadující okamžitou akci“; |
|
c) |
pokud jsou splněna všechna kritéria oznamování v systému RAPEX stanovená v článku 22 nařízení (ES) č. 765/2008 (17), členský stát vypracuje a Komisi předloží oznámení v systému RAPEX, které je v aplikaci RAPEX klasifikováno jako „oznámení podle článku 22“. |
Pokud jsou splněna všechna kritéria oznamování stanovená v článku 11 směrnice o obecné bezpečnosti výrobků (18), členský stát vypracuje a Komisi předloží oznámení, které je při oznámení v systému RAPEX klasifikováno jako „oznámení podle článku 11“.
Navíc se členské státy vyzývají, aby předkládaly oznámení, pokud jsou splněna kritéria stanovená v článku 23 nařízení (ES) č. 765/2008 (19).
Na základě výše uvedeného zdůvodnění v části II kapitole 2 se členské státy vyzývají, aby vypracovaly a Komisi přímo nebo nepřímo předložily oznámení, které je v systému RAPEX klasifikováno jako „oznámení podle článku 23“, pokud jsou splněna kritéria stanovená v témže článku.
Předtím, než je oznámení odesláno Komisi, kontaktní místo RAPEX (viz část II kapitola 5.1) oznamujícího členského státu zkontroluje, zda jsou všechna kritéria pro oznamování splněna.
3.1.2 Oznámení pro informaci
Pokud kritéria stanovená v těchto pokynech pro oznámení uvedená v části II kapitolách 2.1 a 2.2 těchto pokynů nejsou splněna, může se kontaktní místo RAPEX (viz část II kapitola 5.1) rozhodnout, že využije aplikaci RAPEX k odeslání tohoto oznámení pro informaci. Taková oznámení se v systému RAPEX klasifikují jako „oznámení pro informaci“ a je možné je poslat v těchto situacích:
|
a) |
Pokud jsou splněna všechna kritéria oznamování v systému RAPEX stanovená v článku 12 směrnice o obecné bezpečnosti výrobků nebo článku 22 nařízení (ES) č. 765/2008, nicméně oznámení neobsahuje všechny informace (zejména o identifikaci výrobků a distribučních kanálech), které ostatní členské státy potřebují k tomu, aby zajistily odpovídající opatření (20) následující po tomto oznámení. Příkladem oznámení, jež lze prostřednictvím aplikace RAPEX distribuovat jako „oznámení pro informaci“, je oznámení, v němž chybí název výrobku, značka a obrázek, a proto nelze oznámený výrobek správně identifikovat a rozlišit od ostatních výrobků stejné kategorie nebo typu, které jsou dostupné na trhu. Posouzení, zda dané oznámení obsahuje dostatek informací, aby ostatní členské státy mohly zajistit následné kroky, se vždy provádí případ od případu. |
|
b) |
Pokud si je členský stát vědom skutečnosti, že spotřební výrobek, který je k dispozici na trhu EU, představuje vážné riziko pro zdraví a bezpečnost spotřebitelů, nebo v případě výrobků, na které se vztahuje nařízení (ES) č. 765/2008, si je vědom skutečnosti, že spotřební nebo profesionální výrobek představuje vážné riziko pro zdraví a bezpečnost nebo jiné relevantní veřejné zájmy konečných uživatelů, nicméně výrobce nebo distributor zatím nepodnikl preventivní a omezovací opatření ani orgán členského státu taková opatření nepřijal ani o nich nerozhodl. Pokud se informace o takovém výrobku rozšíří prostřednictvím aplikace RAPEX před přijetím odpovídajících opatření, oznamující členský stát následně informuje Komisi (co nejdříve, nejpozději ve lhůtě stanovené v dodatku 4 těchto pokynů) o konečném rozhodnutí, které bylo přijato v souvislosti s oznámeným výrobkem (zejména jaký typ preventivních nebo omezujících opatření byl přijat nebo proč taková opatření přijata nebyla). Pokud oznamující členský stát přijme opatření později, informuje Komisi, která provede aktualizaci oznámení podle článku 12 směrnice o obecné bezpečnosti výrobků nebo článku 22 nařízení (ES) č. 765/2008. |
|
c) |
Pokud se členský stát rozhodne oznámit preventivní a omezující opatření přijatá v souvislosti se spotřebním výrobkem představujícím vážné riziko pro zdraví a bezpečnost spotřebitelů, který má pouze místní účinky („místní událost“). Jak bylo uvedeno v části I kapitole 6.2, obsahuje-li však oznámení o „místní události“ informace o bezpečnosti výrobků, které by mohly zajímat i ostatní členské státy, mělo by být posláno tak, jako by se jednalo o oznámení podle článku 11 směrnice o obecné bezpečnosti výrobků. |
|
d) |
Pokud se oznámení týká výrobku, jehož bezpečnostní hlediska (zejména výše rizika pro zdraví a bezpečnost spotřebitelů) jsou předmětem diskuse na úrovni EU s cílem zajistit společný přístup členských států k posuzování rizik a/nebo vynucovacím opatřením (21). |
|
e) |
Pokud nelze s jistotou rozhodnout, že bylo splněno jedno nebo více kritérií oznamování, nicméně oznámení obsahuje informace o bezpečnosti výrobků, které by mohly zajímat i ostatní členské státy. |
Při posílání „oznámení pro informaci“ kontaktní místo RAPEX (viz část II kapitola 5.1) jasně uvede své důvody, proč oznámení posílá.
3.2 Obsah oznámení
3.2.1 Rozsah údajů
Oznámení zasílaná Komisi prostřednictvím aplikace RAPEX obsahují tyto typy údajů:
|
a) |
Informace umožňující identifikaci oznámeného výrobku, tj. kategorii výrobku, název výrobku, značku, číslo modelu a/nebo typu, čárový kód, číslo výrobní série nebo výrobní číslo, celní kód, popis výrobku a jeho balení spolu s vyobrazením výrobku, obalu a etiket. Podrobná a přesná identifikace výrobku je klíčovým prvkem dozoru nad trhem a vynucování, neboť umožňuje vnitrostátním orgánům identifikovat oznámený výrobek, odlišit ho od dalších výrobků stejného nebo podobného typu nebo kategorie, které jsou dostupné na trhu, a nalézt ho na trhu a přijmout nebo schválit vhodná opatření. |
|
b) |
Informace o určení původu výrobku, tj. země původu, jméno/název, adresa a kontaktní údaje výrobce a vývozců, jako jsou telefonní číslo a e-mailová adresa. Členské státy zejména uvádějí veškeré dostupné informace o výrobcích a vývozcích se sídlem ve třetích zemích, které úzce spolupracují s EU v oblasti bezpečnosti výrobků. K formuláři je rovněž třeba přiložit tyto doklady, pokud jsou k dispozici: kopie objednávek, kupní smlouvy, faktury, přepravní doklady, celní prohlášení atd. Tyto doklady by měly být předány ve formátu pdf nebo jakémkoli jiném formátu, který aplikace podporuje. Podrobné informace o výrobcích ze třetích zemí umožňují Komisi prosazovat účinnější vynucování bezpečnosti výrobků v těchto zemích a pomáhají snižovat počet výrobků představujících riziko pro spotřebitele a dovážených do EU. |
|
c) |
Kdykoli je to možné, informace o tom, kde přesně byl výrobek dán k dispozici (obchodní dům, místní obchod nebo trh, on-line atd.). |
|
d) |
Informace o bezpečnostních požadavcích platných pro oznámený výrobek, včetně referenčního čísla a názvu platných právních předpisů a norem. |
|
e) |
Popis rizika spojeného s oznámeným výrobkem, včetně popisu výsledků laboratorních nebo vizuálních testů, protokolů o zkouškách a certifikátů potvrzujících, že oznámený výrobek nesplňuje bezpečnostní požadavky, úplného posouzení rizik se závěry a informací o známých nehodách nebo incidentech (viz část I kapitola 3.3.1 těchto pokynů). |
|
f) |
Informace o dodavatelských řetězcích oznámeného výrobku v členských státech, zejména informace o zemích určení, dále informace o dovozcích, případně o distributorech oznámeného výrobku v Evropě, jsou-li k dispozici. |
|
g) |
Informace o přijatých opatřeních, zejména o jejich typu (povinná nebo dobrovolná), kategorii (např. stažení z trhu nebo zpětné převzetí od spotřebitelů), působnosti (např. vnitrostátní, místní), datu vstupu v platnost a době trvání opatření (např. trvalá, dočasná). |
|
h) |
Označení toho, zda jsou oznámení, jeho část nebo přílohy důvěrné. Požadavek na zachování důvěrnosti je vždy doplněn vysvětlením, v němž se jasně uvádějí důvody tohoto požadavku. |
|
i) |
Informace o tom, zda je výrobek padělaný, jsou-li k dispozici. Za tímto účelem Komise poskytne členským státům veškeré specifické nástroje dostupné na úrovni EU s cílem usnadnit identifikaci padělaných výrobků. |
|
j) |
Informace o hlášených nehodách souvisejících s výrobkem, které pokud možno uvádějí důvod nehody (riziko související s tím, jak spotřebitel výrobek používá, nebo riziko, které je danému výrobku inherentní). |
|
k) |
Doplňující informace ohledně toho, zda bylo oznámení předloženo v rámci koordinovaného prosazování práva na evropské úrovni. |
|
l) |
Informace o tom, zda orgány členského státu hodlají zaslat další oznámení týkající se stejného výrobku nebo podobných výrobků. Ty by měly být uvedeny v původním oznámení. |
Členské státy se vybízejí, aby vyhledávaly a poskytovaly informace o dodavatelských řetězcích oznámeného výrobku v zemích mimo EU, které v oblasti bezpečnosti výrobků s EU úzce spolupracují.
3.2.2 Úplnost údajů
Oznámení by měla být co nejúplnější. Prvky, které mají být obsaženy v oznámení, jsou uvedeny v dodatku 1 těchto pokynů a jsou zahrnuty do aplikace RAPEX. Ve všech kolonkách formuláře pro oznámení by měly být vyplněny požadované údaje. Nejsou-li v době předkládání oznámení požadované informace k dispozici, oznamující členský stát to ve formuláři jasně uvede a vysvětlí. Jakmile má oznamující členský stát chybějící informace k dispozici, provede aktualizaci svého oznámení. Komise aktualizované oznámení zkontroluje předtím, než ho potvrdí a rozšíří v systému.
Kontaktní místa RAPEX poskytují všem vnitrostátním orgánům, které jsou zapojené do sítě RAPEX, pokyny ohledně rozsahu údajů požadovaných pro vyplnění oznámení. To pomůže zajistit správnost a úplnost informací, které tyto orgány poskytnou kontaktnímu místu RAPEX (viz část II kapitola 5.1).
Členské státy by měly dodržet stanovené lhůty a neodkládat oznámení v systému RAPEX týkající se výrobku, který představuje život ohrožující riziko pro zdraví a bezpečnost spotřebitelů nebo jiných konečných uživatelů a/nebo v případech, kdy oznámení v systému RAPEX vyžaduje okamžitou akci ze strany členských států, z toho důvodu, že zatím nemají k dispozici část údajů požadovaných podle pokynů.
Před předložením oznámení zkontroluje kontaktní místo RAPEX, zda dotčený výrobek již v aplikaci RAPEX neoznámil jiný členský stát (aby se zamezilo zbytečné duplicitě). Pokud byl již výrobek oznámen, kontaktní místo RAPEX nevypracuje nové oznámení, nýbrž předloží následné oznámení na stávající oznámení a poskytne veškeré doplňující informace, které by mohly být důležité pro orgány v jiném členském státě, jako jsou další identifikační čísla vozidla, podrobný seznam dovozců a distributorů, další protokoly o zkouškách atd. (viz též část II kapitola 5.1).
3.2.3 Aktualizace údajů
Oznamující členský stát informuje Komisi (co nejdříve a nejpozději ve lhůtě stanovené v dodatku 4 těchto pokynů) o každém vývoji, který vyžaduje provedení změn v oznámení předávaném prostřednictvím aplikace RAPEX. Členský stát Komisi zejména oznámí veškeré změny (vyplývající např. z rozhodnutí soudu během odvolacího řízení) statusu oznámených opatření, posouzení rizik a nových rozhodnutí týkajících se důvěrnosti.
Komise přezkoumá informace, které jí poskytl oznamující členský stát, a provede aktualizaci dotčených informací v aplikaci RAPEX, v případě potřeby pak i na internetové stránce systému RAPEX.
3.2.4 Odpovědnost za předávané informace
Odpovědnost za poskytnuté informace nese oznamující členský stát (22).
Oznamující členský stát a odpovědný vnitrostátní orgán zajistí, že veškeré údaje poskytované prostřednictvím aplikace RAPEX jsou přesné, aby se zamezilo jakékoliv záměně s podobnými výrobky stejné kategorie nebo typu, které jsou dostupné na trhu EU.
Orgány zapojené do postupu oznamování (např. tím, že provádějí posouzení rizik oznámeného výrobku nebo poskytují informace o distribučních kanálech) nesou odpovědnost za informace poskytnuté prostřednictvím aplikace RAPEX. Kontaktní místo RAPEX zkontroluje a potvrdí všechna oznámení, která dostalo od odpovědných orgánů, před jejich předáním Komisi (viz též část II kapitola 5.1).
Žádné kroky podniknuté Komisí, jako je zkoumání oznámení, jejich potvrzování a šíření prostřednictvím aplikace RAPEX a zveřejňování na internetové stránce systému RAPEX, neznamenají převzetí odpovědnosti za předávané informace, kterou nadále nese oznamující členský stát.
3.3 Subjekty zapojené do postupu oznamování a jejich úlohy
Do postupu oznamování jsou zapojeny tyto strany, které mají tyto povinnosti:
3.3.1 Hospodářské subjekty
Hospodářské subjekty nejsou přímo zapojené do předkládání oznámení v aplikaci RAPEX.
Avšak v případě výrobku, který představuje riziko, hospodářské subjekty ihned informují příslušné orgány ve všech členských státech, kde byl výrobek uveden na trh. Podmínky a podrobnosti poskytování těchto informací jsou stanoveny v příloze I směrnice o obecné bezpečnosti výrobků.
Tyto informace zpracovává členský stát, v němž je oznamující výrobce/distributor usazen (dále jen „hlavní členský stát“).
Informace o výrobcích představujících riziko mohou hospodářské subjekty předávat prostřednictvím brány pro varování ze strany podniků ohledně bezpečnosti výrobků („Product Safety Business Alert Gateway“), což je nástroj dostupný na internetové stránce RAPEX (viz část II kapitola 5.3.2). Hospodářské subjekty by měly uvést podrobný popis rizika, které výrobek představuje, a mohou využít nástroj „RAG“ určený pro tento účel (viz část I kapitola 5.3).
Posouzení rizik provedená hospodářskými subjekty nejsou pro orgány členského státu odpovědné za provedené vlastního posouzení rizik závazná. Je tedy možné, že orgán členského státu dojde k jinému závěru ohledně posouzení rizik, než je závěr uvedený ve výstraze předané prostřednictvím brány pro podniky („Business Gateway“).
3.3.2 Orgány členských států
Orgány členských států prostřednictvím aplikace RAPEX oznámí Komisi povinná i dobrovolná opatření přijatá na jejich území proti výrobkům představujícím riziko.
Členské státy určí, kdo je ve vztahu k systému RAPEX odpovědný za vypracování a předkládání oznámení a za následná opatření.
3.3.3 Orgány provádějící kontroly na vnějších hranicích
Opatření přijatá orgány provádějícími kontroly na vnějších hranicích, která brání tomu, aby byly na trh EU uváděny spotřební výrobky, jež představují vážné riziko pro zdraví a bezpečnost spotřebitelů (např. rozhodnutí zastavit dovoz na hranicích EU), by se Komisi měla oznamovat prostřednictvím aplikace RAPEX stejným způsobem jako opatření přijatá orgány dozoru nad trhem, která omezují uvádění výrobků na trh nebo jejich používání.
3.3.4 Evropská komise
Komise může informovat kontaktní místa RAPEX (viz část II kapitola 5.1) o výrobcích dovezených do Společenství a Evropského hospodářského prostoru nebo ze Společenství a z Evropského hospodářského prostoru vyvezených, které představují vážná rizika (23).
Komise může předávat členským státům informace o výrobcích představujících riziko a pocházejících ze zemí EU i mimo ně, které se podle dostupných informací pravděpodobně nacházejí na trhu EU. To se týká zejména informací, které Komise dostává ze třetích zemí, od mezinárodních organizací, podniků nebo prostřednictvím jiných systémů včasného varování.
Tyto informace mohou být šířeny mezi členskými státy jinými prostředky než aplikací RAPEX.
3.4 Pracovní postup
3.4.1 Vypracování oznámení
3.4.1.1
Podle vnitrostátní úpravy mohou oznámení vytvářet různé vnitrostátní orgány zapojené do procesu oznamování v systému RAPEX (místní/regionální orgány dozoru nad trhem, orgány provádějící kontroly na vnějších hranicích atd.).
3.4.1.2
V některých případech může vytvořit oznámení Komise, jak je vysvětleno v bodě 3.3.4.
3.4.2 Předložení oznámení Komisi
Za předložení všech oznámení k potvrzení Komisí je odpovědné kontaktní místo RAPEX. (Viz část II kapitola 5.1).
3.4.3 Zkoumání oznámení Komisí
Komise kontroluje všechna oznámení, která obdrží prostřednictvím aplikace RAPEX, aby zajistila jejich správnost a úplnost, než je předá členským státům.
3.4.3.1
Při posuzování správnosti oznámení Komise zejména kontroluje, zda:
|
a) |
oznámení splňuje všechny relevantní požadavky stanovené ve směrnici o obecné bezpečnosti výrobků nebo v článku 22 nařízení (ES) č. 765/2008 a v těchto pokynech; |
|
b) |
oznámený výrobek již nebyl oznámen (aby se zamezilo zbytečné duplicitě, i mezi systémy ICSMA a RAPEX); |
|
c) |
oznámení, které předložil oznamující členský stát k potvrzení, je klasifikováno podle kritérií stanovených v části II kapitole 2 těchto pokynů; |
|
d) |
poskytnuté informace, včetně posouzení rizika, řádně zohledňují platné právní předpisy a příslušné normy; |
|
e) |
byl použit správný postup oznamování. |
3.4.3.2
Po potvrzení správnosti oznámení Komise zkontroluje, zda je úplné. Jako referenční bod slouží část II kapitoly 3.2.1 a 3.2.2 těchto pokynů. Zvláštní pozornost se věnuje těm částem oznámení, které se týkají identifikace výrobku, popisu rizika, přijatých opatření, sledovatelnosti a distribučních kanálů.
Komise není odpovědná za provádění posouzení rizik výrobku, pouze za kontrolu, že oznámení obsahuje příslušné posouzení rizik se všemi prvky uvedenými v části II kapitole 3.2.1 těchto pokynů (s výjimkami uvedenými v bodě 3.4.3.3). Viz též část I kapitola 5.1 těchto pokynů.
3.4.3.3
Členské státy by měly ke každému oznámení předložit posouzení rizik, avšak v některých případech může Komise potvrdit oznámení, která byla předložena bez podrobného a individuálního posouzení rizik:
a) Oznámení výrobků představujících chemické riziko
Úroveň rizika výrobku může být považována za vážnou, pokud výrobek obsahuje chemickou látku, která je buď zakázána, nebo je v koncentraci vyšší než limit stanovený evropskými právními předpisy. Proto může být v případech, kdy jsou přijata opatření proti výrobkům obsahujícím chemickou látku podléhající omezení podle právních předpisů EU, oznámení předloženo bez podrobného posouzení rizik.
b) Oznámení kosmetických přípravků
Potvrzení oznámení, která neobsahují podrobné posouzení rizik, může být taktéž možné v případě kosmetických přípravků obsahujících zakázané látky nebo látky podléhající omezení, které jsou podloženy stanoviskem vědeckého výboru EU, jež dokládá, že přítomnost látek nad stanovené limity představuje riziko pro zdraví a bezpečnost spotřebitelů. V tomto specifickém odvětví výrobků může být třeba vzít v úvahu i jiné faktory (např. koncentraci nebo dobu expozice).
Nicméně pokud byla přijata opatření v souvislosti s výrobkem obsahujícím nepovolené chemické látky, pro něž nebylo vydáno žádné vědecké stanovisko potvrzující, že výrobek představuje riziko, může být na základě individuálního posouzení vyžadováno řádné posouzení rizik s cílem prokázat, že výrobek představuje vážné nebo nižší než vážné riziko. Případy, kdy je nutné posouzení rizik, avšak takové posouzení rizik není předloženo, lze v systému RAPEX potvrdit pouze „pro informaci“.
Pokud jde o výrobky, na které se vztahují omezující opatření orgánů dozoru nad trhem z důvodu obsahu chemické látky, která je uvedena na seznamu složek, na něž se vztahují omezení obsažená v právních předpisech EU a kde nejsou k dispozici vědecké údaje hodnotící riziko, musí být oznámení posuzována případ od případu. Případy, kdy je nutné posouzení rizik, avšak takové posouzení rizik není předloženo, lze v systému RAPEX potvrdit pouze „pro informaci“.
c) Oznámení dalších výrobků
Pokud existují řádně doložené důkazy, že některé prvky určitých výrobků soustavně vedou ke specifickému riziku a úrovni rizika (např. stahovací šňůry nebo funkční šňůrky v oblasti hlavy, krku nebo hrudníku na oděvech pro malé děti představují vždy vážné riziko), není pro daný výrobek požadováno žádné další posouzení rizik.
3.4.3.4
Pokud by během svého zkoumání měla Komise otázky týkající se oznámení, může pozastavit potvrzování oznámení a požádat oznamující členský stát o doplňující informace nebo o vysvětlení. Oznamující členský stát poskytne tyto doplňující informace ve lhůtě uvedené v žádosti Komise o informace.
3.4.3.5
Je-li to nutné, může Komise provést šetření, aby posoudila bezpečnost výrobku. Toto šetření lze provést zejména tehdy, pokud existují vážné pochybnosti ohledně rizik, které představuje výrobek oznámený prostřednictvím aplikace RAPEX. Tyto pochybnosti mohou vzniknout buď během zkoumání oznámení ze strany Komise, nebo na základě upozornění Komise ze strany členského státu (např. prostřednictvím následného oznámení) nebo třetí strany (např. výrobce).
V rámci tohoto šetření může Komise zejména:
|
a) |
požádat jakýkoli členský stát o informace nebo o vysvětlení, |
|
b) |
požádat o nezávislé posouzení rizik a nezávislé testování (laboratorní nebo vizuální) výrobku, který je předmětem šetření, |
|
c) |
konzultovat vědecké výbory, Společné výzkumné středisko nebo jinou instituci, která se zaměřuje na bezpečnost spotřebních výrobků, |
|
d) |
svolat zasedání výboru zřízeného směrnicí o obecné bezpečnosti výrobků, sítě pro bezpečnost spotřebitelů a/nebo kontaktních míst RAPEX a konzultovat příslušné pracovní skupiny s cílem projednat vývoj v šetření. |
Pokud se šetření týká výrobku oznámeného v aplikaci RAPEX, může Komise pozastavit potvrzování oznámení, nebo pokud bylo oznámení již potvrzeno a rozšířeno prostřednictvím aplikace RAPEX, může Komise dočasně odstranit přehled zveřejněný na internetové stránce systému RAPEX. Po ukončení šetření může Komise (v případě potřeby po konzultacích s oznamujícím členským státem) v závislosti na jeho výsledku zejména potvrdit pozastavené oznámení a rozšířit ho prostřednictvím aplikace RAPEX, ponechat potvrzené oznámení v aplikaci RAPEX (s určitými změnami) nebo oznámení z aplikace RAPEX natrvalo stáhnout.
Komise informuje všechny členské státy o:
|
a) |
svém rozhodnutí zahájit šetření s jasným uvedením důvodů pro své rozhodnutí, |
|
b) |
svém rozhodnutí ukončit šetření s předložením závěrů a změn prošetřovaných oznámení (pokud k nějakým změnám došlo), |
|
c) |
všech důležitých událostech během šetření. |
3.4.4 Potvrzování a šíření oznámení
Komise potvrdí a prostřednictvím aplikace RAPEX rozšíří všechna oznámení, která byla při šetření vyhodnocena jako správná a úplná, ve lhůtě uvedené v dodatku 5 těchto pokynů.
Pokud byla během šetření zaslána oznamujícímu členskému státu žádost o doplňující informace nebo vysvětlení (následovaná případně upomínkou), může Komise přijmout toto rozhodnutí:
|
a) |
pokud Komise obdržela požadované doplňující informace nebo vysvětlení, přezkoumá dané oznámení a může ho potvrdit, případně se změnou klasifikace (např. z kategorie „oznámení pro informaci“ na kategorii „oznámení podle článku 12“), nebo pozastavit do té doby, než obdrží další vysvětlení, |
|
b) |
pokud Komise neobdržela požadované doplňující informace nebo vysvětlení ve stanovené lhůtě nebo pokud jsou tyto informace a tato vysvětlení nedostatečná, rozhodne se Komise na základě poskytnutých informací a podle okolností buď oznámení potvrdí po změně jeho klasifikace (např. z kategorie „oznámení podle článku 12“ na kategorii „oznámení pro informaci“), nebo ho nepotvrdí. |
Poté, co se členské státy dohodly na společném přístupu k posuzování rizik nebo vynucovacím opatřením, může Komise v závislosti na okolnostech a stanoviscích členských států přijmout jedno z následujících opatření:
|
a) |
ponechat dotčená oznámení v aplikaci RAPEX, |
|
b) |
změnit klasifikaci oznámení uložených v aplikaci RAPEX, |
|
c) |
stáhnout oznámení z aplikace RAPEX (24). |
3.4.5 Zveřejnění oznámení
3.4.5.1
Veřejnost má právo být informována o výrobcích, které představují riziko. Aby splnila tento závazek, zveřejňuje Komise přehledy nových oznámení na internetové stránce systému RAPEX (25).
Z důvodů externí komunikace budou na internetových stránkách systému RAPEX v budoucnu nazývány „Safety Gate“.
Členské státy stejným způsobem poskytují veřejnosti informace v národních jazycích o výrobcích, které představují vážné riziko pro spotřebitele, a o opatřeních přijatých k řešení tohoto rizika. Tyto informace lze šířit prostřednictvím internetu, v tištěné podobě, elektronickými médii atd.
Veřejnosti se poskytují informace v podobě souhrnu oznámení, který obsahuje zejména údaje umožňující identifikaci výrobku a informace o rizicích a opatřeních přijatých k zabránění těmto rizikům nebo k jejich omezení. Komise a členské státy se mohou rozhodnout zveřejnit další prvky oznámení pouze v případě, že tyto informace nejsou vzhledem ke své povaze důvěrné povahy (profesní tajemství) a není třeba je chránit.
Na internetových stránkách systému RAPEX jsou zveřejněna tato oznámení v souladu s požadavky stanovenými v článku 16 směrnice o obecné bezpečnosti výrobků:
|
a) |
oznámení spadající do působnosti článku 12 směrnice o obecné bezpečnosti výrobků, |
|
b) |
oznámení spadající do působnosti článku 22 nařízení (ES) č. 765/2008, |
|
c) |
oznámení spadající do působnosti článku 11 směrnice o obecné bezpečnosti výrobků v případě výrobků, které představují nižší než vážné riziko a u nichž byl rovněž uznán přeshraniční účinek. Jak je stanoveno v kapitole 3.4, je třeba takový scénář podle článku 11 oznámit, pokud existuje přeshraniční účinek, |
|
d) |
oznámení spadající do působnosti článku 23 nařízení (ES) č. 765/2008 týkající se výrobků, které představují nižší než vážná rizika, a to bez ohledu na to, zda byla přijatá opatření povinná nebo dobrovolná (26), |
|
e) |
oznámení podaná pouze pro informaci, jestliže o to oznamující členský stát požádá zaškrtnutím příslušného políčka v systému RAPEX, zejména pokud jsou přijata dobrovolná opatření a dotčené produkty jsou dostatečně identifikovány. Zveřejnění těchto oznámení by mohlo být nutné z hlediska zajištění vhodného řízení rizik. |
3.4.5.2
Členské státy a Komise by neměly poskytnout veřejnosti žádné informace o výrobku oznámeném prostřednictvím aplikace RAPEX, pokud by takové zveřejnění mělo ohrozit ochranu soudních řízení, sledování a vyšetřování nebo služební tajemství, kromě informací o vlastnostech výrobků týkajících se bezpečnosti, které musí být, jestliže to okolnosti vyžadují, zveřejněny v zájmu ochrany zdraví a bezpečnosti spotřebitelů, nebo v případě výrobků, na které se vztahuje nařízení (ES) č. 765/2008, také v zájmu ochrany dalších relevantních veřejných zájmů konečných spotřebitelů (27).
3.4.5.3
Oznamující členský stát může ve svém oznámení uvést, že požaduje zachování důvěrnosti. Ve své žádosti jasně uvede, kterých částí oznámení se má zachování důvěrnosti týkat.
Každý požadavek na zachování důvěrnosti je navíc doplněn vysvětlením, v němž se jasně uvádějí důvody tohoto požadavku (28).
Požadavky na zachování důvěrnosti musí přezkoumat Komise. Komise zkontroluje, zda je žádost úplná (tj. že uvádí, které části oznámení jsou důvěrné, a obsahuje odůvodnění) a oprávněná (tj. v souladu s ustanoveními směrnice o obecné bezpečnosti výrobků a s těmito pokyny). Poté, co konzultuje příslušné kontaktní místo RAPEX, rozhodne Komise o platnosti požadavku. (Viz část II kapitola 5.1).
3.4.5.4
Ustanovení čl. 16 odst. 2 směrnice o obecné bezpečnosti výrobků uvádí, že ochrana služebního tajemství nebo důvěrnosti nesmí bránit předávání informací důležitých pro zajištění účinnosti kontroly trhu a činností dozoru příslušným orgánům. Oznámení, která jsou částečně nebo zcela důvěrná, jsou přezkoumána Komisí a po jejich potvrzení a rozšíření prostřednictvím aplikace RAPEX následují obvyklé následné činnosti ze strany členských států. Důvěrnost oznámení nebo jeho částí nebrání tomu, aby s ním bylo manipulováno a aby bylo prostřednictvím aplikace RAPEX předáno příslušným vnitrostátním orgánům.
Jediný podstatný rozdíl v manipulaci a následných krocích spočívá v tom, že Komise a členské státy by neměly veřejnosti poskytnout žádné části oznámení, které jsou důvěrné. Tyto části musejí zůstat důvěrné, a neměly by tedy být zveřejněny v žádné podobě. Orgány členských států, které prostřednictvím aplikace RAPEX obdrží důvěrné informace, zaručí jejich ochranu při provádění svých činností.
3.4.5.5
Oznamující členský stát stáhne svůj požadavek na zachování důvěrnosti ihned poté, co orgán uvedeného členského státu zjistí, že tento požadavek již není oprávněný, a informuje o tom Komisi. Poté, co Komise od oznamujícího členského státu obdrží žádost o stažení požadavku na zachování důvěrnosti, informuje všechny členské státy o tomto stažení.
Oznámení, které již není zčásti nebo zcela důvěrné, je poskytnuto veřejnosti v souladu s „obecnými pravidly“ platnými pro zveřejňování oznámení stanovenými v těchto pokynech.
3.4.6 Kroky následující po oznámení
3.4.6.1
Členské státy zajistí, aby po „oznámení podle článku 12“, „oznámení podle článku 12 vyžadující okamžitou akci“ a oznámeních podle článku 22 nařízení (ES) č. 765/2008 a po informacích o výrobcích představujících riziko zaslaných Komisí (kapitola 3.3.4) následovaly odpovídající kroky, a to co nejdříve, nejpozději však ve lhůtě uvedené v dodatku 4 těchto pokynů.
Oznámení pro informaci ani oznámení podle článku 11 směrnice o obecné bezpečnosti výrobků a oznámení podle článku 23 nařízení (ES) č. 765/2008 (oznámení ohledně nižších než vážných rizik) nevyžadují zvláštní následné činnosti. Tato oznámení často neobsahují údaje potřebné pro účinné a efektivní vynucování v souvislosti s oznámeným výrobkem (např. oznámený výrobek a/nebo opatření nejsou dostatečně určeny) nebo úroveň rizika není považována za vážnou.
I když v uvedených případech není nijak zvlášť zapotřebí přijmout následná opatření, je přesto důležité, aby členské státy prověřily, zda se případně nedomnívají, že riziko je nižší než vážné, aby případně mohly reagovat na informace odlišného posouzení rizik. Členské státy se proto vyzývají, aby zajistily následné kroky po těchto oznámeních v případě, že je pravděpodobné, že oznámený výrobek byl spotřebitelům dán k dispozici na jejich trhu a identifikace výrobku umožňuje, aby byla přijata příslušná opatření.
3.4.6.2
Po přijetí oznámení členský stát přezkoumá informace uvedené v oznámení a provede příslušné akce, aby:
|
a) |
zjistil, zda byl výrobek uveden na jeho území, |
|
b) |
posoudil, jaká preventivní nebo omezovací opatření je třeba přijmout v souvislosti s oznámeným výrobkem vyskytujícím se na jeho trhu s ohledem na opatření, která přijal oznamující členský stát, a na zvláštní okolnosti, jimiž by bylo možné odůvodnit přijetí různých druhů opatření nebo jejich nepřijetí, |
|
c) |
provedl další posouzení rizik a testování oznámeného výrobku, je-li to nutné, |
|
d) |
shromáždil doplňující informace, které by mohly být důležité pro ostatní členské státy (např. informace o distribučních kanálech oznámeného výrobku v jiných členských státech). |
3.4.6.3
K zajištění efektivních a účinných následných kroků by vnitrostátní orgány měly používat osvědčené postupy, kam patří:
a) Kontroly trhu
Vnitrostátní orgány provádějí pravidelné (plánované a náhodné) kontroly trhu, aby zjistily, zda jsou spotřební výrobky oznámené prostřednictvím aplikace RAPEX k dispozici spotřebitelům. Pokud je členský stát uveden jako cílová země, provedou se na trhu posílené kontroly, zejména kontaktováním hospodářských subjektů uvedených v oznámení.
b) Spolupráce se sdruženími podnikatelů
Vnitrostátní orgány v případě potřeby poskytují sdružením podnikatelů přehledy nejnovějších oznámení a zjišťují, zda jejich členové vyráběli nebo distribuovali některé z oznámených výrobků. Vnitrostátní orgány poskytují podnikům pouze souhrny oznámení, jako jsou týdenní přehledy zveřejňované na internetové stránce RAPEX. Celá oznámení se třetím stranám nepředávají, neboť některé informace (např. podrobný popis rizik nebo informace o distribučních kanálech) jsou často důvěrné a měly by být chráněny.
c) Zveřejňování údajů v systému RAPEX prostřednictvím internetu nebo jiných elektronických a tištěných médií
Vnitrostátní orgány na svých internetových stránkách nebo prostřednictvím jiných médií pravidelně upozorňují spotřebitele a podniky na spotřební výrobky oznámené prostřednictvím aplikace RAPEX, např. odkazují spotřebitele a podniky na internetovou stránku systému RAPEX. Informace zveřejňované tímto způsobem umožňují spotřebitelům zjistit, zda vlastní a používají výrobky představující riziko, a orgánům často poskytují užitečnou zpětnou vazbu.
d) Kontroly na internetu
Vnitrostátní orgány pravidelně provádějí kontroly na internetu a snaží se zjistit, zda jsou výrobky oznámené v systému RAPEX dostupné na on-line trzích. Kontrolní postupy na internetu mohou zahrnovat automatizované procházení webu (web crawling), vytěžování dat (data mining), automatizovanou extrakci dat z výstupů pro uživatele (data scraping) atd.
Vnitrostátní orgány provádějí současně různé následné kroky a neměly by se zaměřovat pouze na jednu činnost.
Vhodné kroky následující po oznámeních rozšířených prostřednictvím aplikace RAPEX by měl podniknout ten členský stát, v němž je výrobce, zástupce nebo dovozce oznámeného výrobku usazen („hlavní členský stát“). „Hlavní členský stát“ mívá často lepší právní a technické prostředky k získávání informací o oznámeném případu, které ostatním členským státům pomohou podniknout účinné následné činnosti.
3.4.7 Stažení/odstranění oznámení
3.4.7.1
Oznámení šířená prostřednictvím aplikace RAPEX jsou v systému uložena na neomezenou dobu. Komise nicméně může v situacích uvedených v této kapitole oznámení ze systému RAPEX trvale stáhnout.
3.4.7.1.1 Situace, za kterých je možné předložené nebo potvrzené oznámení stáhnout
|
a) |
Existuje důkaz, že jedno nebo více kritérií oznamování (29) nebylo splněno, takže oznámení není oprávněné. To se zejména týká případů, kdy se potvrdí, že prvotní posouzení rizik bylo provedeno nesprávně a že oznámený výrobek nepředstavuje riziko. Týká se to rovněž situací, kdy byla oznámená opatření úspěšně napadena v soudním nebo jiném řízení a již nejsou platná. |
|
b) |
Nebyla přijata žádná opatření v souvislosti s výrobkem oznámeným prostřednictvím aplikace RAPEX (pro informaci) předtím, než bylo rozhodnuto o přijetí opatření nebo provedení akcí (30). |
|
c) |
Po projednání na úrovni EU se členské státy dohodly, že je zbytečné si vyměňovat informace o některých bezpečnostních hlediscích, která byla oznámena prostřednictvím aplikace RAPEX (31). |
|
d) |
Výrobky uvedené v oznámení se již na trhu prokazatelně nevyskytují a všechny výrobky, které byly dány do oběhu, již byly prokazatelně staženy z trhu a z oběhu ve všech členských státech. |
Stažení oznámení, které bylo předloženo nebo potvrzeno, nelze požadovat na základě skutečnosti, že u oznámeného výrobku byly provedeny změny potřebné k tomu, aby splňoval všechny příslušné požadavky na bezpečnost, ledaže byly předloženy důkazy, že všechny dotčené výrobky (kusy), které byly spotřebitelům dány k dispozici, již byly staženy z trhu a z oběhu ve všech členských státech a že se již na trhu nevyskytují.
3.4.7.1.2 Žádost členských států o trvalé nebo dočasné stažení oznámení
Komise může stáhnout oznámení ze systému RAPEX pouze na žádost oznamujícího členského státu, neboť ten je plně odpovědný za informace předávané prostřednictvím tohoto systému. Komise nicméně vyzývá ostatní členské státy, aby ji informovaly o veškerých skutečnostech, které by mohly stažení odůvodnit.
3.4.7.1.3 Obsah žádosti o trvalé nebo dočasné stažení oznámení
Ke každé žádosti o stažení oznámení je třeba přiložit odůvodnění, v němž se jasně uvedou důvody této žádosti, a veškeré dostupné doklady na jejich podporu. Komise přezkoumá každou žádost a zkontroluje zejména odůvodnění a doprovodné doklady. Komise si může předtím, než přijme rozhodnutí, vyžádat doplňující informace, vysvětlení nebo stanovisko oznamujícího členského státu nebo jiných členských států.
3.4.7.1.4 Rozhodnutí o stažení oznámení
Pokud se na základě poskytnutého odůvodnění Komise rozhodne, že oznámení ze systému RAPEX stáhne, odstraní ho z:
|
a) |
aplikace RAPEX (nebo jiným způsobem zajistí, aby ho uživatelé systému nemohli vidět), |
|
b) |
z internetové stránky systému RAPEX (je-li to nutné). |
Komise informuje všechny členské státy o stažení oznámení poštou nebo jinými stejně účinnými prostředky, v případě nutnosti informuje také veřejnost zveřejněním opravy na internetové stránce systému RAPEX.
3.4.7.2
3.4.7.2.1 Situace, za nichž je dočasné odstranění oznámení možné
V oprávněných případech může Komise dočasně odstranit oznámení z internetové stránky systému RAPEX, zejména v případě, že má oznamující členský stát podezření, že posouzení rizik uvedené v oznámení bylo provedeno nesprávně a že oznámený výrobek nepředstavuje riziko. Oznámení může být z internetové stránky systému RAPEX dočasně odstraněno, dokud se posouzení rizik oznámeného výrobku nevyjasní.
3.4.7.2.2 Žádost členských států o dočasné odstranění oznámení
Komise může oznámení z aplikace RAPEX dočasně odstranit pouze na žádost oznamujícího členského státu, neboť ten je plně odpovědný za informace předávané prostřednictvím této aplikace. Komise nicméně vyzývá ostatní členské státy, aby ji informovaly o veškerých skutečnostech, které by mohly toto odstranění odůvodnit.
3.4.7.2.3 Obsah žádosti o dočasné odstranění oznámení
Ke každé žádosti o dočasné odstranění oznámení je třeba přiložit odůvodnění, v němž se uvedou důvody této žádosti, a veškeré dostupné doklady na jejich podporu. Komise přezkoumá každou žádost a zkontroluje zejména odůvodnění a podpůrné doklady. Komise si může předtím, než přijme rozhodnutí, vyžádat doplňující informace, vysvětlení nebo stanovisko oznamujícího členského státu nebo jiných členských států.
3.4.7.2.4 Rozhodnutí o odstranění oznámení
Pokud se na základě poskytnutého odůvodnění Komise rozhodne, že oznámení z internetové stránky systému RAPEX odstraní, informuje o tom všechny členské státy prostřednictvím elektronické pošty nebo jiných stejně účinných prostředků, v případě nutnosti informuje také veřejnost zveřejněním opravy na internetové stránce systému RAPEX.
3.4.7.2.5 Opětovné zveřejnění dočasně odstraněného oznámení
Oznamující členský stát informuje Komisi ihned poté, co pominou důvody pro odstranění oznámení z internetové stránky systému RAPEX. Komisi zejména sdělí výsledky nově provedených posouzení rizik, aby jí umožnil určit, zda má zachovat oznámení v aplikaci RAPEX a znovu ho zveřejnit na internetové stránce systému, nebo zda jej má z aplikace RAPEX natrvalo stáhnout (na žádost oznamujícího členského státu).
Po vyjasnění posouzení rizik může Komise na odůvodněnou žádost oznamujícího členského státu opět zveřejnit oznámení na internetové stránce systému RAPEX.
Komise informuje ostatní členské státy o opětovném zveřejnění oznámení na internetové stránce systému RAPEX prostřednictvím elektronické pošty nebo jiných stejně účinných prostředků a rovněž informuje veřejnost tím, že na internetové stránce systému RAPEX nahradí původní opravu opravou novou.
3.4.8 Oznámení starší než deset let
Komise přemístí všechna oznámení, která jsou starší než deset let, do samostatného oddílu internetových stránek systému RAPEX. Tato oznámení budou veřejnosti ještě k dispozici k nahlédnutí.
3.5 Načasování a lhůty pro oznámení
3.5.1 Načasování oznámení
Podle čl. 12 odst. 1 směrnice o obecné bezpečnosti výrobků a článku 22 nařízení (ES) č. 765/2008 musí členské státy prostřednictvím aplikace RAPEX neprodleně oznámit Komisi preventivní a omezující opatření týkající se výrobků, které představují vážná rizika. Toto ustanovení platí jak pro povinná, tak pro dobrovolná opatření, i když načasování oznámení se liší.
a) Povinná opatření
Tato opatření se prostřednictvím aplikace RAPEX oznamují ihned poté, co byla přijata nebo co bylo rozhodnuto o jejich přijetí, i když pravděpodobně budou nebo již jsou předmětem odvolání na vnitrostátní úrovni nebo podléhají požadavkům na zveřejnění.
Tento přístup odpovídá cíli systému RAPEX, tj. zajistit rychlou výměnu informací mezi členskými státy a Komisí, aby se zamezilo dodávkám a používání výrobků, které představují riziko.
b) Dobrovolná opatření
Podle čl. 5 odst. 3 směrnice o obecné bezpečnosti výrobků a článku 22 nařízení (ES) č. 765/2008 jsou hospodářské subjekty povinny oznámit příslušným orgánům členského státu dobrovolné akce a opatření, které provedly k zabránění rizikům, jež pro spotřebitele představují výrobky, které dodaly na trh (nejlépe prostřednictvím oznámení přes „bránu pro podniky“ („Business Gateway“)). Orgán členského státu, který obdrží tento druh oznámení, tuto informaci použije jako základ pro oznámení (jsou-li splněna všechna kritéria oznamování), které ihned po obdržení oznámení prostřednictvím brány pro podniky („Business Gateway“) odešle.
Pokud se dobrovolná opatření přijímají ve formě dohody mezi hospodářským subjektem a orgánem členského státu nebo na základě doporučení výrobci nebo distributorovi od některého orgánu, zašle se oznámení ihned po uzavření takové dohody nebo po přijetí daného doporučení.
Aby se zajistilo společné uplatňování oznamovací povinnosti, stanoví část III dodatek 4 těchto pokynů konkrétní lhůty pro předkládání oznámení Komisi prostřednictvím aplikace RAPEX (32).
3.5.2 Lhůty (33)
Členské státy předkládají přijatá preventivní a omezující opatření Komisi co nejdříve, nejpozději ve lhůtách stanovených v části III dodatku 4 těchto pokynů. Na vnitrostátní úrovni byla přijata příslušná opatření týkající se předávání informací mezi vnitrostátními orgány odpovědnými za bezpečnost výrobků a kontaktním místem RAPEX, aby se zajistilo dodržování požadovaných lhůt (viz část II kapitola 5.1).
Uvedené lhůty platí nezávisle na jakémkoli odvolání nebo na požadavku na úřední zveřejnění.
3.5.3 Naléhavé situace
Všem oznámením, která se týkají výrobků představujících vážné riziko a která vyžadují okamžitou akci, předchází telefonát kontaktního místa RAPEX na číslo mobilního telefonu týmu Komise odpovědného za systém RAPEX s cílem usnadnit okamžitou akci a stanovit následná opatření. Toto pravidlo platí zejména pro oznámení předávaná během víkendů nebo dovolených. (Viz též část II kapitola 5.1).
4 Následné kroky
4.1 Informace o následných krocích
Členské státy informují Komisi o veškerých zjištěních v návaznosti na následné činnosti, které provedly v souvislosti s oznámeními v systému RAPEX (tj. „oznámeními podle článku 12“ a „oznámeními vyžadujícími okamžitou akci“ i oznámeními podle článku 22 nařízení (ES) č. 765/2008) a informacemi o výrobcích představujících riziko, které jim zaslala Komise (kapitola 3.3.4).
Členské státy se dále vyzývají, aby Komisi informovaly o všech následných činnostech týkajících se oznámení v případě nižších než vážných rizik a oznámení pro informaci.
4.2 Obsah následných oznámení
4.2.1 Rozsah údajů
Výsledky následných činností se Komisi sdělují ve formě následných oznámení. Aby se sladil druh podávaných informací a pracovní zátěž omezila na minimum, předkládají členské státy následná oznámení zejména za těchto situací:
a) Nalezení oznámeného výrobku na trhu
Následná oznámení se zasílají ve chvíli, kdy vnitrostátní orgány najdou oznámený výrobek na trhu nebo na vnějších hranicích. Toto následné oznámení obsahuje podrobné údaje o dotčeném výrobku (např. jeho název, značku, číslo modelu, čárový kód, číslo výrobní série) a informace o celkovém počtu kusů nalezených na trhu. Dále se uvádějí tyto podrobné informace o přijatých opatřeních: typ (povinná nebo dobrovolná), kategorie (např. stažení z trhu, zpětné převzetí od spotřebitelů), působnost (např. celostátní, místní), datum vstupu v platnost a doba trvání (např. trvalé, dočasné). Pokud byl oznámený výrobek na trhu nalezen, ale nebyla přijata žádná opatření, je třeba v následném oznámení uvést konkrétní důvody pro toto nepřijetí.
Aby se snížilo zatížení vnitrostátních orgánů, pokud jde o jejich následné činnosti, nemusí členské státy Komisi informovat prostřednictvím následného oznámení o výsledcích následných činností, pokud nebyl oznámený výrobek na trhu nalezen (ledaže si Komise informace vyžádá).
b) Odlišné posouzení rizik
Následné oznámení se zasílá ve chvíli, kdy se závěry posouzení rizik provedeného orgánem reagujícího členského státu liší od závěrů uvedených v původním oznámení. Toto následné oznámení obsahuje podrobný popis rizika (včetně výsledků testů, posouzení rizik a informací o známých nehodách a incidentech) spolu s doprovodnými doklady (protokoly o zkouškách, certifikáty atd.). Reagující členský stát by navíc měl prokázat, že posouzení rizik předkládané v následném oznámení bylo provedeno u výrobku shodného s oznámeným výrobkem, tj. u výrobku stejné značky, stejného názvu, čísla modelu, čísla výrobní série, původu atd.
c) Doplňující informace
Následné oznámení se zasílá ve chvíli, kdy vnitrostátní orgány shromáždí doplňující informace (během svých následných činností), které by mohly být užitečné pro dozor nad trhem a vynucování v dalších členských státech.
Členské státy se vyzývají, aby shromažďovaly doplňující informace, které by mohly mít význam pro orgány jiných členských států i třetích zemí, které s EU v oblasti bezpečnosti výrobků úzce spolupracují. K těmto informacím patří údaje o původu výrobku (např. informace o zemi původu, výrobci a/nebo vývozcích) a informace o dodavatelských řetězcích (např. informace o zemích určení, dovozcích a distributorech). Země provádějící následné činnosti přikládá k následnému oznámení veškerou doprovodnou dokumentaci, kterou má k dispozici, jako jsou kopie objednávek, kupní smlouvy, faktury, celní prohlášení atd.
Členské státy mohou rovněž uvést, zda byla provedena určitá následná opatření, i když na jejich území nebyl výrobek nalezen.
4.2.2 Úplnost následných oznámení
Kontaktní místo RAPEX reagujícího členského státu spolu s odpovědným vnitrostátním orgánem zajistí, že všechny údaje poskytované v následném oznámení jsou přesné a úplné a že nedojde k záměně s jinými podobnými výrobky, které jsou dostupné na trhu EU. (Viz též část II kapitola 5.1).
Standardní formulář pro následné oznámení je uveden v části III dodatku 2 těchto pokynů. Nejsou-li při předkládání následného oznámení některé důležité informace k dispozici, musí to reagující členský stát ve formuláři následného oznámení uvést. Jakmile jsou tyto informace k dispozici, může reagující členský stát požádat o aktualizaci svého následného oznámení. Komise aktualizované následné oznámení zkontroluje předtím, než ho potvrdí a prostřednictvím systému rozšíří.
Kontaktní místo RAPEX poskytuje všem orgánům ve svém členském státě, které jsou zapojené do sítě RAPEX, pokyny ohledně rozsahu údajů požadovaných pro správné vyplnění formuláře pro následné oznámení. To pomůže zajistit správnost a úplnost informací, které tyto orgány kontaktnímu místu poskytnou. (Viz část II kapitola 5.1).
4.2.3 Aktualizace potvrzení následných oznámení
Reagující členský stát informuje Komisi (co nejdříve a nejpozději ve lhůtě stanovené v části III dodatku 4 těchto pokynů) o každém vývoji, který vyžaduje provedení změn v následném oznámení šířeném prostřednictvím aplikace RAPEX. Členské státy Komisi zejména oznámí změny statusu přijatých opatření nebo změny provedené v posouzení rizik předkládaném spolu s následným oznámením.
Komise přezkoumá informace, které jí poskytl reagující členský stát, a případně provede aktualizaci dotčených informací.
4.2.4 Odpovědnost za následná oznámení
Odpovědnost za informace poskytnuté v následných oznámeních nese oznamující členský stát (34).
Odpovědnost za informace poskytnuté v následných oznámeních nese orgán zapojený do následných činností (např. tím, že provádí posouzení rizik nebo přijímá omezující opatření). Kontaktní místo RAPEX zkontroluje a potvrdí všechna následná oznámení připravená příslušnými orgány před jejich předáním Komisi. (Viz též část II kapitola 5.1).
Žádné kroky podniknuté Komisí, jako je zkoumání a potvrzování následných oznámení, neznamenají převzetí odpovědnosti za předávané informace, kterou nadále nese členský stát předkládající následné oznámení.
4.2.5 Reakce na následná oznámení
Členské státy mohou reagovat na případná následná oznámení týkající se jejich vlastních oznámení zahájením diskuse v on-line prostoru pro spolupráci, který mají členské státy k dispozici pro výměnu informací (viz část II kapitola 5.3.2). Tím se zajistí, že je reakce viditelná pro všechny členy systému RAPEX.
4.3 Subjekty zapojené do následných činností a jejich úlohy
Strany zapojené do postupu následného oznamování a jejich úkoly:
4.3.1 Hospodářské subjekty (35)
Hospodářské subjekty nejsou přímo zapojené do předkládání následných oznámení. Hospodářské subjekty však musí spolupracovat s vnitrostátními orgány a poskytovat jim veškeré informace týkající se výrobku, který je předmětem stávajícího oznámení, s cílem usnadnit vypracování a předkládání následných oznámení prostřednictvím aplikace RAPEX.
4.3.2 Orgány dozoru nad trhem
Orgány dozoru nad trhem informují Evropskou komisi prostřednictvím aplikace RAPEX o veškerých následných činnostech nebo dalších informacích týkajících se oznámení.
4.3.3 Evropská komise
Evropská komise přezkoumá a potvrdí následná oznámení podle specifikací obsažených v části II kapitole 4.2.
4.4 Pracovní postup
4.4.1 Vypracování a předložení následného oznámení členským státem
Za předložení následných oznámení prostřednictvím aplikace RAPEX je odpovědné kontaktní místo RAPEX. (Viz část II kapitola 5.1).
4.4.2 Zkoumání následných oznámení Komisí
4.4.2.1
Komise zkontroluje všechna následná oznámení, která obdrží prostřednictvím aplikace RAPEX, než je potvrdí a předá členským státům. Tyto kontroly jsou zaměřeny na správnost a úplnost poskytnutých informací.
Komise zkontroluje, zda následné opatření splňuje všechny příslušné požadavky stanovené ve směrnici o obecné bezpečnosti výrobků a v těchto pokynech a zda byl dodržen správný postup. Po potvrzení správnosti následného oznámení Komise zkontroluje jeho úplnost. Pro tuto kontrolu se jako referenční bod použije kapitola 4.2.2 těchto pokynů.
Komise věnuje zvláštní pozornost následným oznámením obsahujícím posouzení rizik. Zejména ověřuje, zda je popis rizika úplný, jasně formulovaný a řádně doložený a zda se posouzení rizik skutečně týká výrobku uvedeného v oznámení.
4.4.2.2
Před potvrzením následného oznámení může Komise požadovat, aby jí reagující členský stát ve stanovené lhůtě poskytl doplňující informace nebo vysvětlení. Potvrzení následného oznámení může být podmíněno obdržením požadovaných údajů.
Komise může požadovat stanovisko kteréhokoli členského státu na potvrzené následné oznámení, zejména oznamujícího členského státu. Členský stát předloží své stanovisko Komisi ve lhůtě, kterou Komise stanoví. Oznamující členský stát navíc informuje Komisi o tom, zda je nutno provést změny oznámení (např. v posouzení rizik) nebo jeho statusu (např. trvalé stažení oznámení ze systému).
4.4.3 Potvrzování a šíření následných oznámení
Komise potvrdí a rozšíří všechna následná oznámení, která byla vyhodnocena jako správná a úplná, ve lhůtě uvedené v dodatku 5 těchto pokynů.
Komise nepotvrdí následná oznámení, u nichž se posouzení rizik liší od posouzení rizik uvedeného v oznámení, jehož se týkají, pokud není posouzení rizik úplné, jasně formulované a řádně doložené a pokud není zřejmé, že se skutečně týká výrobku uvedeného v oznámení.
4.4.4 Trvalé stažení následného oznámení ze systému RAPEX
Následná oznámení šířená prostřednictvím aplikace RAPEX jsou v systému ponechána stejně dlouhou dobu jako oznámení, k němuž se vztahují. Komise může potvrzené následné oznámení z aplikace RAPEX natrvalo stáhnout, pokud bylo ze systému RAPEX staženo oznámení, k němuž se toto následné oznámení vztahuje (v souladu s částí II kapitolou 3.4.7.1.1 těchto pokynů). Komise může dále stáhnout potvrzené následné oznámení, pokud jasně uvádí nesprávné informace a zejména pokud:
|
a) |
výrobek, který reagující členský stát nalezl na svém trhu, je jiný než výrobek uvedený v oznámení, |
|
b) |
opatření, která přijal reagující členský stát, byla úspěšně napadena v soudním nebo jiném řízení a následně stažena, |
|
c) |
se prokázalo, že posouzení rizik, které provedl reagující členský stát, je nesprávné nebo se vztahuje k jinému výrobku než k tomu, který je uveden v oznámení. |
Použijí se ustanovení kapitol 3.4.7.1.2 a 3.4.7.1.3.
Poté, co Komise rozhodne o stažení následného oznámení, je následné oznámení ze systému RAPEX odstraněno (nebo je jinak zajištěno, aby ho uživatelé systému neviděli).
Komise informuje všechny členské státy o stažení následného oznámení prostřednictvím on-line prostoru pro spolupráci uvedeného v části II kapitole 5.3.2 nebo pomocí jiných stejně účinných prostředků.
4.5 Lhůty pro předkládání následných oznámení
Členské státy předkládají následná oznámení Komisi co nejdříve, nejpozději ve lhůtě stanovené v dodatku 4 těchto pokynů.
Na vnitrostátní úrovni jsou zavedena příslušná opatření týkající se předávání informací mezi všemi příslušnými orgány a kontaktním místem RAPEX, aby se zajistilo dodržení požadovaných lhůt. (Viz část II kapitola 5.1).
Uvedené lhůty platí nezávisle na jakémkoli řízení o opravném prostředku nebo na požadavku na úřední zveřejnění.
4.6 Žádosti o zachování důvěrnosti
Reagující členský stát může ve svém následném oznámení uvést, že požaduje zachování důvěrnosti. Ve své žádosti musí jasně uvést, kterých částí následného oznámení se má důvěrnost týkat. Každý požadavek na zachování důvěrnosti je navíc doplněn vysvětlením, v němž se jasně uvádějí důvody tohoto požadavku.
Žádosti o zachování důvěrnosti přezkoumává Komise, která určí, zda je žádost oprávněná (tj. v souladu s ustanoveními směrnice o obecné bezpečnosti výrobků a těchto pokynů) a úplná (tj. uvádí, na které části formuláře se vztahuje pravidlo o zachování důvěrnosti a zda obsahuje odůvodnění). Po konzultaci odpovědného kontaktního místa RAPEX vydá Komise závěrečné rozhodnutí o zachování důvěrnosti. (Viz část II kapitola 5.1).
Komise a členské státy nakládají s následnými oznámeními obsahujícími požadavek na zachování důvěrnosti stejným způsobem jako s jinými následnými opatřeními. Důvěrnost následného oznámení nebo jeho částí nebrání tomu, aby byla prostřednictvím aplikace RAPEX předána příslušným vnitrostátním orgánům. Komise ani členské státy by však neměly veřejnosti poskytnout žádné části následného oznámení, které jsou důvěrné. Tyto informace jsou důvěrné, tudíž je nelze v žádné formě zveřejnit.
Členský stát předkládající následné oznámení stáhne svůj požadavek na zachování důvěrnosti ihned poté, co zjistí, že oprávněnost takového požadavku již neplatí. Poté, co Komise od reagujícího členského státu obdrží žádost o stažení požadavku na zachování důvěrnosti, informuje všechny členské státy o jeho stažení.
5 Sítě RAPEX
5.1 Vnitrostátní kontaktní místa RAPEX
Každý členský stát zřídí jedno kontaktní místo RAPEX s cílem provozovat systém RAPEX na vnitrostátní úrovni. Členské státy rozhodnou, pod kterým vnitrostátním orgánem kontaktní místo RAPEX zřídí. Každý členský stát rovněž uspořádá svou vnitrostátní síť RAPEX tak, aby zajistil efektivní výměnu informací mezi vnitrostátním kontaktním místem a různými orgány zapojenými do systému RAPEX. (Viz část I kapitola 5.4 a část II kapitola 1.2).
5.1.1 Organizace
Každý členský stát poskytne vnitrostátnímu kontaktnímu místu zdroje a informace, které potřebuje k provádění svých úkolů, zejména k provozování systému s účinnou zpětnou vazbou / kontinuitou činnosti.
Kontaktní místo RAPEX má svou samostatnou elektronickou adresu pro účast v systému RAPEX, k níž mají přístup všichni pracovníci kontaktního místa (např. rapex@…). Pracovní nebo soukromé elektronické adresy úředníků, kteří jsou odpovědní za provoz kontaktního místa RAPEX, by se neměly používat jako elektronická adresa kontaktního místa RAPEX. Kontaktní místo RAPEX má rovněž přímé telefonní číslo, jehož prostřednictvím je dosažitelné během pracovní doby i po jejím skončení.
5.1.2 Úkoly
Hlavními úkoly kontaktního místa RAPEX jsou:
|
a) |
organizovat a řídit práci vnitrostátní sítě RAPEX v souladu s pravidly stanovenými v těchto pokynech, |
|
b) |
školit orgány zapojené do sítě v používání systému RAPEX a být jim nápomocné, |
|
c) |
zajistit, aby byly řádně prováděny všechny úkoly systému RAPEX vyplývající ze směrnice o obecné bezpečnosti výrobků a těchto pokynů, zejména neprodlené poskytování požadovaných informací Komisi (tj. oznámení, následných oznámení, doplňujících informací atd.), |
|
d) |
předávat informace mezi Komisí a vnitrostátními orgány dozoru nad trhem a orgány provádějícími kontroly na vnějších hranicích, |
|
e) |
kontrolovat a potvrzovat úplnost informací, které obdrží od všech orgánů, před jejich předáním Komisi prostřednictvím aplikace RAPEX, |
|
f) |
před předáním oznámení zkontrolovat, zda již nebyl výrobek oznámen nebo zda v aplikaci RAPEX neproběhla výměna informací o tomto výrobku (aby se zamezilo duplicitě), |
|
g) |
účastnit se zasedání pracovní skupiny pro kontaktní místa RAPEX a dalších akcí souvisejících s fungováním systému RAPEX, |
|
h) |
navrhovat možná zlepšení fungování systému, |
|
i) |
informovat neprodleně Komisi o veškerých technických problémech s fungováním aplikace RAPEX, |
|
j) |
koordinovat veškeré vnitrostátní činnosti a iniciativy podniknuté v souvislosti se systémem RAPEX, |
|
k) |
vysvětlovat zainteresovaným subjektům fungování systému RAPEX a jejich povinnosti, zejména povinnost obchodního oznámení stanovenou v čl. 5 odst. 3 směrnice o obecné bezpečnosti výrobků. |
5.2 Sítě RAPEX zřízené na úrovni EU a na vnitrostátní úrovni
5.2.1 Síť kontaktních míst RAPEX
Komise organizuje a řídí práci sítě kontaktních míst RAPEX. Tato síť se skládá ze všech kontaktních míst RAPEX zřízených v jednotlivých členských státech a zemích Evropského hospodářského prostoru (EHP).
Komise pravidelně svolává zasedání sítě kontaktních míst RAPEX s cílem projednat fungování systému (např. informovat o nejnovějším vývoji v souvislosti se systémem RAPEX, vyměňovat si zkušenosti a know-how) a zlepšit spolupráci mezi kontaktními místy RAPEX.
5.2.2 Sítě RAPEX zřízené na vnitrostátní úrovni
Kontaktní místa RAPEX organizují a řídí práci své „vnitrostátní sítě RAPEX“. Tuto síť tvoří:
|
a) |
kontaktní místo RAPEX, |
|
b) |
orgány dozoru nad trhem, které jsou odpovědné za monitorování bezpečnosti výrobků, a |
|
c) |
orgány provádějící kontroly na vnějších hranicích. |
Kontaktní místa RAPEX se vyzývají, aby zajistily organizaci a fungování vnitrostátní sítě RAPEX tak, aby všechny zainteresované orgány znaly své úkoly a povinnosti při provozování systému RAPEX. To by mělo být v souladu s informacemi obsaženými v těchto pokynech.
Kontaktní místa RAPEX se vyzývají, aby usnadňovala pravidelnou výměnu informací a diskuse se svými vnitrostátními sítěmi, aby se tak se všemi zainteresovanými orgány jednalo o organizaci a fungování systému RAPEX, a v případě potřeby pořádala kurzy odborné přípravy.
5.3 Nástroje RAPEX pro vnitřní komunikaci, praktická a technická opatření pro systém RAPEX a osvědčené postupy
5.3.1 Jazyky
Používání jazyků v oznámeních a následných oznámeních i ve sděleních vyměňovaných mezi kontaktními místy RAPEX a Komisí musí zohledňovat cíle systému RAPEX a musí zajistit rychlou výměnu informací mezi členskými státy a Komisí o výrobcích, které představují vážné riziko.
S cílem zjednodušit práci sítě se orgány členských států vyzývají, aby používaly stávající internetové stránky Evropské komise eTranslation, aby se zajistilo, že všechny členské státy porozumí všemu, co je prostřednictvím systému RAPEX sdělováno.
V on-line prostoru pro spolupráci je k dispozici odkaz na tento překladatelský nástroj, pomocí kterého je možné předkládat dokumenty nebo úryvky z textů k překladu ze všech a do všech jazyků EU (36). (Viz část II kapitola 5.3.2).
5.3.2 On-line nástroje RAPEX
a) Systém RAPEX
Komise zřídila a udržuje internetovou aplikaci, která se používá jako komunikační nástroj pro účely systému RAPEX. Členské státy používají tento systém k vytváření a předkládání oznámení a následných oznámení prostřednictvím aplikace RAPEX a Komise ho používá k potvrzování a šíření dokumentů, které obdržela.
Komise umožňuje přístup k systému všem kontaktním místům RAPEX, odpovědným vnitrostátním orgánům a příslušným útvarům Komise. Stanoví pravidla pro poskytování přístupu k systému a s ohledem na potřeby a technické možnosti umožňuje přístup co největšímu počtu uživatelů.
Pokud systém RAPEX dočasně nefunguje (z jiných důvodů, než je pravidelná a plánovaná údržba), měly by členské státy zasílat Komisi pouze oznámení o vážných rizicích (tj. „oznámení podle článku 12“, „oznámení podle článku 12 vyžadující okamžitou akci“ nebo „oznámení podle článku 22 nařízení (ES) č. 765/2008“).
Předkládání dalších oznámení a následných oznámení se pozastavuje, dokud není fungování systému RAPEX obnoveno. Po dobu, co systém nefunguje, posílají se oznámení RAPEX Komisi elektronickou poštou na adresu: [email protected] nebo na jinou předem uvedenou adresu. Pokud není předání elektronickou poštou možné, zasílají se oznámení RAPEX Komisi jakýmkoli jiným prostředkem, který se považuje za vhodný (37).
b) Brána pro varování ze strany podniků ohledně bezpečnosti výrobků („Product Safety Business Alert Gateway“)
Účelem „brány pro varování ze strany podniků ohledně bezpečnosti výrobků“ („Product Safety Business Alert Gateway“, také známé jako „brána pro podniky“ („Business Gateway“)) je zjednodušit praktické aspekty povinnosti, kterou mají výrobci a distributoři nebo jejich pověřený zástupce podle čl. 5 odst. 3 směrnice o obecné bezpečnosti výrobků, informovat příslušné vnitrostátní orgány členských států, pokud je jim na základě informací, které mají k dispozici, nebo jako odborníkům známo nebo by mělo být známo, že výrobek, který uvedli na trh, je nebezpečný.
„Bránu pro podniky“ („Business Gateway“) tvoří dvě složky: i) formulář pro oznámení a ii) on-line databáze. Formulář pro oznámení je určen pouze výrobcům a distributorům, aby mohli na základě své povinnosti podle čl. 5 odst. 3 směrnice o obecné bezpečnosti výrobků informovat příslušné vnitrostátní orgány členských států, že výrobek, který uvedli na trh, je nebezpečný. On-line databáze je určena vnitrostátním orgánům členských států, které mají odpovědnost za přijímání oznámení o nebezpečných spotřebních výrobcích předložených výrobci a distributory. Jsou-li splněna všechna kritéria, může příslušný orgán členského státu použít poskytnuté informace k předložení oznámení v systému RAPEX.
c) On-line prostor pro spolupráci
Komise spravuje také on-line prostor pro spolupráci, jenž slouží pro výměnu informací mezi Komisí a příslušnými vnitrostátními orgány členských států. Tento portál obsahuje platformu EU pro bezpečnost spotřebních výrobků (EU Consumer Product Safety Platform), která je v souvislosti se všemi záležitostmi týkajícími se systému RAPEX otevřena pracovníkům kontaktních míst RAPEX a jejich kolegům, kteří se v příslušných vnitrostátních orgánech zabývají otázkami bezpečnosti výrobků. Žádost o přístup k on-line prostoru musí podat kontaktní místa RAPEX v příslušném členském státě a schválit Komise.
Tento prostor obsahuje také oddíl spravovaný Komisí s užitečnými tipy a informacemi o fungování systému RAPEX a vstupy členských států.
d) „Nástroj RAG“ (38)
Komise vyvinula tento nástroj, který k dispozici na internetových stránkách systému RAPEX, s cílem usnadnit posuzování rizik u výrobků oznámených prostřednictvím systému RAPEX v souladu se zásadami stanovenými v dodatku 6.
5.3.3 Kontaktní údaje
Komise poskytne kontaktním místům RAPEX kontaktní údaje týmu Komise odpovědného za systém RAPEX, včetně jmen, e-mailových adres a telefonních čísel.
Kontaktní místa RAPEX poskytnou Komisi své kontaktní údaje, včetně jmen interních pracovníků, názvu a adresy orgánu, pod nímž je kontaktní místo RAPEX zřízeno, e-mailových adres a telefonních čísel pracovníků. Kontaktní místo RAPEX Komisi neprodleně oznámí veškeré změny kontaktních údajů. Komise zveřejní a aktualizuje kontaktní údaje kontaktních míst RAPEX na internetové stránce RAPEX.
Členské státy zpracovávají kontaktní údaje včetně osobních údajů s ohledem na právní předpisy EU v oblasti ochrany údajů. Při výměně informací prostřednictvím systému RAPEX by členské státy měly při zpracování osobních údajů zajistit, aby byly šířeny a předávány jen v nezbytně nutném rozsahu.
5.3.4 Fungování systému RAPEX mimo pravidelnou pracovní dobu
Systém RAPEX funguje nepřetržitě. Komise a kontaktní místa RAPEX zajistí, aby pracovníci odpovědní za provoz systému RAPEX byli vždy k dosažení (prostřednictvím telefonu, elektronické pošty nebo jiných stejně účinných prostředků) a schopni provést jakýkoli nezbytný úkon včetně naléhavých případů a mimo pravidelnou pracovní dobu, např. o víkendech a svátcích.
Komise poskytne kontaktním místům RAPEX telefonní číslo pro naléhavé situace, aby bylo možné kontaktovat tým Komise odpovědný za systém RAPEX mimo pracovní dobu, které má přednost před jinými komunikačními prostředky.
Kontaktní místa RAPEX sdělí Komisi své kontaktní údaje, včetně telefonních čísel úředníků, které lze kontaktovat během pracovní doby i mimo ni. Kontaktní místa RAPEX Komisi neprodleně oznámí veškeré změny kontaktních údajů.
ČÁST III
DODATKY
1. Kolonky a informace obsažené v oznámeních (39)
Kolonky, které budou zveřejněny na internetu, jsou podbarveny šedě.
|
Oznamovací formulář |
|
|
Oddíl 1: Obecné informace |
|
|
Věc č. |
|
|
Datum vytvoření |
|
|
Datum potvrzení/rozšíření |
|
|
Typ oznámení* |
|
|
Oznamující země |
|
|
Úplné kontaktní údaje oznamujícího orgánu* |
|
|
Oddíl 2: Výrobek |
|
|
Profesionální/spotřební výrobek |
|
|
Kategorie výrobku* |
|
|
Kategorie podle portálu OECD (pokud jsou známy) |
|
|
Výrobek (co výrobek představuje)* |
|
|
Název* |
|
|
Značka* |
|
|
Typ/číslo modelu: * |
|
|
Číslo výrobní série/čárový kód* |
|
|
Celní kód* |
|
|
Popis výrobku a obalu* |
|
|
Celkový počet kusů uvedených v oznámení (je-li znám)* |
|
|
Fotografie: |
|
|
Oddíl 3: Platné předpisy a normy |
|
|
Právní ustanovení (směrnice, rozhodnutí, nařízení atd.)* |
|
|
Normy* |
|
|
Prokázání shody* |
|
|
Je výrobek padělaný? * |
|
|
Osvědčení |
|
|
Oddíl 4: Sledovatelnost |
|
|
Země původu (kde byl výrobek zhotoven)* |
|
|
Země určení* |
|
|
Úplné kontaktní údaje výrobce nebo jeho zástupce (zástupců)* |
|
|
Úplné kontaktní údaje vývozce (vývozců)* |
|
|
Úplné kontaktní údaje dovozce (dovozců)* |
|
|
Úplné kontaktní údaje distributora (distributorů)* |
|
|
Úplné kontaktní údaje obchodníka (obchodníků)* |
|
|
Je výrobek prodáván (také) on-line? |
|
|
Uveďte podrobnosti: Adresa URL |
|
|
Oddíl 5: Posouzení rizik |
|
|
Kategorie rizika* |
|
|
Úroveň rizika |
|
|
Souhrn výsledků testů* |
|
|
Popis technického problému, který vede k největšímu riziku |
|
|
Popis rizika (jak vede technická vada k riziku)* |
|
|
Právní ustanovení a/nebo normy EU, podle nichž byl výrobek testován a které nesplnil* |
|
|
Informace o známých nehodách a incidentech* |
|
|
Oddíl 6: Opatření |
|
|
Druh přijatých opatření* |
|
|
U dobrovolných opatření: |
Druh hospodářského subjektu přijímajícího oznámená opatření* |
|
Název hospodářského subjektu přijímajícího oznámená opatření* |
|
|
U povinných opatření: |
Název orgánu, který ukládá oznámená opatření* |
|
Druh hospodářského subjektu, kterému bylo opatření uloženo* |
|
|
Kategorie opatření* |
|
|
Datum vstupu v platnost* |
|
|
Doba trvání* |
|
|
Rozsah* |
|
|
Bylo oznámení zasláno výrobcem nebo distributorem podle čl. 5 odst. 3 směrnice o obecné bezpečnosti výrobků? * |
|
|
Adresa URL na stránku společnosti o stažení výrobku z oběhu (je-li k dispozici) |
|
|
Oddíl 7: Důvěrnost |
|
|
Je oznámení důvěrné?* |
|
|
Rozsah důvěrnosti |
|
|
Odůvodnění |
|
|
Oddíl 8: Ostatní |
|
|
Další informace |
|
|
Důvody pro zaslání „oznámení pro informaci“ |
|
|
Přílohy |
|
|
Fotografie (výrobky, obal a etiketa) |
|
|
Osvědčení |
|
|
Protokol o zkouškách a posouzení rizik |
|
|
Oznámení odeslané hospodářským subjektem prostřednictvím „brány pro podniky“ („Business Gateway“) |
|
|
Přijatá opatření |
|
|
* Označuje povinné kolonky. |
|
2. Kolonky a informace obsažené v následných oznámeních (40)
Kolonky, které budou zveřejněny na internetu, jsou podbarveny šedě.
|
Oddíl 1: Obecné informace |
|
|
Věc č. |
|
|
Potvrzený typ oznámení |
|
|
Oznamující země |
|
|
Datum vytvoření |
|
|
Datum potvrzení/rozšíření |
|
|
Číslo podání |
|
|
Číslo následného oznámení |
|
|
Reagující země |
|
|
Úplné kontaktní údaje oznamujícího orgánu |
|
|
Kategorie výrobku potvrzeného oznámení |
|
|
Oznamovaný výrobek |
|
|
Oznamovaný název |
|
|
Výrobek (co výrobek je) |
|
|
Název (na výrobku nebo obalu) |
|
|
Značka (na výrobku nebo obalu) |
|
|
Typ/číslo modelu |
|
|
Číslo výrobní série / čárový kód (nebo jiné informace, na jejichž základě lze určit, o jaké výrobky se jedná) |
|
|
Fotografie (výrobky, obal a etiketa) |
|
|
Oddíl 2: Typ následného oznámení |
|
|
Nalezený výrobek* |
|
|
Celkový počet nalezených kusů (je-li znám)* |
|
|
Přijatá opatření / nepřijatá opatření |
|
|
Druh přijatých opatření: * |
|
|
U dobrovolných opatření: |
Druh hospodářského subjektu přijímajícího oznámená opatření* |
|
Název hospodářského subjektu přijímajícího oznámená opatření* |
|
|
U povinných opatření: |
Název orgánu, který ukládá oznámená opatření* |
|
Druh hospodářského subjektu, kterému bylo opatření uloženo* |
|
|
Kategorie opatření* |
|
|
Datum vstupu v platnost* |
|
|
Doba trvání* |
|
|
Rozsah* |
|
|
Přijatá opatření |
|
|
Adresa URL na stránku společnosti o stažení výrobku z oběhu (je-li k dispozici) |
|
|
Odlišné posouzení rizik* |
|
|
Kategorie rizika* |
|
|
Souhrn výsledků testů (popis technických vad)* |
|
|
Údaje o právních ustanoveních a normách (s doložkami), podle nichž byl výrobek testován* |
|
|
Odlišné posouzení rizik* |
|
|
Informace o známých nehodách a incidentech* |
|
|
Přílohy (certifikáty, protokol o zkouškách a posouzení rizik...) |
|
|
Další informace* |
|
|
Doplňující informace o distribučních kanálech a/nebo původu výrobků |
|
|
Doplňující informace o posouzení rizik |
|
|
Další doplňující informace |
|
|
Oddíl 3: Důvěrnost |
|
|
Je reakce důvěrná? * |
|
|
Rozsah důvěrnosti |
|
|
Odůvodnění |
|
|
Přílohy |
|
|
Fotografie (výrobek, obal a etiketa) |
|
|
Protokoly o zkouškách a posouzení rizik |
|
|
Osvědčení |
|
|
Přijatá opatření |
|
|
* Označuje povinné kolonky. |
|
3. Systém oznamování
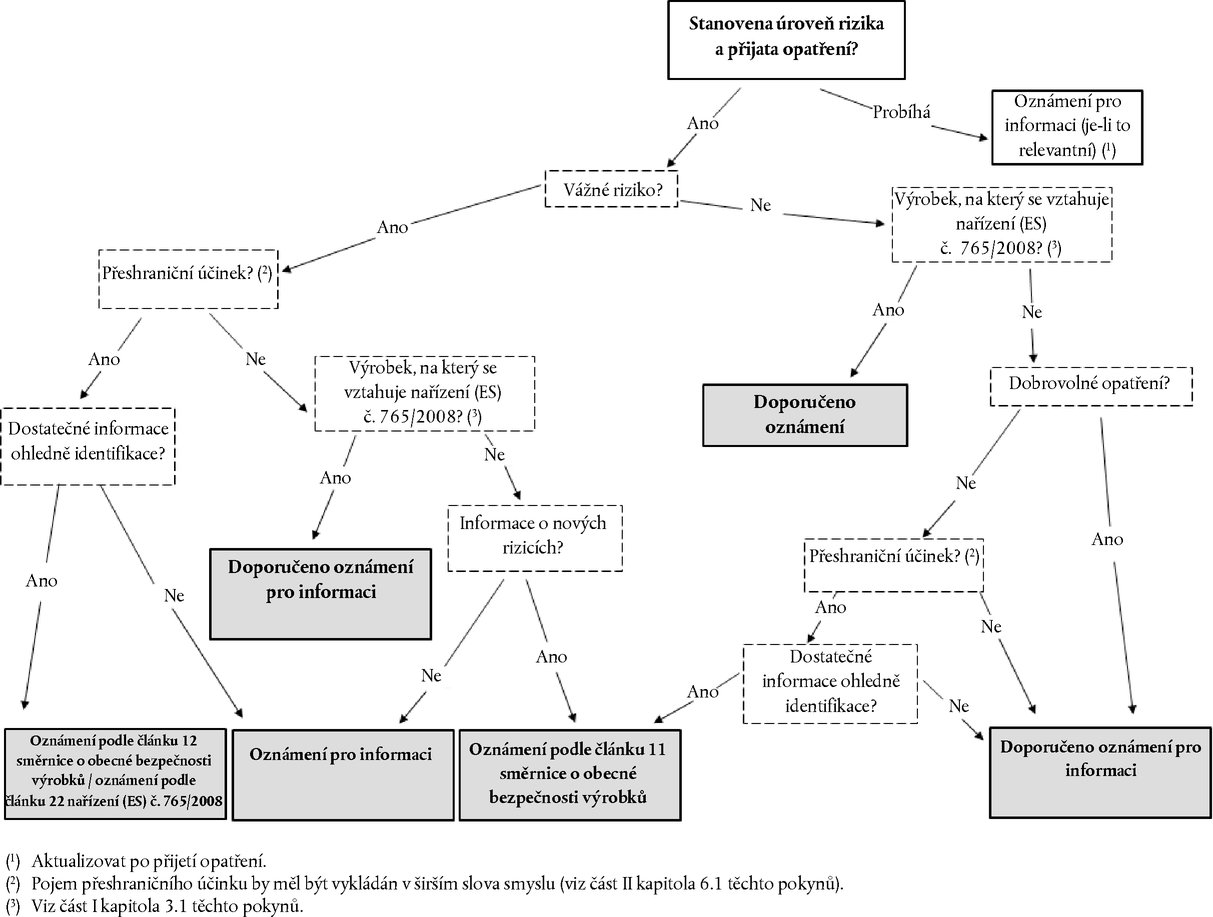
Oznámení podle článku 12 směrnice o obecné bezpečnosti výrobků / oznámení podle článku 22 nařízení (ES) č. 765/2008
Oznámení podle článku 11 směrnice o obecné bezpečnosti výrobků
Přeshraniční účinek? (2)
Výrobek, na který se vztahuje nařízení (ES) č. 765/2008? (3)
Oznámení pro informaci (je-li to relevantní) (1)
Dostatečné informace ohledně identifikace?
Doporučeno oznámení
Informace o nových rizicích?
Doporučeno oznámení pro informaci
Výrobek, na který se vztahuje nařízení (ES) č. 765/2008? (3)
Doporučeno oznámení pro informaci
Stanovena úroveň rizika a přijata opatření?
Dostatečné informace ohledně identifikace?
Oznámení pro informaci
Přeshraniční účinek? (2)
Dobrovolné opatření?
Vážné riziko?
Ne
Ano
Ne
Ne
Ne
Ano
Ne
Ne
Ne
Probíhá
Ano
Ne
Ano
Ano
Ne
Ano
Ano
Ano
Ano
Ano
(1) Aktualizovat po přijetí opatření.
(2) Pojem přeshraničního účinku by měl být vykládán v širším slova smyslu (viz část II kapitola 6.1 těchto pokynů).
(3) Viz část I kapitola 3.1 těchto pokynů.
4. Lhůty pro členské státy
Členské státy musí jednat ve stanovených lhůtách, není-li jejich překročení řádně odůvodněno
|
Postup oznamování |
Akce |
Lhůta |
||||||
|
|
Oznámení |
Zaslat „oznámení podle článku 12 vyžadující okamžitou akci“ |
Do tří dnů po:
|
|||||
|
Zaslat oznámení podle článku 12 nebo článku 22 nařízení (ES) č. 765/2008 |
Do deseti dnů po:
|
|||||||
|
Potvrdit opatření, pokud bylo oznámení zasláno před rozhodnutím o přijetí opatření |
Do 45 dnů po předložení oznámení |
|||||||
|
Aktualizace oznámení |
Do pěti dnů po přijetí informací o vývoji vyžadujícím změny v oznámení |
|||||||
|
Následná oznámení |
Zajistit následné kroky k: |
„oznámení podle článku 12 vyžadujícímu okamžitou akci“ |
Do 20 dnů po přijetí oznámení |
|||||
|
„oznámení podle článku 12“ a „oznámení od Evropské komise“, jakož i oznámení podle článku 22 nařízení (ES) č. 765/2008 |
Do 45 dnů po přijetí oznámení |
|||||||
|
Zaslat následné oznámení k: |
„oznámení podle článku 12 vyžadující okamžitou akci“ |
Do tří dnů po:
|
||||||
|
„oznámení podle článku 12“ a „oznámení od Evropské komise“, jakož i oznámení podle článku 22 nařízení (ES) č. 765/2008 |
Do pěti dnů po:
|
|||||||
|
Aktualizace následného oznámení |
Do pěti dnů po přijetí informací o vývoji vyžadujícím změny v následném oznámení |
|||||||
|
Postup oznamování stanovený podle článku 11 směrnice o obecné bezpečnosti výrobků |
Oznámení |
Zaslat „oznámení podle článku 11“ |
Do deseti dnů po přijetí „povinných opatření“ |
|||||
|
Aktualizace oznámení |
Do pěti dnů po přijetí informací o vývoji vyžadujícím změny v oznámení |
|||||||
5. Lhůty pro Komisi
|
Postup oznamování |
Akce |
Lhůta |
|
|
Systém EU pro rychlou výměnu informací „RAPEX“ zřízený podle článku 12 směrnice o obecné bezpečnosti výrobků |
Oznámení |
Potvrdit „oznámení podle článku 12 vyžadující okamžitou akci“ |
Do tří dnů po přijetí oznámení |
|
Potvrdit „oznámení podle článku 12“ jakož i oznámení podle článku 22 nařízení (ES) č. 765/2008 |
Do pěti dnů po přijetí oznámení |
||
|
Potvrdit „oznámení pro informaci“ |
Do deseti dnů po přijetí oznámení |
||
|
Následná oznámení |
Potvrdit následná oznámení zaslaná k „oznámení podle článku 12 vyžadujícímu okamžitou akci“ |
Do tří dnů po přijetí následného oznámení |
|
|
Potvrdit následné oznámení zaslané k „oznámení podle článku 12“ a k „oznámení od Evropské komise“, jakož i oznámení podle článku 22 nařízení (ES) č. 765/2008 |
Do pěti dnů po přijetí následného oznámení |
||
|
Potvrdit následné oznámení zaslané k „oznámení pro informaci“ |
Do deseti dnů po přijetí následného oznámení |
||
|
Postup oznamování stanovený podle článku 11 směrnice o obecné bezpečnosti výrobků |
Oznámení |
Potvrdit „oznámení podle článku 11“ |
Do deseti dnů po přijetí oznámení |
|
Následná oznámení |
Potvrdit následná oznámení zaslaná k „oznámení podle článku 11“ |
Do deseti dnů po přijetí následného oznámení |
|
POKYNY PRO POSUZOVÁNÍ RIZIK U SPOTŘEBNÍCH VÝROBKŮ (41)
1. Úvod
Spotřební výrobky mohou při svém používání způsobit škodu na zdraví; například horká žehlička může přivodit popáleniny, o nůžky nebo nože se můžeme pořezat a čisticí prostředek pro domácnost může poškodit kůži. K těmto druhům poškození obvykle nedochází, protože díky všeobecným znalostem nebo návodům víme, jak spotřební výrobky používat bezpečně. Riziko poškození nicméně nadále existuje.
Toto riziko lze posoudit různými způsoby. Pro kvantifikaci rizika u spotřebních výrobků se používá řada metod, například metoda nomogramu (42), maticová metoda (43) či metoda dříve doporučovaná pro systém včasného varování EU RAPEX (44). Zatímco na obecných zásadách posuzování rizik vždy existovala shoda, způsoby kvantifikace rizik se neustále vyvíjejí. Tato skutečnost vede k rozdílnosti výsledků a následným diskuzím, jakož i k úvahám o tom, jak by mohl vypadat optimální postup.
Účelem těchto pokynů k posouzení rizika je tedy tuto situaci zlepšit a v rámci směrnice o obecné bezpečnosti výrobků (45) nabídnout transparentní a prakticky použitelnou metodu, kterou by měly při posuzování rizik nepotravinářských spotřebních výrobků vhodně využívat příslušné orgány členských států. Tyto pokyny vycházejí z metody posuzování rizik, která byla vyvinuta pro jiné účely a přizpůsobena specifickým požadavkům nepotravinářských spotřebních výrobků.
Před zavedením pokynů do praxe bude samozřejmě zapotřebí určitého školení, ale tento úkol bude výrazně usnadněn stávajícími odbornými znalostmi v oblasti posuzování rizik. Podporu budou představovat také výměny názorů mezi posuzovateli rizik, protože odbornost a zkušenosti získané za řadu let mají neocenitelný význam.
Tyto pokyny předkládají metodu posuzování rizik v malých, zvladatelných krocích, a tím pomáhají zaměřit se na významné otázky týkající se výrobku, jeho uživatelů a jeho použití a přispívají k tomu, aby byly hned na začátku zjištěny možné rozdíly mezi názory různých posuzovatelů rizik, a aby tedy nebylo nutné vést časově náročné diskuze. Díky tomu by měly vést ke konzistentním a věrohodným výsledkům posouzení rizik, založeným na důkazech a vědeckém poznání, a v důsledku toho také k široce přijatelnému konsenzu o rizicích, která mohou být spojena s mnoha nepotravinářskými spotřebními výrobky.
V oddílu 5 je uveden stručný přehled a vývojový diagram ukazující, jak vypracovat posouzení rizik v souladu s těmito pokyny. „Spotřebními výrobky“ se v těchto pokynech vždy rozumějí nepotravinářské spotřební výrobky.
Tyto pokyny nemají nahradit jiné pokyny, které se mohou týkat velice specifických výrobků nebo mohou být výslovně stanoveny v právních předpisech, například pro oblast chemických látek, kosmetiky, farmaceutických výrobků nebo zdravotnických prostředků. Používání takových zvláštních pokynů se důrazně doporučuje, protože jsou konkrétně uzpůsobeny pro svůj předmět, ale rozhodnout o tom, jak nejlépe posoudit rizika spojená s určitým výrobkem, musí vždy posuzovatel.
Tyto pokyny by rovněž neměli používat výrobci „jen proto, aby se vyhnuli vážným rizikům“ při navrhování a výrobě výrobků. Spotřební výrobky musí být bezpečné a cílem těchto pokynů je pomáhat příslušným orgánům se zjišťováním vážných rizik v případech, kdy výrobek navzdory veškerému úsilí výrobce bezpečný není.
2. Posuzování rizik – přehled
2.1. Riziko – kombinace nebezpečí a pravděpodobnosti
Riziko se obvykle chápe jako něco, co ohrožuje zdraví, či dokonce životy lidí, nebo něco, co může způsobit značnou hmotnou škodu. Lidé však i při vědomí možné škody riskují, protože ke škodě ve skutečnosti vždy nedochází. Příklady:
|
— |
Lezení po žebříku je vždy spojeno s možností pádu a úrazu. „Pád“ je tudíž „zabudován do žebříku“; je neoddělitelnou součástí používání žebříku a nelze jej vyloučit. „Pád“ se proto označuje jako vnitřní nebezpečí (intrinsic hazard) žebříku. |
|
— |
Toto nebezpečí se ovšem neprojeví vždy, protože mnoho lidí žebříky používá, aniž by spadli a zranili se. Z toho vyplývá, že existuje určitá pravděpodobnost, ale nikoli jistota, že se vnitřní nebezpečí projeví. Toto nebezpečí existuje vždy, ale pravděpodobnost, že se projeví, je možné minimalizovat, například opatrností člověka, který žebřík používá. |
|
— |
Používání čisticího prostředku pro domácnost, který obsahuje hydroxid sodný, k uvolnění ucpaných odpadních trubek je vždy spojeno s možností velmi těžkého poškození kůže, pokud se s ní výrobek dostane do kontaktu, či dokonce trvalého oslepnutí v případě, že se kapky výrobku dostanou do oka. Důvodem je skutečnost, že hydroxid sodný je vysoce žíravá látka, a to znamená, že daný čisticí prostředek je svou podstatou nebezpečný. |
Pokud se ovšem s čisticím prostředkem správně zachází, nebezpečí se neprojeví. Správné zacházení může znamenat použití plastových rukavic a ochranných brýlí. V takovém případě jsou oči a kůže chráněny a pravděpodobnost poškození se výrazně sníží.
Riziko je tedy kombinace závažnosti možného poškození spotřebitele a pravděpodobnosti, že toto poškození nastane.
2.2. Posouzení rizik ve třech krocích
Pro stanovení rizika je třeba provést tři kroky:
|
1. |
Anticipovat scénář poškození zdraví, při němž vnitřní nebezpečí výrobku způsobí škodu na zdraví spotřebitele (viz tabulka 1). Stanovit závažnost poškození zdraví spotřebitele. Měřítkem pro kvantifikaci vnitřního nebezpečí výrobku je rozsah nepříznivého účinku, který může mít na zdraví spotřebitele. Posuzovatel rizik tedy anticipuje „scénář poškození zdraví“, který v jednotlivých krocích popisuje, jak nebezpečí vede k poškození zdraví spotřebitele (viz tabulka 2). Stručně řečeno, scénář poškození zdraví popisuje nehodu, která se spotřebiteli stane s dotyčným výrobkem, a závažnost poškození, které tato nehoda spotřebiteli způsobí. Poškození zdraví může mít různou závažnost v závislosti na nebezpečnosti výrobku, na způsobu jeho použití spotřebitelem, na typu spotřebitele, který výrobek používá, a na mnoha dalších faktorech (viz oddíl 3). Čím je poškození zdraví vážnější, tím vážnější je nebezpečí, které je způsobilo, a naopak. „Závažnost poškození zdraví“ je tudíž prostředkem ke kvantifikaci nebezpečí. V těchto pokynech se navrhuje rozlišovat 4 stupně závažnosti, od poškození zdraví, která jsou obvykle zcela vratná, až po velmi vážná poškození zdraví, která způsobí trvalou invaliditu v rozsahu větším než přibližně 10 %, či dokonce smrt (viz tabulka 3). |
|
2. |
Stanovit pravděpodobnost, že vnitřní nebezpečí výrobku v praxi skutečně poškodí zdraví spotřebitele. Scénář poškození zdraví popisuje, jakým způsobem nebezpečí poškodí zdraví spotřebitele, ale tento scénář nastane pouze s určitou pravděpodobností. Tuto pravděpodobnost lze vyjádřit v procentech nebo zlomkem, například „> 50 %“ nebo „> 1/1 000“ (viz levá strana tabulky 4). |
|
3. |
Stanovit riziko na základě kombinace nebezpečí (stanoveného podle závažnosti poškození zdraví) a pravděpodobnosti (vyjádřené zlomkem). Tuto kombinaci lze určit vyhledáním obou hodnot v příslušné tabulce (viz tabulka 4); tabulka udává úrovně rizika, které jsou označeny jako „vážné“, „vysoké“, „střední“ a „nízké“ riziko. Pokud je možné předvídat různé scénáře poškození zdraví, mělo by být určeno riziko pro každý scénář a nejvyšší zjištěné riziko je třeba označit jako „rizikovost“ výrobku. Nejvyšší riziko má obvykle zásadní význam, protože vysokou úroveň ochrany lze účinně zajistit jedině opatřením proti nejvyššímu riziku. Na druhé straně může být zjištěno riziko, které je nižší než nejvyšší riziko, ale přesto vyžaduje zvláštní opatření ke snížení rizik. V takovém případě je důležité přijmout rovněž opatření proti tomuto riziku, aby byla účinně snížena všechna rizika. Po provedení uvedených tří kroků je posouzení rizik v podstatě hotové. Diagram pro provedení posouzení rizika se nachází na konci oddílu 5. |
2.3. Několik užitečných rad
Vyhledání informací
Jak je patrné z příkladů uvedených v kapitole 2.1, vyžaduje každý z tří uvedených kroků posouzení rizik (viz bod 2.2) schopnost předvídat, co se může stát a s jakou pravděpodobností se to stane, protože posuzovaný výrobek obvykle ještě nezpůsobil žádnou nehodu, a příslušné riziko se tedy (zatím) neprojevilo. V tomto procesu jsou užitečné předchozí zkušenosti s obdobnými výrobky a také veškeré další informace o výrobku, například o jeho konstrukci, mechanické stabilitě, chemickém složení a provozu, návod k použití včetně případných pokynů k řízení rizik, informace o typech spotřebitelů, pro které je výrobek určen (a pro které určen není), jakož i protokoly o zkouškách, statistiky nehod, informace z Evropské databáze úrazů (IDB) (46) či informace o stížnostech spotřebitelů, o chování různých spotřebitelů při používání výrobku a o stažení výrobků z oběhu. Užitečnými zdroji informací mohu být také požadavky na výrobky stanovené v právních předpisech, v normách pro výrobky nebo v kontrolních seznamech (například podle normy ISO 14121: Bezpečnost strojních zařízení – posouzení rizika).
Posuzované výrobky však mohou být dosti specifické, a tyto zdroje proto nemusí potřebné informace obsahovat. Shromážděné informace také mohou být neúplné, rozporné nebo ne zcela věrohodné. Tak tomu může být zejména u statistik nehod, jsou-li v nich evidovány pouze kategorie výrobků. Pokud chybí historie nehod nebo pokud je počet nehod malý nebo nejsou závažné, neměl by být tento fakt chápán jako předpoklad nízkého rizika. Ale i na statistiky o jednotlivých výrobcích je třeba pohlížet s velkou opatrností, protože výrobek se mohl v čase změnit, například z hlediska konstrukce nebo složení. Informace je vždy nutné kriticky posoudit.
Zvláště užitečná může být zpětná vazba od ostatních odborníků, protože ti mohou čerpat ze svých praktických zkušeností a podat doporučení, která při posuzování určitého rizika spojeného s výrobkem nejsou bezprostředně zřejmá. Mohou také poradit s posouzením rizik pro jiné typy spotřebitelů, včetně zranitelných spotřebitelů, například dětí (viz tabulka 1), poněvadž ti mohou s výrobkem zacházet odlišně. Současně mohou pomoci s posouzením rizik různých poškození zdraví, která může výrobek způsobit, a způsobů, jak používání výrobku k těmto poškozením vede. Kromě toho mohou posoudit, zda scénář poškození zdraví není „zcela nerealistický“, tedy příliš nepravděpodobný, a následně posuzovatele rizik nasměrovat k realističtějším předpokladům.
Zpětná vazba od zkušených kolegů tak sice není povinná, ale může být v několika směrech prospěšná. Posuzovatel rizik z orgánu veřejné správy může požádat o radu mimo jiné kolegy ze stejného orgánu, z jiných orgánů, z průmyslu, z jiných zemí či z vědeckých uskupení. Naopak každý posuzovatel rizik v průmyslu může využít svých kontaktů s veřejnými orgány a dalšími subjekty, když má před uvedením na trh posoudit nový či vylepšený výrobek.
Nově získané informace by se samozřejmě vždy měly použít k aktualizaci stávajícího posouzení rizik.
Provedení analýzy citlivosti posouzení rizik
Jestliže veškeré vyhledávání informací a dotazy na ostatní odborníky nevedou k získání požadovaných velice specifických údajů, může pomoci takzvaná analýza citlivosti. V rámci této analýzy se pro každý parametr posouzení rizik dosadí nižší a vyšší hodnota, než jaká byla zvolena předtím, a provede se s ní celý postup posouzení rizik. Výsledné úrovně rizika ukáží, jak citlivě úroveň rizika reaguje na zadání nižších a vyšších hodnot. Tímto způsobem je možné odhadnout rozmezí, ve kterém se bude nacházet skutečná rizikovost výrobku.
Pokud lze odhadnout nejpravděpodobnější hodnotu pro každý parametr, je třeba postup provést s těmito nejpravděpodobnějšími hodnotami a výsledná úroveň rizika bude představovat nejpravděpodobnější riziko.
V oddílu 6 je analýza citlivosti vysvětlena na příkladu.
Kontrola posouzení rizik jinými odborníky
Zpětná vazba od kolegů bude užitečná také při dokončování posouzení rizik. Kolegové totiž budou moci poradit ohledně předpokladů a odhadů použitých ve třech krocích zmíněných v bodu 2.2. Přispějí svými zkušenostmi, a tím napomohou ke vzniku spolehlivějšího, solidnějšího, transparentnějšího a v konečném důsledku také přijatelnějšího posouzení rizik. Proto se v ideálním případě doporučuje poradit se před dokončením posouzení rizik s dalšími odborníky, například formou skupinové diskuze. Příslušné skupiny, které by mohly mít 3 až 5 členů, by měly zahrnovat odborníky se znalostmi odpovídajícími posuzovanému výrobku: techniky, chemiky, (mikro)biology, statistiky, manažery bezpečnosti výrobků a další. Skupinová diskuze bude zvláště užitečná, je-li výrobek na trhu nový a nebyl dosud nikdy posuzován.
Posouzení rizik by měla být solidní a realistická. Protože však vyžadují řadu předpokladů, mohou různí posuzovatelé rizik dospět k různým závěrům podle toho, jaké údaje a další důkazy se jim podařilo shromáždit, nebo kvůli svým odlišným zkušenostem. Proto je nezbytné, aby spolu posuzovatelé rizik komunikovali za účelem dosažení shody nebo alespoň určitého konsenzu. Posouzení rizik v jednotlivých krocích popsané v těchto pokynech by však mělo zvýšit produktivitu těchto diskuzí. Každý krok posouzení rizik je nutné jasně a podrobně popsat. Jakékoli sporné body tak mohou být rychle identifikovány a konsenzu může být dosaženo snadněji. Výsledkem budou přijatelnější posouzení rizik.
Dokumentace posouzení rizik
Posouzení rizik je důležité dokumentovat, včetně popisu výrobku a všech parametrů zvolených při vypracování posouzení, jako jsou výsledky zkoušek, typy spotřebitelů zvolené pro scénáře poškození zdraví a hodnoty pravděpodobnosti podkladových údajů a předpokladů. To vám umožní jednoznačně demonstrovat, jak jste odhadli úroveň rizika, a pomůže vám to rovněž udržovat si přehled o všech změnách, když budete posouzení aktualizovat.
Několik nebezpečí, několik poškození zdraví – ale jen jedno riziko
Pokud je zjištěno několik nebezpečí, několik scénářů poškození zdraví nebo různé stupně závažnosti poškození zdraví či různé hodnoty pravděpodobnosti, měl by být pro každou z těchto alternativ proveden celý postup posouzení rizik s cílem stanovit riziko pro každou z nich. V důsledku toho může mít výrobek několik úrovní rizika. Celková rizikovost výrobku pak odpovídá nejvyšší zjištěné úrovni rizika, protože nejúčinnějším způsobem snížení rizika je obvykle opatření proti riziku nejvyšší úrovně. Pouze ve zvláštních případech může být nižší než nejvyšší riziko považováno za zvláště důležité, protože může vyžadovat specifická opatření pro řízení rizik.
Jako příklad několika rizik je možné uvést kladivo, které může mít nedostatečně pevnou hlavu i nedostatečně pevné topůrko a obě tyto součásti se mohou při používání kladiva rozlomit a zranit spotřebitele. Jestliže příslušné scénáře vedou k různým úrovním rizika, za „rizikovost“ kladiva se označí nejvyšší riziko.
Je možné tvrdit, že:
|
— |
rozhodující by mělo být zjevně nejvýznamnější nebezpečí, protože to by způsobilo nejvážnější poškození zdraví. V příkladu s kladivem v bodu 2.1 by mohlo jít o rozlomení hlavy kladiva, poněvadž části zlomené hlavy mohou uživateli vletět do očí a případně jej i oslepit. Na druhé straně zlomené topůrko se nikdy neroztříští na malé části, které by mohly oči tak výrazně poškodit, |
|
— |
toto by ovšem bylo posouzení nebezpečí, a nikoli posouzení rizik. Posouzení rizik se zabývá také pravděpodobností, že k poškození zdraví skutečně dojde. „Nejvýznamnější nebezpečí“ tak může způsobit poškození zdraví s mnohem menší pravděpodobností než některé menší nebezpečí, a tudíž může představovat nižší riziko. Naopak scénář vedoucí k méně vážnému poškození zdraví může být mnohem pravděpodobnější než scénář vedoucí ke smrti, a toto méně závažné poškození proto může představovat vyšší riziko, |
|
— |
rozhodujícím faktorem z hlediska „rizikovosti“ výrobku by měla být nejvyšší pravděpodobnost, že se scénář poškození zdraví uskuteční. V příkladu s kladivem v bodu 2.1 to znamená, že je-li topůrko velmi slabé, nejpravděpodobnější scénář poškození zdraví bude spočívat ve zlomení topůrka, a to by tedy mělo být rozhodující. |
Tato úvaha by ovšem nezahrnovala závažnost poranění očí, která by mohlo způsobit rozlomení hlavy kladiva. Zkoumání samotné pravděpodobnosti by proto neposkytlo úplný obrázek.
Z toho vyplývá, že riziko je vyváženou kombinací jednak nebezpečí a jednak pravděpodobnosti poškození zdraví, k němuž může nebezpečí vést. Rizikem se nepopisuje nebezpečí ani pravděpodobnost, nýbrž oboje současně. Tím, že se nejvyšší riziko bude považovat za „rizikovost“ výrobku, bude bezpečnost výrobků zajištěna nejúčinněji (s výjimkou zvláštních rizik vyžadujících zvláštní řízení rizik, jak je uvedeno na začátku tohoto oddílu).
Mohou se rizika kumulovat?
Prakticky u každého výrobku je možné vypracovat několik scénářů poškození zdraví vedoucích k několika rizikům. Úhlová bruska může například představovat riziko úrazu elektrickým proudem kvůli nedostatečně chráněným elektrickým vodičům a současně riziko požáru, protože se přístroj může během běžného používání přehřát a vznítit. Jestliže se obě tato rizika pokládají za „vysoká“, vede jejich spojení k tomu, že bruska celkově představuje „vážné riziko“?
Je-li s jedním výrobkem spojeno několik rizik, je pochopitelně pravděpodobnější, že se jedno z nich projeví a způsobí poškození zdraví. Celková pravděpodobnost poškození zdraví je proto větší. To ovšem neznamená, že celková rizikovost je automaticky vyšší:
|
— |
celková pravděpodobnost se nevypočítá prostým součtem jednotlivých pravděpodobností. Nutné jsou složitější výpočty, jejichž výsledkem je vždy pravděpodobnost nižší než součet všech jednotlivých pravděpodobností. |
|
— |
Mezi dvěma po sobě jdoucími úrovněmi pravděpodobnosti existuje desetinásobný rozdíl (tabulka 4). To znamená, že k vyšší celkové pravděpodobnosti (případně riziku) by vedl jedině velký počet různých scénářů se stejnou úrovní pravděpodobnosti. |
|
— |
Hodnoty pravděpodobnosti jsou odhady, které nemusí být úplně přesné, protože u nich kvůli zajištění vysoké úrovně ochrany často dochází k chybě ve prospěch větší bezpečnosti. Z toho důvodu je užitečnější zabývat se přesnějším odhadem pravděpodobnosti scénáře vedoucího k nejvyššímu riziku než sčítat hrubé odhady pravděpodobnosti nejrůznějších scénářů. |
|
— |
S trochou snahy je možné vypracovat stovky scénářů poškození zdraví. Pokud by se rizika prostě sčítala, celkové riziko by záviselo na počtu vypracovaných scénářů poškození zdraví a mohlo by se zvyšovat „donekonečna“. To by nedávalo smysl. |
Prostá kumulace rizik se tedy neprovádí. Jestliže však existuje několik významných rizik, opatření pro jejich řízení může být nutné přijmout rychleji nebo může být nutné, aby byla tato opatření důraznější. Například existují-li dvě rizika, může být nezbytné výrobek okamžitě stáhnout z trhu i z oběhu, zatímco v případě jediného rizika může postačovat zastavení prodeje.
Řízení rizik závisí na mnoha faktorech, nejen na počtu rizik, která může výrobek v jednom okamžiku představovat. Proto se věnujeme souvislosti mezi rizikem a řízením rizik (oddíl 4).
Dodržování mezních hodnot v právních předpisech a normách
Při výkonu dozoru nad trhem se u spotřebních výrobků často zkouší, zda splňují mezní hodnoty nebo požadavky stanovené v právních předpisech a normách pro bezpečnost výrobků. U výrobku, který splňuje mezní hodnoty či požadavky (47), se předpokládá, že je bezpečný z hlediska bezpečnostních parametrů, kterých se tyto hodnoty nebo požadavky týkají. Tento předpoklad je možné učinit proto, že rizika, která výrobek představuje při svém zamýšleném a rozumně předvídatelném používání, byla vzata v úvahu při stanovování mezních hodnot nebo požadavků. Výrobci tak musí zajistit, aby jejich výrobky splňovaly tyto hodnoty nebo požadavky, protože pak se musí u svých výrobků zabývat pouze riziky, kterých se tyto mezní hodnoty či požadavky netýkají.
Příkladem mezní hodnoty
|
— |
v právním předpisu je limit 5 mg/kg benzenu v hračkách, který se nesmí překročit podle bodu 5 přílohy XVII nařízení REACH5 (48) ve znění nařízení Komise (ES) č. 552/2009 (49), |
|
— |
v normě je válec pro malé části: malé části hračky určené pro děti mladší 36 měsíců se nesmějí celé vejít do válce popsaného v normě pro hračky (50). V opačném případě představují riziko, |
|
— |
jestliže výrobek nesplňuje stanovené mezní hodnoty, předpokládá se, že není bezpečný. Pokud jde o mezní hodnoty stanovené |
|
— |
v právních předpisech, například o kosmetických prostředcích nebo o omezeních uvádění na trh a používání, výrobek se nesmí dodávat na trh, |
|
— |
v normách, může se výrobce přesto pokusit formou úplného posouzení rizik svého výrobku prokázat, že je daný výrobek tak bezpečný, jako by mezní hodnotu uvedenou v normě splňoval. To ovšem může vyžadovat více úsilí (a může to být nemožné v případech, jako je válec pro malé části uvedený v první odrážce tohoto výčtu) než výroba výrobku v souladu s mezní hodnotou podle normy. |
Nedodržení mezních hodnot automaticky neznamená, že výrobek představuje „vážné riziko“ (což je nejvyšší úroveň rizika podle těchto pokynů). Aby bylo zajištěno přijetí vhodných opatření ke snížení rizik, bude se proto vyžadovat posouzení rizik u těch částí výrobku, které porušují právní předpis nebo normu nebo se na ně právní předpisy ani normy nevztahují.
Kromě toho se u některých výrobků, například kosmetických prostředků, vyžaduje posouzení rizik i v případě, že mezní hodnoty stanovené v právních předpisech splňují. Toto posouzení rizik by mělo prokázat bezpečnost celého výrobku (51).
Z výše uvedeného vyplývá, že dodržení mezních hodnot stanovených v právních předpisech nebo normách znamená předpoklad bezpečnosti, ale přesto nemusí být dostatečné.
Zvláštní pokyny pro posuzování rizik ve zvláštních případech
Pro chemické látky existují zvláštní pokyny k vypracování posouzení rizik (52), a proto se jim tyto pokyny podrobně nevěnují. Postupuje se nicméně podle stejných zásad jako u „běžných“ spotřebních výrobků:
|
— |
identifikace a posouzení nebezpečnosti – to odpovídá stanovení závažnosti poškození zdraví, jak je popsáno v oddíle 2.2, |
|
— |
posouzení expozice – v tomto kroku se vyjádří expozice jako pravděpodobná dávka chemické látky, kterou může spotřebitel zvlášť nebo společně absorbovat orální, inhalační nebo dermální cestou při používání výrobku způsobem předpokládaným ve scénáři poškození zdraví. Tento krok odpovídá určení pravděpodobnosti, že k poškození zdraví skutečně dojde, |
|
— |
charakterizace rizika – tento krok v podstatě spočívá v porovnání dávky chemické látky, kterou spotřebitel pravděpodobně absorbuje, (= expozice) s odvozenou úrovní, při které nedochází k nepříznivým účinkům, (DNEL) dané chemické látky. Pokud je expozice dostatečně nižší než DNEL, jinými slovy je-li míra charakterizace rizika (RCR) zřetelně nižší než 1, kontrola rizika se pokládá za dostatečnou. Toto odpovídá stanovení úrovně rizika. Jestliže je úroveň rizika dostatečně nízká, opatření pro řízení rizik nemusí být zapotřebí. |
Jelikož chemická látka může představovat několik nebezpečí, obvykle se stanovuje riziko pro „hlavní účinek na zdraví“, což je účinek na zdraví (nebo „koncový bod“, jako je akutní toxicita, dráždivost, senzibilizace, karcinogenita, mutagenita či toxicita pro reprodukci) pokládaný za nejdůležitější.
Existují také zvláštní pokyny pro kosmetické prostředky (53) a zvláštní pokyny mohou existovat i pro jiné výrobky či jiné účely.
Používání takovýchto zvláštních pokynů se důrazně doporučuje, protože jsou konkrétně uzpůsobeny pro dotyčné zvláštní případy. Pokud ovšem údaje vyžadované zvláštními pokyny nejsou k dispozici ani je nelze odhadnout, mohou být pro předběžné posouzení rizik použity tyto pokyny. Takové posouzení rizik bude nutné provést s náležitou péčí a pozorností, aby se předešlo nesprávným výkladům.
3. Sestavování posouzení rizik v jednotlivých krocích
V tomto oddílu jsou podrobně popsány body, které je třeba vzít v úvahu, a otázky, které je třeba položit při přípravě posouzení rizik.
3.1 Výrobek
Výrobek by měl být jednoznačně identifikován. Sem patří název výrobku, značka, název modelu, číslo typu, případně číslo výrobní šarže, osvědčení, s nímž může být výrobek dodáván, případný uzávěr odolný proti otevření dětmi, totožnost osoby, která výrobek uvedla na trh, a země původu. Za součást popisu výrobku lze považovat také fotografii výrobku, jeho obalu a (případně) typového štítku, jakož i protokoly o zkouškách informující o nebezpečích výrobku.
V konkrétních případech se nebezpečí může týkat pouze určité části výrobku, která od něj může být oddělena a také samostatně nabízena spotřebitelům. V takových případech postačí posoudit jen tuto část výrobku. Příkladem jsou dobíjecí baterie přenosných počítačů, které se mohou přehřívat.
Popis výrobku zahrnuje veškeré štítky, které mohou mít význam pro posouzení rizik, zejména upozornění na nebezpečí. Také návody k použití mohou obsahovat relevantní informace o rizicích výrobku a způsobech jejich minimalizace, kupříkladu používáním osobních ochranných prostředků nebo tím, že se v používání výrobku zabrání dětem. Tak je tomu například u řetězové pily.
Některé výrobky, například stavebnicový nábytek, si musí spotřebitelé před použitím sami sestavit. V takovém případě je třeba se ptát, zda je návod k sestavení natolik jasný, aby výrobek připravený k použití mohl splňovat všechny příslušné bezpečnostní požadavky. Nebo se mohou spotřebitelé při montáži výrobku dopustit chyb, které by mohly vést k nepředvídaným rizikům?
Posouzení rizik by se vždy mělo zabývat celou dobou životnosti výrobku. To je zvláště důležité, posuzují-li se rizika spojená s nově vyvinutým výrobkem. Změní se druh nebo rozsah nebezpečí v důsledku stárnutí a používání? Povede stárnutí výrobku nebo případně jeho rozumně předvídatelné nevhodné používání k novým nebezpečím? Jak dlouhá je „doba bezporuchového fungování výrobku“? Jaká je životnost výrobku včetně skladovací trvanlivosti? Jak dlouho je výrobek v praxi používán spotřebitelem, než se z něj stane odpad?
Další aspekty může být nutné zvážit u výrobků, které jsou po určité době nepoužitelné, i když nebyly nikdy použity. To se týká například elektricky vyhřívaných přikrývek či ohřívacích podušek. Tyto výrobky mají obvykle tenké elektrické kabely, které po deseti letech začnou být křehké, i když se výrobek nikdy nepoužíval. Topné kabely se pak mohou dotknout, způsobit zkrat a zapálit ložní prádlo.
Konečně by každé posouzení rizik mělo zahrnovat také obal výrobku.
3.2 Nebezpečí výrobku
Nebezpečím se rozumí vnitřní vlastnost výrobku, která může poškodit zdraví spotřebitele, který výrobek používá. Nebezpečí může mít různé podoby:
|
— |
mechanické nebezpečí, například ostré hrany, které mohou pořezat prsty, nebo úzké otvory, ve kterých se mohou prsty zachytit, |
|
— |
nebezpečí udávení, například to, které představují malé části, které se oddělí od hračky, dítě je může spolknout a udávit se, |
|
— |
nebezpečí udušení, například stahovacími šňůrami v kapuci větrovky, které mohou vést k uškrcení, |
|
— |
elektrické nebezpečí, dané například částmi pod napětím, které mohou způsobit úraz elektrickým proudem, |
|
— |
nebezpečí zahřátí či požáru, například u ventilátoru topného tělesa, který se přehřívá, může začít hořet a způsobit popáleniny, |
|
— |
tepelné nebezpečí, například horký vnější povrch trouby, který může způsobit popáleniny, |
|
— |
chemické nebezpečí, například u toxické látky, kterou se může spotřebitel otrávit bezprostředně po požití, nebo u karcinogenní látky, která může po delší době vyvolat zhoubný nádor. Některé chemické látky mohou spotřebitele poškodit teprve po opakované expozici, |
|
— |
mikrobiologické nebezpečí, například bakteriální kontaminace kosmetických prostředků, které mohou způsobit infekci kůže, |
|
— |
nebezpečí hluku, například nadměrně hlasité vyzváněcí tóny u hraček v podobě mobilních telefonů, které mohou poškodit sluch dětí, |
|
— |
jiná nebezpečí, například výbuch, imploze, zvukový a ultrazvukový tlak, tlak tekutiny nebo záření zdrojů laserového světla. |
Pro účely těchto pokynů byla nebezpečí rozdělena do skupin podle toho, zda souvisejí s velikostí, tvarem či povrchem výrobku, s potenciální, kinetickou nebo elektrickou energií, s extrémními teplotami či jinými faktory, jak je uvedeno v tabulce 2. Tabulka má sloužit jen jako vodítko a každý posuzovatel rizik by měl příslušný scénář přizpůsobit posuzovanému výrobku. Všechny druhy nebezpečí se samozřejmě netýkají každého výrobku.
Tabulka 2 by přesto měla posuzovatelům rizik pomoci s vyhledáním a identifikací všech možných nebezpečí u spotřebních výrobků, které posuzují. Pokud výrobek představuje několik nebezpečí, je pro každé z nich třeba vypracovat vlastní posouzení rizik a nejvyšší zjištěné riziko pak považovat za „rizikovost“ výrobku. Aby bylo možné snížit všechna rizika, je samozřejmě třeba uvést také rizika vyžadující zvláštní opatření pro řízení rizik.
Všimněte si, že jedno nebezpečí může vést k několika poškozením zdraví v rámci stejného scénáře. Například špatně fungující brzdy motocyklu mohou způsobit nehodu, jejímž následkem bude poranění hlavy, rukou a nohou řidiče, a mohou způsobit dokonce popáleniny v případě, že se při této nehodě vznítí benzín. V této situaci by všechna zranění spadala do stejného scénáře poškození zdraví a bylo by třeba odhadnout závažnost všech zranění společně. Tato společně posuzovaná zranění jsou samozřejmě velmi vážná. Některá zranění by však neměla být přidávána do různých scénářů.
V každodenní praxi dozoru nad trhem může postačovat i posouzení rizik vyplývajících z jediného nebezpečí. Jestliže rizika plynoucí z tohoto nebezpečí opodstatňují přijetí opatření pro řízení rizik, toto opatření může být bez otálení přijato. Aby byla zajištěna dostatečná účinnost tohoto opatření, měl by si být posuzovatel rizik ovšem jist, že se u zjištěného rizika jedná o nejvyšší riziko (nebo jedno z nejvyšších rizik). Tak je tomu vždy, je-li toto riziko vážné, protože to je nejvyšší možná úroveň rizika podle těchto pokynů. V případech nižších než vážných rizik však mohou být zapotřebí další posouzení rizik a v pozdější fázi případně i zvláštní řízení rizik. Závěrem lze uvést, že díky zkušenostem s posuzováním rizik v praxi dozoru nad trhem je počet potřebných posouzení rizik možné omezit na minimum.
Zjišťování nebezpečí pomocí zkoušek a norem
Nebezpečí jsou často zjišťována a kvantifikována pomocí zkoušek. Tyto zkoušky a způsoby jejich provádění mohou být stanoveny v evropských nebo mezinárodních normách pro výrobky. Skutečnost, že výrobek vyhovuje „harmonizované“ evropské normě („EN …“), na kterou byl zveřejněn odkaz v Úředním věstníku, zakládá předpoklad bezpečnosti (ovšem jen u bezpečnostních parametrů, na které se příslušné hodnoty nebo normy vztahují). V takových případech lze předpokládat, že z hlediska konkrétního testovaného nebezpečí je výrobek spojen jen s minimálním rizikem a s vysokou úrovní ochrany.
Mohou se nicméně vyskytnout případy, v nichž se předpoklad bezpečnosti neuplatní. Tehdy je nutné připravit zvláště dobře zdokumentované posouzení rizik, včetně výzvy ke změně harmonizované normy.
Jestliže výrobek naopak ve zkoušce neobstojí, obvykle lze předpokládat existenci rizika, pokud výrobce není schopen předložit důkazy o bezpečnosti výrobku.
Výrobky mohou představovat riziko, i když nepoškozují zdraví
Výrobky mohou být příčinou rizika, přestože nejsou samy o sobě nebezpečné, a to z důvodu nevhodnosti pro jejich zamýšlené použití. Tak tomu může být například u osobních ochranných prostředků či záchranných prostředků, jako jsou reflexní vesty, které si řidiči automobilů oblékají po nehodě. Účelem těchto vest je upoutat pozornost přijíždějících řidičů a účastníků silničního provozu a upozornit je na nehodu, zvláště v noci. Pokud jsou však reflexní proužky příliš malé nebo nedostatečně odrážejí světlo, vesty nemusí být vidět, a tudíž uživatele požadovaným způsobem nechrání. Takové vesty proto představují riziko, ačkoli samy o sobě nejsou nebezpečné. Dalším příkladem může být prostředek na ochranu proti slunečnímu záření, na kterém je uvedeno označení „vysoká ochrana“ (ochranný sluneční faktor 30), ale který ve skutečnosti poskytuje jen „nízkou ochranu“ (ochranný faktor 6). Důsledkem může být těžké spálení sluncem.
3.3 Spotřebitel
Na úroveň rizika mohou mít velký vliv schopnosti a chování spotřebitele, který výrobek používá. Proto je nanejvýš důležité mít jasnou představu o typu spotřebitele, s nímž se pracuje ve scénáři poškození zdraví.
Pro zjištění nejvyššího rizika, a tedy „rizikovosti“ výrobku, může být nutné vypracovat scénáře poškození zdraví s různými typy spotřebitelů. Nestačí například vzít v potaz pouze nejzranitelnější spotřebitele, protože pravděpodobnost, že budou postiženi nepříznivými následky, může být v daném scénáři tak nízká, že je výsledné riziko nižší než ve scénáři poškození zdraví pro spotřebitele, kteří nepatří do zranitelné skupiny.
V úvahu je třeba vzít také osoby, které samy výrobek nepoužívají, ale mohou se nacházet v blízkosti uživatele. Například při práci s řetězovou pilou mohou odlétat třísky, které mohou zasáhnout do oka osobu v okolí. Tak se může stát, že i když je riziko spojené s řetězovou pilou účinně řízeno tím, že sám uživatel používá ochranné prostředky a řídí se veškerými dalšími opatřeními pro řízení rizik uvedenými výrobcem, lidé v okolí mohou být vážně ohroženi. Proto je třeba například v návodu k použití řetězové pily uvést upozornění na rizika pro osoby v okolí a informovat o tom, jak tato rizika minimalizovat.
Při přípravě scénáře poškození zdraví by proto měly být zohledněny níže uvedené aspekty týkající se typu spotřebitelů a způsobů, jakým výrobek používají. Tento seznam není úplný, ale měl by posuzovatele rizik motivovat k tomu, aby scénáře poškození zdraví popisovali s dostatečnou mírou podrobnosti. Je třeba poznamenat, že „spotřebiteli“ se zde rozumí i osoby, které výrobek samy nepoužívají, ale může na ně mít vliv, protože se nacházejí v jeho blízkosti.
|
— |
Zamýšlený/nezamýšlený uživatel: zamýšlený uživatel výrobku může výrobek používat snadno, protože se řídí návodem nebo protože je dobře obeznámen s daným druhem výrobků, včetně jejich zjevných i nezjevných nebezpečí. Nebezpečí, které výrobek představuje, se pak nemusí projevit a rizikovost výrobku může být malá. Nezamýšlený uživatel s výrobkem obeznámen být nemusí a nemusí nebezpečí rozpoznat. Riskuje tedy poškození zdraví, a riziko pro spotřebitele je tak vyšší. V závislosti na výrobku a způsobu jeho používání tak může být riziko pro zamýšleného uživatele jiné než riziko pro nezamýšleného uživatele. |
|
— |
Zranitelní spotřebitelé: rozlišit lze několik kategorií zranitelných a velmi zranitelných spotřebitelů: děti (0 až 36 měsíců, > 36 měsíců až < 8 let, 8 až 14 let) a další skupiny, například starší osoby (viz tabulka 1). Všechny děti mají zhoršenou schopnost rozeznat nebezpečí. Když se například děti dotknou horkého povrchu, zaznamenají žár až zhruba po 8 vteřinách (kdy už utrpěly popáleniny), kdežto dospělí si žáru všimnou okamžitě. Pro zranitelné spotřebitele může být také obtížné zohlednit upozornění nebo mohou mít určité potíže s použitím výrobku, který ještě nikdy nepoužívali. Mohou se také chovat způsobem, který je více vystavuje nebezpečí, například když malé děti lezou a vkládají si předměty do úst. Výrobky také mohou přitahovat děti svým atraktivním vzhledem, a to je v rukou dětí činí vysoce rizikovými. Na druhé straně by se děti neměly běžně dostat rovnou do potíží, pokud jsou pod dohledem rodičů nebo jiných dospělých osob. Kromě toho i spotřebitelé, kteří obvykle nejsou zranitelní, se mohou v konkrétní situaci zranitelnými stát. Tak je tomu kupříkladu tehdy, když jsou návody nebo upozornění na výrobku napsány cizím jazykem, kterému spotřebitel nerozumí. Konečně v konkrétním případě chemických látek mohou být k jejich toxicitě děti vnímavější než průměrná dospělá osoba. S dětmi by se proto nemělo jednat jako s „malými dospělými“. Z toho plyne závěr, že výrobek, který je obvykle bezpečný pro průměrného dospělého, nemusí být bezpečný pro zranitelné spotřebitele. To je třeba brát v potaz při určování závažnosti a pravděpodobnosti poškození zdraví (viz oddíl 3.5), a tedy rizika. |
|
— |
Určené a rozumně předvídatelné použití: navzdory jasné srozumitelnosti návodu, včetně případných upozornění, mohou spotřebitelé výrobky používat k jiným účelům, než pro které jsou určeny. Jelikož upozornění nemusí být zcela účinná, je tudíž při posuzování rizik nutné zohledňovat i jiná než zamýšlená použití. Tento aspekt je zvláště důležitý pro výrobce, protože ten je povinen zajistit, aby byl výrobek bezpečný za všech rozumně předvídatelných podmínek použití. Rozumně předvídatelné použití může být nutné stanovit na základě zkušenosti, protože v úředních statistikách nehod ani v jiných zdrojích nemusí být k dispozici žádné informace. V takových případech může být těžké stanovit hranici mezi „rozumně předvídatelnými“ a „zcela nerealistickými“ scénáři. Nicméně podle těchto pokynů mohou být zvažovány i „zcela nerealistické“ scénáře, a to i když vedou k velmi vážným poškozením zdraví, protože takové scénáře budou mít vždy velmi nízkou pravděpodobnost. Tím se případně zabrání tomu, aby takovéto scénáře měly přílišný vliv na určení celkové rizikovosti výrobku. |
|
— |
Četnost a délka používání: různí spotřebitelé mohou výrobek používat častěji nebo méně často a po delší nebo kratší časové úseky. To závisí na atraktivitě výrobku a snadnosti jeho použití. Díky každodennímu nebo dlouhodobému používání se spotřebitel může důkladně seznámit s výrobkem a jeho specifiky, včetně příslušných nebezpečí, návodů a upozornění, čímž se riziko zmenší. Na druhé straně může každodenní nebo dlouhodobé používání vést k tomu, že si spotřebitel na výrobek příliš zvykne, a k určité uživatelské únavě, kdy spotřebitel bezstarostně ignoruje návody a upozornění, a riziko se tak zvýší. Konečně může každodenní nebo dlouhodobé používání urychlit stárnutí výrobku, což rovněž zvyšuje riziko, protože jeho části, které nejsou odolné vůči tak častému používání, se mohou rychle porouchat a způsobit nebezpečí a případně i poškození zdraví. |
|
— |
Rozpoznání nebezpečí, bezpečné chování a ochranné prostředky: o některých výrobcích je známo, že jsou nebezpečné. Jde například o nůžky, nože, vrtačky pro kutily, řetězové pily, in-line brusle, jízdní kola, motocykly či automobily. Ve všech těchto případech je nebezpečí spojené s výrobkem jednoznačně známé nebo snadno rozpoznatelné nebo je popsáno v návodu, který bude obsahovat také opatření pro řízení rizik. Spotřebitel se pak může chovat opatrně nebo používat osobní ochranné prostředky jako rukavice, přilby nebo bezpečnostní pásy, čili používat výrobek způsobem minimalizujícím riziko. Jindy nemusí být nebezpečí spojené s výrobkem tak snadno rozpoznatelné, například v případě zkratu u elektrické žehličky, upozornění mohou být přehlédnuta nebo špatně pochopena a spotřebitelé budou moci jen zřídka přijímat preventivní opatření. |
|
— |
Chování spotřebitele, dojde-li k incidentu: jestliže nebezpečí zasáhne spotřebitele, může poškodit jeho zdraví. Při posuzování rizik je tedy důležité zvážit, jak může spotřebitel reagovat. Klidně výrobek odloží a podnikne preventivní kroky, jako je hašení požáru, který výrobek způsobil, nebo výrobek v panice odhodí? Zranitelní spotřebitelé, zejména děti, se koneckonců nemusí chovat stejně jako ostatní, kteří nepatří do zranitelné skupiny. |
|
— |
Kulturní zázemí spotřebitele a způsob, jakým se výrobek používá v jeho vlasti, mohou též ovlivnit rizikovost výrobku. Tyto kulturní rozdíly musí brát v úvahu zejména výrobci, když uvádějí nový výrobek na určitý trh. Zkušenosti výrobců v této oblasti tak mohou být cenným zdrojem informací pro orgány připravující posouzení rizik. |
3.4 Scénář poškození zdraví: kroky vedoucí k poškození
Většina scénářů poškození zdraví se skládá z těchto tří hlavních kroků:
|
1. |
výrobek má „vadu“ nebo během doby své předpokládané životnosti může způsobit „nebezpečnou situaci“; |
|
2. |
následkem „vady“ nebo „nebezpečné situace“ je nehoda; |
|
3. |
nehoda vede k poškození zdraví. |
Tyto tři hlavní kroky lze rozdělit do dalších kroků s cílem popsat mimo jiné, jak může nebezpečí spojené s výrobkem vést k poškození zdraví. Nicméně tyto „kroky k poškození zdraví“ musí být jasné a stručné – bez nadměrné podrobnosti či nadměrného počtu kroků. S rostoucí zkušeností bude čím dále snadnější stanovit podmínky výskytu jakéhokoli daného poškození zdraví a „nejkratší cestu k poškození zdraví“ (nebo „kritickou cestu k poškození zdraví“).
Pravděpodobně nejsnadnější je začít se scénářem, kdy spotřebitel, kterému je výrobek určen, výrobek používá v souladu s návodem nebo, neexistuje-li návod, v souladu s běžným způsobem zacházení a používání. Jestliže toto posouzení vede k nejvyšší úrovni rizika, obvykle není třeba provádět další posouzení a mohou být přijata vhodná opatření ke snížení rizik. Obdobně je-li v konkrétní stížnosti spotřebitele oznámen určitý incident, může pro dosažení závěru ohledně vhodných opatření ke snížení rizik postačovat jediný scénář poškození zdraví.
Jinak je možné vypracovat další scénáře zahrnující zranitelné spotřebitele, zejména děti (viz tabulka 1), drobné nebo výraznější odchylky od běžného používání, používání za odlišných klimatických podmínek, například ve velmi chladném nebo velmi horkém podnebí, nepříznivé podmínky používání, například bez denního světla či náležitého osvětlení, používání způsobem navrhovaným při prodeji výrobku (například u lampičky prodávané v hračkářství je třeba posoudit také rizika při jejím používání dětmi), používání výrobku po celou dobu jeho životnosti (včetně opotřebení) atd. Každý z těchto scénářů by měl být zvažován v rámci celého postupu posouzení rizik.
Pokud výrobek představuje několik nebezpečí, scénář poškození zdraví, a tedy i scénář rizika by měl být vypracován pro každé z nich. Počet scénářů poškození zdraví je nicméně možné omezit kontrolou věrohodnosti týkající se toho, zda určitý scénář poškození zdraví může vést k riziku vyžadujícímu přijetí opatření.
Ze všech vypracovaných scénářů bude z hlediska opatření ke snížení rizik, která je třeba přijmout, obvykle rozhodující scénář vedoucí k nejvyššímu riziku (= „rizikovost“ výrobku), protože opatřením proti nejvyššímu riziku se rizika snižují nejúčinněji. Výjimkou z tohoto pravidla může být konkrétní nižší než nejvyšší riziko, které vyplývá z jiného nebezpečí a je možné řídit je pomocí specifických opatření. Přitom je samozřejmě nutné řešit i nejvyšší riziko.
Obecným pravidlem je, že scénáře poškození zdraví mohou vést k nejvyšší úrovni rizika, pokud:
|
— |
zvažovaná poškození zdraví spadají do nejvyšších stupňů závažnosti (stupeň 4 nebo 3), |
|
— |
celková pravděpodobnost scénáře poškození zdraví je dosti vysoká (alespoň > 1/100). |
Další pomoc v tomto ohledu nabízí tabulka 4. Tyto úvahy mohou přispět k omezení počtu scénářů.
Za počet scénářů poškození zdraví je samozřejmě nadále odpovědný posuzovatel rizik. Tento počet přitom závisí na počtu faktorů, které je nutné vzít v úvahu při určování „rizikovosti“ výrobku. Proto není možné uvést konkrétní počet scénářů poškození zdraví, které mohou být v určitém případě zapotřebí.
S cílem napomoci k vypracování vhodného počtu scénářů obsahují tyto pokyny tabulku s typickými scénáři poškození zdraví (tabulka 2). Tyto scénáře je třeba přizpůsobit konkrétnímu výrobku, typu spotřebitele a dalším okolnostem.
3.5 Závažnost poškození zdraví
Nebezpečí může vést k poškození zdraví spotřebitele v různých stupních závažnosti. Závažnost poškození zdraví tak odpovídá účinku, který má dané nebezpečí na spotřebitele za podmínek popsaných ve scénáři poškození zdraví.
Závažnost poškození zdraví může záviset na:
|
— |
druhu nebezpečí (viz seznam nebezpečí uvedený v oddíle 3.2 a v tabulce 2). Mechanické nebezpečí, například ostré hrany, může vést k pořezání prstů; takové poranění je okamžitě patrné a spotřebitel podnikne kroky k jeho vyléčení. Naproti tomu chemické nebezpečí může způsobit rakovinu. To obvykle není zjevné a nemoc se může rozvinout až po mnoha letech. Přitom je považována za velmi vážnou, protože rakovina je obtížně vyléčitelná nebo nevyléčitelná, |
|
— |
velikosti nebezpečí. Kupříkladu povrch zahřátý na 50 °C může způsobit lehké popáleniny, zatímco povrch o teplotě 180 °C způsobí těžké popáleniny, |
|
— |
tom, jak dlouho nebezpečí na spotřebitele působí. Při krátkodobém kontaktu se zdrojem nebezpečí odření může dojít jen k povrchovému poškrábání pokožky spotřebitele, zatímco při delším kontaktu mohou být sedřeny velké části kůže, |
|
— |
tom, která část těla je poškozena. Například propíchnutí kůže na paži ostrým hrotem je bolestivé, ale stejné poranění oka je vážnější a může i ohrozit život; |
|
— |
tom, jaký vliv má nebezpečí na jednu nebo několik částí těla. Elektrické nebezpečí může způsobit úraz elektrickým proudem se ztrátou vědomí a následně požár, který může vést k poškození plic, když osoba v bezvědomí vdechuje kouř, |
|
— |
typu spotřebitele a jeho chování. Výrobek s upozorněním může dospělý spotřebitel používat bez újmy na zdraví, protože dokáže používání výrobku přizpůsobit své chování. Naproti tomu dítě nebo jiný zranitelný spotřebitel (viz tabulka 1), který si nemůže upozornění přečíst a pochopit, může utrpět velmi vážné zranění. |
Za účelem kvantifikace závažnosti poškození zdraví ukazuje tabulka 3 v těchto pokynech, jak poškození klasifikovat do čtyř kategorií podle toho, zda jsou vratná, tj. zda je možné se uzdravit a do jaké míry. Tato kategorizace má sloužit jen jako vodítko; posuzovatel rizik by měl v případě potřeby kategorii změnit a změnu uvést v posouzení rizik.
Pokud se v rámci posouzení rizik zvažuje několik scénářů poškození zdraví, závažnost každého poškození by měla být klasifikována zvlášť a mělo by se s ní pracovat v celém procesu posouzení rizik.
Příklad: Spotřebitel zatlouká kladivem hřebík do stěny. Hlava kladiva není dost pevná (je vyrobena z nesprávného materiálu) a rozlomí se, přičemž jeden úlomek vletí spotřebiteli do oka tak prudce, že způsobí slepotu. Poškozením zdraví tedy je „poranění oka, cizí těleso v oku: trvalá ztráta zraku (jedno oko)“, což je podle tabulky 3 poškození zdraví stupně 3.
3.6 Pravděpodobnost poškození zdraví
„Pravděpodobností poškození zdraví“ se rozumí pravděpodobnost, že se scénář poškození zdraví během očekávané doby životnosti výrobku opravdu uskuteční.
Tuto pravděpodobnost není snadné odhadnout. Jestliže je však scénář popsán v jednotlivých krocích, může být každému kroku přiřazena určitá pravděpodobnost a celková pravděpodobnost scénáře se získá vynásobením těchto dílčích pravděpodobností. Tento krokový přístup by měl odhadování celkové pravděpodobnosti usnadnit. Je-li vypracováno několik scénářů, u každého z nich je samozřejmě nutné zjistit jeho vlastní celkovou pravděpodobnost.
Pokud je ale scénář poškození zdraví popsán v jediném kroku, jeho pravděpodobnost je také možné určit jedině v jednom celkovém kroku. To by však byl pouhý „odhad od oka“, který by se mohl stát terčem tvrdé kritiky, a celé posouzení rizik by tak mohlo být zpochybněno. Je tudíž lepší dát přednost transparentnějšímu přiřazení pravděpodobností scénáři složenému z několika kroků, zejména proto, že dílčí pravděpodobnosti je možné založit na nezpochybnitelných důkazech.
V těchto pokynech se pro účely klasifikace celkové pravděpodobnosti rozlišuje 8 pravděpodobnostních úrovní: od < 1/1 000 000 po > 50 % (viz levá strana tabulky 4). Na následujícím příkladu hlavy kladiva, která se rozlomí při zatloukání hřebíku do zdi, je možné ukázat, jak se přiřazuje pravděpodobnost jednotlivým krokům a jak se klasifikuje celková pravděpodobnost:
|
Krok 1: |
Hlava kladiva se rozlomí, když uživatel zatlouká do zdi hřebík, protože je vyrobena z nedostatečně pevného materiálu. Nedostatečná pevnost byla zjištěna zkouškou. S ohledem na zjištěnou hodnotu pevnosti je pravděpodobnost, že se hlava kladiva během očekávané doby životnosti kladiva rozlomí, stanovena na 1/10. |
|
Krok 2: |
Jeden z úlomků kladiva po rozlomení zasáhne uživatele. Pravděpodobnost této události je stanovena na 1/10, protože se má za to, že povrch horní části těla vystavený odlétávajícím úlomkům zabírá 1/10 polokoule před stěnou. Samozřejmě pokud by uživatel stál velmi blízko u zdi, jeho tělo by zabíralo větší část této polokoule a pravděpodobnost by byla vyšší. |
|
Krok 3 |
Úlomek uživatele zasáhne do hlavy. Odhaduje se, že hlava tvoří asi 1/3 horní části těla, a pravděpodobnost tedy činí 1/3. |
|
Krok 4: |
Úlomek uživatele zasáhne do oka. U očí se má za to, že zabírají asi 1/20 povrchu hlavy, a pravděpodobnost tak činí 1/20. |
Vynásobením pravděpodobností těchto kroků se získá celková pravděpodobnost scénáře, tedy: 1/10 × 1/10 × 1/3 × 1/20 = 1/6 000. To znamená pravděpodobnost > 1/10 000 (viz levá strana tabulky 4).
Poté, co byla celková pravděpodobnost scénáře poškození zdraví vypočítána, měla by být zkontrolována její věrohodnost. To je úkol vyžadující dosti zkušeností a z toho plyne, že je vhodné požádat o pomoc osoby, které mají zkušenosti s posuzováním rizik (viz oddíl „Kontrola posouzení rizik jinými odborníky“). Po získání zkušeností s těmito pokyny by odhadování pravděpodobnosti mělo být snazší a tento úkol bude usnadněn také rostoucím počtem příkladů, které budou k dispozici.
Přiřazování hodnot pravděpodobnosti různým scénářům poškození zdraví pro stejný výrobek může vést k těmto výsledkům:
|
— |
Jestliže výrobek v určitém scénáři používají zranitelnější spotřebitelé, pravděpodobnost může být obecně nutné zvýšit, protože u zranitelnějších spotřebitelů může k poškození zdraví dojít snadněji. To se týká zejména dětí, protože děti obvykle nemají dostatek zkušeností, a proto se nechovají tak, aby poškození předcházely, spíše naopak (viz též bod „zranitelní spotřebitelé“ v oddílu 3.3). |
|
— |
Jestliže je riziko snadno rozpoznatelné, například díky upozorněním na výrobku, může být nutné pravděpodobnost snížit, protože uživatel bude výrobek používat opatrněji, aby pokud možno předešel poškození zdraví. To se však nemusí vztahovat na scénář poškození zdraví, v němž figuruje malé dítě nebo jiný zranitelný uživatel (viz tabulka 1), který neumí číst. |
|
— |
Jestliže byly hlášeny nehody, které zapadají do scénáře poškození zdraví, pravděpodobnost tohoto scénáře se může zvýšit. V případech, kdy jsou nehody hlášeny jen zřídka nebo se o jejich výskytu vůbec neví, může být užitečné obrátit se na výrobce s dotazem, zda mu nejsou známy nějaké nehody nebo nepříznivé účinky způsobené výrobkem. |
|
— |
Jestliže je k tomu, aby poškození zdraví nastalo, nutné splnění dosti velkého počtu podmínek, celková pravděpodobnost daného scénáře bude obvykle nižší. |
|
— |
Jestliže jsou podmínky nutné k tomu, aby poškození nastalo, splněny snadno, pravděpodobnost se může zvýšit. |
|
— |
Jestliže výsledky zkoušek výrobku překračují požadované mezní hodnoty (podle příslušné normy nebo právního předpisu) velkým rozdílem, pravděpodobnost, že dojde k poškození zdraví (že se uskuteční scénář), může být vyšší, než kdyby byly výsledky výrobku blízko mezním hodnotám. |
„Pravděpodobností poškození zdraví“ se v tomto případě rozumí pravděpodobnost, že se scénář poškození zdraví skutečně naplní. Pravděpodobnost tudíž nepopisuje celkovou expozici obyvatelstva výrobku, která by se vypočítala například na základě úvahy o tom, kolik milionů kusů výrobku bylo na trhu prodáno, a následně úvahy, že několik z nich se může porouchat. Úvahy tohoto typu ovšem mají význam při určování vhodných opatření ke snížení rizik (viz oddíl 4).
Také statistiky nehod používané pro odhadování pravděpodobnosti je nutné pečlivě zvažovat, i když se týkají konkrétních výrobků. Okolnosti nehody totiž nemusí být popsány dostatečně podrobně, výrobek se mohl změnit v čase, může pocházet od jiného výrobce a podobně. Kromě toho nemusely být subjektům shromažďujícím příslušné statistické údaje hlášeny méně závažné nehody. Statistiky nehod přesto mohou usnadnit porozumění scénářům poškození zdraví a jejich pravděpodobnosti.
3.7 Určení rizika
Poté, co byla stanovena závažnost poškození zdraví a pravděpodobnost, pokud možno pro několik scénářů poškození zdraví, je nutné vyhledat úroveň rizika v tabulce 4. Tabulka 4 kombinuje závažnost poškození zdraví a pravděpodobnost, přičemž nejvyšší riziko odpovídá „rizikovosti“ výrobku. Rizika vyžadující zvláštní opatření pro řízení rizik je rovněž třeba uvést, aby bylo zajištěno, že všechna rizika budou snížena na minimum.
V těchto pokynech se rozlišují čtyři úrovně rizika: „vážné“, „vysoké“, „střední“ a „nízké“ riziko. Mezi sousedními stupni závažnosti poškození zdraví nebo úrovněmi pravděpodobnosti se úroveň rizika obvykle mění o jeden stupeň. To je v souladu s obecnou zkušeností, že se riziko nezvyšuje krokově, když se vstupní faktory mění plynule. Ovšem pokud se závažnost poškození zdraví zvýší ze stupně 1 na stupeň 2 (na pravé straně tabulky 4), některé úrovně rizika se zvýší o dva stupně, konkrétně ze středního na vážné riziko a z nízkého na vysoké riziko. To je dáno tím, že tyto pokyny uvádějí čtyři stupně závažnosti poškození zdraví, zatímco původní metoda (viz úvod) jich měla pět. Nicméně čtyři stupně se u spotřebních výrobků pokládají za obvyklý počet, protože zajišťují dostatečně spolehlivý odhad závažnosti. Pět stupňů by znamenalo přílišnou podrobnost, neboť ani závažnost poškození zdraví ani pravděpodobnost nelze stanovit s velmi vysokou přesností.
Na konci posouzení rizik, ať se posuzuje jednotlivý scénář poškození zdraví nebo celková rizikovost výrobku, by se měla zvážit věrohodnost úrovně rizika a míra nejistoty provedených odhadů. To znamená například ověřit, že posuzovatel rizik své odhady a předpoklady založil na nejlepších dostupných informacích. Užitečná může být rovněž zpětná vazba od kolegů a dalších odborníků.
Velice přínosná může být také analýza citlivosti (viz příklad v oddílu 6.3). Jak se úroveň rizika změní, jestliže se závažnost poškození zdraví nebo pravděpodobnost zvýší nebo sníží o jeden stupeň? Pokud se úroveň rizika vůbec nezmění, je dosti pravděpodobné, že byla odhadnuta správně. Jestliže se naopak změní, úroveň rizika může být hraniční. V takovém případě je nutné znovu zvážit scénáře poškození zdraví a přiřazení stupně závažnosti poškození zdraví a hodnoty pravděpodobnosti. Po skončení analýzy citlivosti by měl mít posuzovatel rizik jistotu, že je úroveň rizika dostatečně věrohodná a že ji může zadokumentovat a předat na další místa.
4. Od rizika k opatření: odpovědné řízení rizik
Když je posouzení rizik hotové, obvykle se použije pro účely rozhodování, zda je nezbytné přijmout opatření s cílem snížit riziko, a tedy předejít škodám na zdraví spotřebitelů. Ačkoli přijímání opatření a posuzování rizik jsou dvě samostatné oblasti, uvádíme zde několik bodů pro ilustraci možných kroků navazujících na zjištěná rizika.
V rámci dozoru nad trhem se bude opatření často přijímat za kontaktu s příslušným orgánem a výrobcem, dovozcem nebo distributorem. To může tomuto orgánu pomoci s určením nejúčinnějšího a nejúčelnějšího způsobu řízení daného rizika.
Je-li u spotřebního výrobku zjištěno vážné riziko, mohou opatření k jeho snížení zahrnovat stažení výrobku z trhu nebo z oběhu. Nižší úrovně rizika obvykle vedou k méně přísným opatřením. Pro zajištění bezpečnosti výrobku pak může postačovat umístění upozornění na výrobek nebo zdokonalení návodu. U každé úrovně rizika by tedy měl příslušný orgán zvažovat, zda přijmout opatření a případně jaké opatření.
Mezi rizikem a opatřením ovšem neexistuje automatický vztah. Pokud výrobek vykazuje několik rizik, která jsou nižší než vážná, a jeho celková rizikovost tedy není vážná, může být přesto nutné bezodkladně přijmout opatření, protože kterékoli z těchto rizik se může dosti rychle projevit. Riziková struktura výrobku může poukazovat na nedostatečnou kontrolu kvality ve výrobě (54).
Důležité je rovněž zohlednit celkovou expozici populace. Jestliže je výrobek na trhu ve velkém počtu, a tedy jej používá vysoký počet spotřebitelů, může i jediné nižší než vážné riziko vyžadovat rychlé kroky k zamezení nepříznivým účinkům na zdraví spotřebitelů.
Nižší než vážná rizika mohou vyžadovat přijetí opatření také v případě, že by dotčený výrobek mohl způsobovat smrtelné nehody, i když jsou takové nehody krajně nepravděpodobné. Může jít například o uzávěr nádoby s nápojem, který by se mohl uvolnit a mohlo by jej spolknout dítě, které by se následkem toho mohlo udávit. Toto riziko je možné odstranit jednoduchou konstrukční změnou uzávěru a žádné další opatření nemusí být zapotřebí. Pokud je riziko smrtelné nehody skutečně nesmírně nízké, může být po určitou dobu povolen i doprodej zásob.
K další aspektům souvisejícím s riziky může patřit vnímání rizika a jeho pravděpodobných důsledků veřejností, jeho kulturní a politická citlivost a způsob, jakým o něm informují sdělovací prostředky. Tyto aspekty mohou být zvláště významné, jsou-li dotčenými spotřebiteli zranitelné osoby, zejména děti. Rozhodnout o tom, jaká opatření jsou zapotřebí, bude úkolem vnitrostátních orgánů dozoru nad trhem.
Přijetí opatření proti riziku může záviset také na samotném výrobku a na „minimálních rizicích slučitelných s použitím výrobku a považovaných za přijatelná a odpovídající vysoké úrovni ochrany“ (55). Toto minimální riziko bude nejspíš mnohem nižší u hraček, které jsou určeny dětem, než u řetězové pily, o níž se ví, že je spojena s tak vysokým rizikem, že pro jeho udržení na zvládnutelné úrovni jsou nutné účinné ochranné prostředky.
Konečně mohou být opatření nezbytná, i když neexistuje žádné riziko, například pokud výrobek nevyhovuje použitelným právním či správním předpisům (např. neúplná označení).
Z výše uvedeného tedy vyplývá, že mezi rizikem a opatřením neexistuje automatický vztah. Orgány dozoru budou brát v potaz celou řadu faktorů, včetně faktorů zmíněných v oddíle 3.3. Vždy je nutné zohlednit zásadu přiměřenosti a opatření musí být účinná.
5. Jak vypracovat posouzení rizika – stručně
1. Popište výrobek a nebezpečí s ním spojené.
Výrobek popište jednoznačně. Týká se nebezpečí celého výrobku nebo jen (oddělitelné) části výrobku?
Je s výrobkem spojeno jen jedno nebezpečí? Je nebezpečí několik? Další informace najdete v tabulce 2. Zjistěte, jaké normy či právní předpisy jsou pro daný výrobek použitelné.
Zjistěte, jaké normy či právní předpisy jsou pro daný výrobek použitelné.
2. Určete typ spotřebitele, se kterým budete pracovat ve scénáři poškození zdraví pro nebezpečný výrobek.
V prvním scénáři poškození zdraví začněte se zamýšleným uživatelem a zamýšleným použitím výrobku. Pro další scénáře použijte jiné spotřebitele (viz tabulka 1) a jiná použití.
3. Popište scénář poškození zdraví, ve kterém zvolené nebezpečí (zvolená nebezpečí) související s výrobkem způsobí poškození zdraví nebo nepříznivé účinky na zdraví u zvoleného spotřebitele.
Kroky vedoucí k poškození zdraví popište jasně a stručně bez nadměrných podrobností („nejkratší cesta k poškození zdraví“, „kritická cesta k poškození zdraví“). Pokud se ve stejném scénáři objeví souběžně několik poškození zdraví, zařaďte je všechny do tohoto scénáře.
Při popisování scénáře poškození zdraví zvažujte četnost a délku používání, rozpoznání nebezpečí spotřebitelem, zda je spotřebitel zranitelný (zejména jde-li o dítě), ochranné prostředky, chování spotřebitele v případě nehody, kulturní zázemí spotřebitele a další faktory, které pokládáte z hlediska posouzení rizik za důležité.
Další informace najdete v oddílu 3.3 a tabulce 2.
4. Určete závažnost poškození zdraví.
Určete stupeň závažnosti poškození zdraví spotřebitele (na stupnici od 1 do 4). Pokud daný scénář poškození zdraví obsahuje několik poškození zdraví spotřebitele, odhadněte závažnost všech těchto poškození společně.
Další informace najdete v tabulce 3.
5. Určete pravděpodobnost scénáře poškození zdraví.
Přiřaďte hodnotu pravděpodobnosti každému kroku scénáře poškození zdraví. Vypočítejte celkovou pravděpodobnost scénáře vynásobením těchto hodnot.
Další informace najdete v levé části tabulky 4.
6. Určete úroveň rizika.
Na základě kombinace závažnosti poškození zdraví a celkové pravděpodobnosti scénáře poškození zdraví vyhledejte úroveň rizika v tabulce 4.
7. Zkontrolujte věrohodnost úrovně rizika.
Pokud se zdá, že úroveň rizika není věrohodná, nebo si nejste jisti závažností poškození zdraví nebo pravděpodobnostmi, změňte příslušné hodnoty o jeden stupeň nahoru a o jeden stupeň dolů a vypočítejte znovu riziko. Tato „analýza citlivosti“ ukáže, zda se při změně vstupních hodnot změní riziko.
Zůstane-li úroveň rizika stejná, můžete si být posouzením rizik poměrně jisti. Pokud se snadno změní, může být vhodné přiklonit se k chybě ve prospěch větší bezpečnosti a pokládat za „rizikovost“ daného spotřebního výrobku získanou vyšší úroveň rizika.
Věrohodnost úrovně rizika můžete také prodiskutovat se zkušenými kolegy.
8. Vypracujte několik scénářů poškození zdraví s cílem stanovit nejvyšší riziko spojené s výrobkem.
Jestliže pomocí prvního scénáře poškození zdraví zjistíte úroveň rizika nižší, než je nejvyšší úroveň rizika podle těchto pokynů, a domníváte se, že výrobek může představovat vyšší riziko, než jaké bylo zjištěno,
|
— |
zvolte jiné spotřebitele (včetně zranitelných spotřebitelů, zejména dětí), |
|
— |
určete jiná použití (včetně rozumně předvídatelných použití) |
s cílem zjistit, v jakém scénáři poškození zdraví je výrobek spojen s nejvyšším rizikem.
Nejvyšší riziko obvykle představuje „rizikovost“ výrobku a umožňuje přijetí nejúčinnějších opatření pro řízení rizik. V konkrétních případech může určité nebezpečí vedoucí k riziku, které je nižší než nejvyšší, vyžadovat specifická opatření pro řízení rizik. To je třeba náležitě zohlednit.
Obecným pravidlem je, že scénáře poškození zdraví mohou vést k nejvyšší úrovni rizika podle těchto pokynů, pokud:
|
— |
zvažovaná poškození zdraví jsou alespoň na stupni 3 nebo 4, — |
|
— |
celková pravděpodobnost scénáře poškození zdraví je alespoň > 1/100. |
Další informace najdete v tabulce 4.
9. Posouzení rizika zadokumentujte a předejte na další místa.
Postupujte transparentně a uveďte také všechny prvky nejistoty, s nimiž jste se při práci na posouzení rizik setkali.
Oddíl 6 těchto pokynů obsahuje příklady týkající se přípravy zpráv o posouzení rizik.
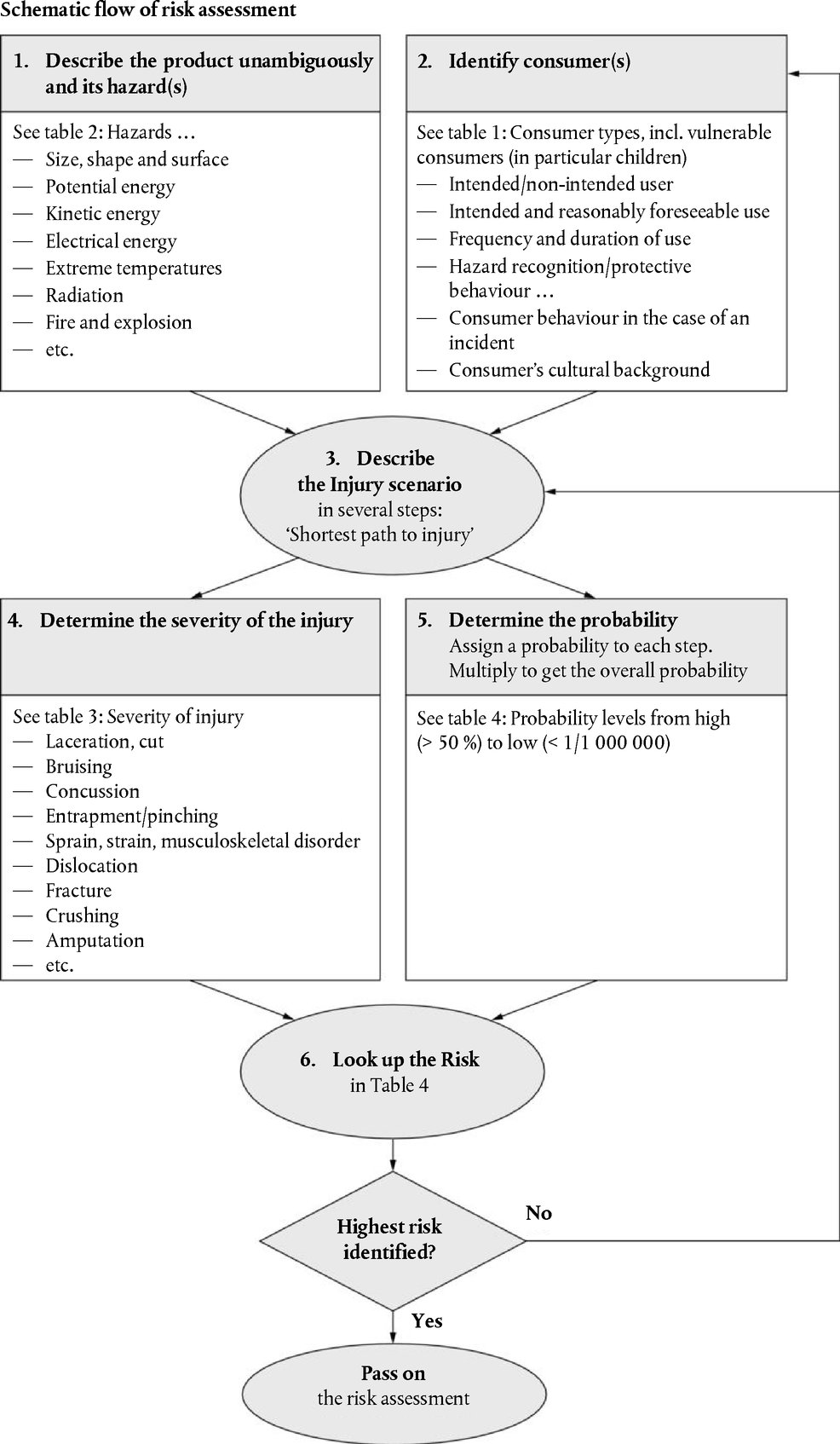
Schematic flow of risk assessment
Pass on the risk assessment
Highest risk identified?
Yes
No
6. Look up the Risk in Table 4
See table 4: Probability levels from high (> 50 %) to low (< 1/1 000 000)
See table 3: Severity of injury
— Laceration, cut
— Bruising
— Concussion
— Entrapment/pinching
— Sprain, strain, musculoskeletal disorder
— Dislocation
— Fracture
— Crushing
— Amputation
— etc.
5. Determine the probability
Assign a probability to each step.
Multiply to get the overall probability
4. Determine the severity of the injury
3. Describe the Injury scenario in several steps: ‘Shortest path to injury’
See table 1: Consumer types, incl. vulnerable consumers (in particular children)
— Intended/non-intended user
— Intended and reasonably foreseeable use
— Frequency and duration of use
— Hazard recognition/protective behaviour …
— Consumer behaviour in the case of an incident
— Consumer's cultural background
See table 2: Hazards …
— Size, shape and surface
— Potential energy
— Kinetic energy
— Electrical energy
— Extreme temperatures
— Radiation
— Fire and explosion
— etc.
2. Identify consumer(s)
1. Describe the product unambiguously and its hazard(s)
6. Příklady
6.1 Skládací židle

Skládací mechanismus skládací židle je zkonstruován tak, že se prsty uživatele mohou zachytit mezi sedadlo a tento mechanismus. To může vést ke zlomeninám, či dokonce ztrátě jednoho nebo několika prstů.
Určení rizik
|
Scénář poškození zdraví |
Druh a místo poškození zdraví |
Závažnost poškození zdraví |
Pravděpodobnost poškození zdraví |
Celková pravděpodobnost |
Riziko |
|
|
Uživatel rozkládá židli, omylem sedadlo uchopí blízko zadního rohu (nedává pozor, něco ho vyruší), prst se zachytí mezi sedadlo a opěradlo. |
lehké skřípnutí prstu |
1 |
rozkládání židle |
1 |
1/500 |
Nízké riziko |
|
uchopení sedadla u zadního rohu při rozkládání |
1/50 |
|
||||
|
zachycení prstu |
1/10 |
> 1/1 000 |
||||
|
lehké skřípnutí |
1 |
|
||||
|
Uživatel rozkládá židli, omylem sedadlo uchopí za boční okraj (nedává pozor, něco ho vyruší), prst se zachytí mezi sedadlo a vzpěrku. |
lehké skřípnutí prstu |
1 |
rozkládání židle |
1 |
1/500 |
Nízké riziko |
|
uchopení sedadla za boční okraj při rozkládání |
1/50 |
|
||||
|
zachycení prstu |
1/10 |
> 1/1 000 |
||||
|
lehké skřípnutí |
1 |
|
||||
|
Uživatel rozkládá židli, židle je sevřená, uživatel se snaží stlačit sedadlo a omylem jej uchopí blízko rohu (nedává pozor, něco ho vyruší), prst se zachytí mezi sedadlo a opěradlo. |
zlomenina prstu |
2 |
rozkládání židle |
1 |
1/500 000 |
Nízké riziko |
|
sevření židle |
1/1 000 |
|
||||
|
uchopení sedadla u rohů při rozkládání |
1/50 |
|
||||
|
zachycení prstu |
1/10 |
> 1/1 000 000 |
||||
|
zlomenina prstu |
1 |
|
||||
|
Uživatel rozkládá židli, židle je sevřená, uživatel se snaží stlačit sedadlo a omylem jej uchopí za boční okraj (nedává pozor, něco ho vyruší), prst se zachytí mezi sedadlo a vzpěrku. |
zlomenina prstu |
2 |
rozkládání židle |
1 |
1/500 000 |
Nízké riziko |
|
sevření židle |
1/1 000 |
|
||||
|
uchopení sedadla za boční okraj při rozkládání |
1/50 |
|
||||
|
zachycení prstu |
1/10 |
> 1/1 000 000 |
||||
|
zlomenina prstu |
1 |
|
||||
|
Uživatel sedí na židli, chce židli přesunout a ve snaze zvednout ji židli uchopí za zadní část sedadla, prst se zachytí mezi sedadlo a opěradlo. |
ztráta prstu |
3 |
sezení na židli |
1 |
1/6 000 |
Vysoké riziko |
|
přesouvání židle při sezení |
1/2 |
|
||||
|
uchopení židle za zadní část při přesouvání |
1/2 |
|
||||
|
židle se částečně složí, čímž vznikne mezera mezi opěradlem a sedadlem |
1/3 |
> 1/10 000 |
||||
|
prst se nachází mezi opěradlem a sedadlem |
1/5 |
|
||||
|
zachycení prstu |
1/10 |
|
||||
|
ztráta (části) prstu |
1/10 |
|
||||
|
Uživatel sedí na židli, chce židli přesunout a ve snaze zvednout ji židli uchopí za zadní část sedadla, prst se zachytí mezi sedadlo a vzpěrku. |
ztráta prstu |
3 |
sezení na židli |
1 |
1/6 000 |
Vysoké riziko |
|
přesouvání židle při sezení |
1/2 |
|
||||
|
uchopení židle za zadní část při přesouvání |
1/2 |
|
||||
|
židle se částečně složí, čímž vznikne mezera mezi opěradlem a sedadlem |
1/3 |
> 1/10 000 |
||||
|
prst se nachází mezi opěradlem a sedadlem |
1/5 |
|
||||
|
zachycení prstu |
1/10 |
|
||||
|
ztráta (části) prstu |
1/10 |
|
||||
Celková rizikovost skládací židle tedy odpovídá stupni „vysoké riziko“.
6.2 Chrániče elektrických zásuvek

Tento příklad se týká chráničů (záslepek) elektrických zásuvek. Jedná se o zařízení, která uživatelé (rodiče) nasazují na elektrické zásuvky, aby předešli tomu, že malé děti vloží dlouhý kovový předmět do zdířky zásuvky a tak se dostanou do kontaktu s částmi pod napětím a utrpí (smrtelný) úraz elektrickým proudem.
Otvory tohoto konkrétního chrániče (kterými procházejí kolíky zástrčky) jsou tak těsné, že se v nich mohou kolíky zachytit. To by mohlo vést k tomu, že uživatel při vytahování zástrčky odstraní ze zásuvky i chránič. Toho si uživatel nemusí všimnout.
Určení rizik
|
Scénář poškození zdraví |
Druh a místo poškození zdraví |
Závažnost poškození zdraví |
Pravděpodobnost poškození zdraví |
Celková pravděpodobnost |
Riziko |
|
|
Chránič je odstraněn ze zásuvky, která zůstane nechráněná. Dítě si hraje s tenkým vodivým předmětem, který lze zastrčit do zásuvky, dostane se do kontaktu s vysokým napětím a je usmrceno elektrickým proudem. |
Zásah elektrickým proudem |
4 |
odstranění chrániče |
9/10 |
27/160 000 |
Vážné riziko |
|
odstranění zůstane nepovšimnuto |
1/10 |
|
||||
|
dítě si hraje s tenkým vodivým předmětem |
1/10 |
|
||||
|
dítě si hraje bez dozoru |
1/2 |
> 1/10 000 |
||||
|
dítě předmět zastrčí do zásuvky |
3/10 |
|
||||
|
kontakt s napětím |
1/2 |
|
||||
|
usmrcení elektrickým proudem kvůli kontaktu s napětím (bez přerušovače obvodu) |
1/4 |
|
||||
|
Chránič je odstraněn ze zásuvky, která zůstane nechráněná. Dítě si hraje s tenkým vodivým předmětem, který lze zastrčit do zásuvky, dostane se do kontaktu s vysokým napětím a utrpí úraz elektrickým proudem. |
Popáleniny 2. stupně |
1 |
odstranění chrániče |
9/10 |
81/160 000 |
Nízké riziko |
|
odstranění zůstane nepovšimnuto |
1/10 |
|
||||
|
dítě si hraje s tenkým vodivým předmětem |
1/10 |
|
||||
|
dítě předmět zastrčí do zásuvky |
3/10 |
|
||||
|
kontakt s napětím |
1/2 |
> 1/10 000 |
||||
|
dítě si hraje bez dozoru |
1/2 |
|
||||
|
popálení elektrickým proudem (bez přerušovače obvodu) |
3/4 |
|
||||
|
Zásuvka je nechráněná. Dítě si hraje s tenkým vodivým předmětem, který lze zastrčit do zásuvky, dostane se do kontaktu s vysokým napětím a je usmrceno elektrickým proudem. |
Zásah elektrickým proudem |
4 |
dítě si hraje s tenkým vodivým předmětem |
1/10 |
3/80 000 |
Vysoké riziko |
|
dítě si hraje bez dozoru |
1/100 |
|
||||
|
dítě předmět zastrčí do zásuvky |
3/10 |
|
||||
|
kontakt s napětím |
1/2 |
> 1/100 000 |
||||
|
usmrcení elektrickým proudem kvůli kontaktu s napětím (bez přerušovače obvodu) |
1/4 |
|
||||
Celková rizikovost chráničů zásuvek tedy odpovídá stupni „vážné riziko“.
6.3 Analýza citlivosti
Faktory, které se používají pro výpočet rizika ve scénáři poškození zdraví, totiž závažnost poškození zdraví a pravděpodobnost, je často nutné odhadovat. To vede k určité nejistotě. Zejména pravděpodobnost může být obtížně odhadnutelná, protože kupříkladu chování spotřebitelů může být těžké předpovědět. Dělá člověk určitý úkon často, nebo jen občas?
Proto je důležité zvážit míru nejistoty těchto dvou faktorů a provést analýzu citlivosti. Účelem této analýzy je zjistit, do jaké míry se úroveň rizika změní, změní-li se odhadnuté faktory. Příklad uvedený v tabulce níže se týká pouze změn pravděpodobnosti, protože závažnost poškození zdraví je obvykle předpovězena s větší jistotou.
Praktický způsob, jak analýzu citlivosti provést, spočívá v tom, že se zopakuje posouzení rizika pro určitý scénář, ale s jinou pravděpodobností u jednoho nebo několika kroků tohoto scénáře. Například svíčka obsahující semena může způsobit požár, protože semena se mohou vznítit a hořet vysokým plamenem. Od nich se může oheň rozšířit na nábytek nebo záclony a lidé, kteří jsou v jiné místnosti, se mohou nadýchat toxického dýmu a utrpět smrtelnou otravu.
|
Scénář poškození zdraví |
Druh a místo poškození zdraví |
Závažnost poškození zdraví |
Pravděpodobnost poškození zdraví |
Výsledná pravděpodobnost |
Riziko |
||||||||
|
Semena nebo zrna začnou hořet vysokým plamenem. Oheň se rozšíří na nábytek nebo záclony. Osoby mimo místnost se nadýchají toxického dýmu. |
smrtelná otrava |
4 |
|
0 00675 > 1/1 000 |
Závažné |
Tabulka ukazuje, jak byly odhadnuty úrovně pravděpodobnosti jednotlivých kroků scénáře.
Celková pravděpodobnost činí 0 00675, což v tabulce 4 odpovídá kategorii > 1/1 000. To vede k závěru o „vážném riziku“. Všimněte si, že přesná pravděpodobnost je blíže hodnotě 1/100 než 1/1 000, a to samo o sobě již vede k určité jistotě ohledně spolehlivosti úrovně rizika, protože se v oblasti vážného rizika tabulky 4 nachází dále, než naznačuje řádek > 1/1 000.
Předpokládejme, že si nejsme jisti 5 % hodnotou pravděpodobnosti, že se lidé nadýchají toxického dýmu. Můžeme pro ni tedy stanovit mnohem nižší hodnotu 0,1 % (0,001 = jedna z tisíce). Pokud provedeme výpočet znovu s touto hodnotou, bude celková pravděpodobnost dosahovat 0,000135, což znamená > 1/10 000. Riziko ovšem zůstane vážné. I kdyby měla být pravděpodobnost z nějakého důvodu desetkrát nižší, riziko by bylo pořád vysoké. I když se tedy pravděpodobnost změní desetinásobně nebo stonásobně, pořád nacházíme vážné nebo vysoké riziko (přičemž „vysoké“ riziko je zde dosti blízko „vážnému“). Tato analýza citlivosti nám tak umožňuje posoudit riziko s jistotou jako vážné.
Obecně ovšem platí, že posouzení rizika by mělo vycházet z „rozumných nejhorších případů“: ne příliš pesimistických při hodnocení každého faktoru, ale rozhodne nikoli příliš optimistických.
Tabulka 1
Spotřebitelé
|
Spotřebitelé |
Popis |
|
velmi zranitelní spotřebitelé |
velmi malé děti: 0 až 36 měsíců ostatní: osoby s rozsáhlým a komplexním postižením |
|
zranitelní spotřebitelé |
malé děti: děti starší 36 měsíců a mladší 8 let, starší děti: děti od 8 do 14 let ostatní: osoby se sníženými tělesnými, smyslovými nebo duševními schopnostmi (např. částečně zdravotně postižené a starší osoby, včetně osob ve věku vyšším než 65 let, s určitým snížením tělesných a duševních schopností) nebo s nedostatkem zkušeností a znalostí |
|
ostatní spotřebitelé |
spotřebitelé jiní než velmi zranitelní nebo zranitelní |
Tabulka 2
Nebezpečí, typické scénáře poškození zdraví a typická poškození zdraví
|
Skupina nebezpečí |
Nebezpečí (vlastnost výrobku) |
Typický scénář poškození zdraví |
Typické poškození zdraví |
|
Velikost, tvar a povrch |
výrobek tvoří překážku |
Člověk o výrobek zakopne a upadne nebo do výrobku narazí. |
pohmožděniny; zlomeniny, otřes mozku |
|
výrobek nepropouští vzduch |
Výrobek člověku (typicky dítěti) zakryje ústa a/nebo nos nebo vnitřní dýchací cesty. |
udušení |
|
|
výrobek je malou částí nebo obsahuje malé části |
Člověk (dítě) malou část spolkne; ta se zachytí v hrtanu a zablokuje dýchací cesty. |
udávení, zablokování vnitřních dýchacích cest |
|
|
možnost ukousnutí malé části výrobku |
Člověk (dítě) malou část spolkne; ta se zachytí v trávicím traktu. |
zablokování trávicího traktu |
|
|
ostrý roh nebo hrot |
Člověk narazí na ostrý roh nebo je zasažen pohybujícím se ostrým předmětem; to vede k bodnému nebo penetrujícímu zranění. |
bodné poranění; poranění oka, cizí těleso v oku; poškození sluchu, cizí těleso v uchu |
|
|
ostrá hrana |
Člověk se dotkne ostré hrany; ta protrhne kůži nebo rozřízne tkáň. |
Tržné rány, řezné rány; amputace |
|
|
kluzký povrch |
Člověk při chůzi po povrchu uklouzne a upadne. |
pohmožděniny; zlomeniny, otřes mozku |
|
|
drsný povrch |
Dojde ke smýknutí člověka po drsném povrchu; následkem je tření a/nebo oděr. |
oděr |
|
|
mezera nebo otvor mezi částmi |
Člověku se dostane končetina nebo celé tělo do otvoru, kde se zachytí prst, paže, krk, hlava, tělo nebo oděv; vinou gravitace nebo pohybu dojde ke zranění. |
rozdrcení, zlomeniny, amputace, uškrcení |
|
|
Potenciální energie |
nízká mechanická stabilita |
Výrobek se převrhne; člověk na výrobku spadne z výšky nebo je výrobkem zasažen člověk v jeho blízkosti; elektrický výrobek se převrhne, rozbije se a odhalí části pod napětím nebo dále funguje a zahřívá okolní povrchy. |
pohmožděniny; vykloubení/dislokace; výron; zlomeniny, otřes mozku, rozdrcení/přejetí; úraz elektrickým proudem; popáleniny |
|
nízká mechanická pevnost |
Výrobek se zhroutí v důsledku přetížení; člověk na výrobku spadne z výšky nebo je výrobkem zasažen člověk v jeho blízkosti; elektrický výrobek se převrhne, rozbije se a odhalí části pod napětím nebo dále funguje a zahřívá okolní povrchy. |
pohmožděniny; vykloubení/dislokace; zlomeniny, otřes mozku; rozdrcení/přejetí; úraz elektrickým proudem; popáleniny |
|
|
uživatel ve výšce |
Člověk vysoko na výrobku ztratí rovnováhu, nemá oporu, které by se mohl držet, a spadne z výšky. |
pohmožděniny; vykloubení/dislokace; zlomeniny, otřes mozku, rozdrcení |
|
|
pružná část nebo pružina |
Stlačená pružná část nebo pružina se náhle uvolní; člověk v dráze pohybu je výrobkem zasažen. |
pohmožděniny; vykloubení/dislokace; zlomeniny, otřes mozku; rozdrcení |
|
|
stlačená kapalina či plyn nebo vakuum |
Stlačená kapalina nebo plyn se náhle uvolní; člověk v blízkosti je zasažen; nebo jsou následkem imploze výrobku letící předměty. |
Vykloubení/dislokace; zlomeniny, otřes mozku; rozdrcení/přejetí; řezné rány (viz též část o požáru a výbuchu) |
|
|
Kinetická energie |
pohybující se výrobek |
Člověk v dráze pohybu výrobku je výrobkem zasažen nebo přejet. |
pohmožděniny; výron; zlomeniny, otřes mozku; rozdrcení |
|
části pohybující se proti sobě |
Část těla se dostane mezi pohybující se části během jejich současného pohybu; část těla je zachycena a stlačena (rozdrcena). |
pohmožděniny; vykloubení/dislokace; zlomenina; rozdrcení |
|
|
části pohybující se přes sebe |
Část těla se dostane mezi pohybující se části během jejich pohybu ve vzájemné blízkosti (pohyb nůžek); část těla je zachycena mezi pohyblivé části a stlačena (přestřižení). |
Tržné rány, řezné rány; amputace |
|
|
rotující části |
Do rotující části se zamotá část těla, vlasy nebo oděv; výsledkem je tažná síla. |
pohmožděniny; zlomenina; tržné rány (kůže na hlavě); uškrcení |
|
|
rotující části ve vzájemné blízkosti |
Do rotujících částí je vtažena část těla, vlasy nebo oděv; výsledkem je tažná síla a tlak na část těla. |
rozdrcení, zlomeniny, amputace, uškrcení |
|
|
zrychlení |
Člověk na akcelerujícím výrobku ztratí rovnováhu, nemá oporu, které by se mohl držet, a spadne s určitou rychlostí. |
Vykloubení/dislokace; zlomeniny, otřes mozku; rozdrcení |
|
|
letící předměty |
Člověk je zasažen letícím předmětem a v závislosti na jeho energii utrpí zranění. |
pohmožděniny; vykloubení/dislokace; zlomeniny, otřes mozku; rozdrcení |
|
|
vibrace |
Člověk držící výrobek ztratí rovnováhu a upadne; nebo dlouhodobý kontakt s vibrujícím výrobkem vede k neurologickým poruchám, osteoartikulárním poruchám, poškození páteře či cévním poruchám. |
pohmožděniny; vykloubení/dislokace; zlomenina; rozdrcení |
|
|
hluk |
Člověk je vystaven hluku, který působí výrobek. V závislosti na hlasitosti a vzdálenosti se může rozvinout tinitus nebo ztráta sluchu. |
poškození sluchu |
|
|
Elektrická energie |
vysoké/nízké napětí |
Člověk se dotkne části výrobku, která je pod vysokým napětím; utrpí úraz elektrickým proudem a může být i usmrcen. |
úraz elektrickým proudem |
|
tvorba tepla |
Výrobek se zahřeje; člověk, který se ho dotkne, se popálí; nebo z výrobku mohou vycházet roztavené částice, pára apod., které člověka zasáhnou. |
popáleniny, opařeniny |
|
|
části pod napětím příliš blízko u sebe |
Mezi částmi pod napětím se objeví elektrický oblouk nebo jiskry. Důsledkem může být požár a intenzivní záření. |
poranění očí, popáleniny, opařeniny |
|
|
Extrémní teploty |
otevřený oheň |
Člověk v blízkosti plamenů může utrpět popáleniny, případně poté, co se na něm vznítí oděv. |
popáleniny, opařeniny |
|
horké povrchy |
Člověk nerozpozná horký povrch a dotkne se jej; utrpí popáleniny. |
popáleniny |
|
|
horké kapaliny |
Při manipulaci s nádobou člověk vylije část kapaliny; kapalina kápne na kůži a způsobí opařeniny. |
opařeniny |
|
|
horké plyny |
Člověk vdechne horké plyny uvolněné z výrobku; následkem je popálení plic; nebo dlouhodobá expozice horkému vzduchu vede k dehydrataci. |
popáleniny |
|
|
studené povrchy |
Člověk nerozpozná studený povrch a dotkne se jej; utrpí omrzliny. |
popáleniny |
|
|
Radiace |
ultrafialové záření, laser |
Kůže nebo oči člověka jsou vystaveny záření, které výrobek vydává. |
popáleniny, opařeniny; neurologické poruchy; poranění očí; rakovina kůže, mutace |
|
zdroj elektromagnetického pole (EMF) s vysokou intenzitou; nízká frekvence nebo vysoká frekvence (mikrovlny) |
Člověk se nachází blízko zdroje elektromagnetického pole (EMF), dochází k expozici těla (centrální nervové soustavy). |
neurologické poškození (poškození mozku), leukémie (u dětí) |
|
|
Požár a výbuch |
hořlavé látky |
Člověk se nachází blízko hořlavé látky; zdroj vznícení látku zapálí; následkem toho člověk utrpí zranění. |
popáleniny |
|
výbušné směsi |
Člověk se nachází blízko výbušné směsi; zdroj vznícení způsobí výbuch; člověk je zasažen rázovou vlnou, hořícím materiálem a/nebo plameny. |
popáleniny, opařeniny; poranění oka, cizí těleso v oku; poškození sluchu, cizí těleso v uchu |
|
|
zdroje vznícení |
Zdroj vznícení způsobí požár; člověk je poraněn plameny nebo v důsledku požáru domu utrpí otravu plyny. |
popáleniny; otrava |
|
|
přehřátí |
Výrobek se přehřeje; požár, výbuch. |
popáleniny, opařeniny; poranění oka, cizí těleso v oku; poškození sluchu, cizí těleso v uchu |
|
|
Toxicita |
toxická pevná nebo tekutá látka |
Člověk požije látku pocházející z výrobku, např. tak, že si výrobek vloží do úst, a/nebo se mu látka dostane na kůži. |
akutní otrava; podráždění, dermatitida |
|
Člověk vdechne pevnou hmotu nebo tekutinu, například zvratky (plicní aspirace). |
akutní otrava v plicích (aspirační pneumonie); infekce |
||
|
toxický plyn, pára nebo prach |
Člověk vdechne látku z výrobku, a/nebo se mu látka dostane na kůži |
akutní otrava v plicích; podráždění, dermatitida |
|
|
senzibilizující látka |
Člověk požije látku pocházející z výrobku, např. tak, že si výrobek vloží do úst a/nebo se mu látka dostane na kůži; a/nebo vdechne plyn, páru nebo prach. |
senzibilizace; alergická reakce |
|
|
dráždivá nebo žíravá pevná nebo tekutá látka |
Člověk požije látku pocházející z výrobku, např. tak, že si výrobek vloží do úst, a/nebo se mu látka dostane na kůži nebo do očí. |
podráždění, dermatitida; poleptání kůže; poranění oka, cizí těleso v oku |
|
|
dráždivý nebo žíravý plyn nebo pára |
Člověk vdechne látku z výrobku a/nebo se mu látka dostane na kůži nebo do očí. |
podráždění, dermatitida; poleptání kůže; akutní otrava nebo žíravé účinky v plicích nebo v očích |
|
|
látky karcinogenní, mutagenní nebo toxické pro reprodukci (CMR) |
Člověk požije látku pocházející z výrobku, např. tak, že si výrobek vloží do úst, a/nebo se mu látka dostane na kůži; a/nebo vdechne látku, jako je plyn, pára nebo prach. |
rakovina, mutace, toxické účinky na reprodukční schopnost |
|
|
Mikrobiologická kontaminace |
mikrobiologická kontaminace |
Člověk se dostane do styku s kontaminovaným výrobkem cestou požití, vdechnutí nebo dotyku s kůží. |
lokální nebo systémová infekce |
|
Výrobek v provozu nebezpečí |
nezdravá poloha těla |
Konstrukce výrobku vede k nezdravé tělesné poloze při jeho používání. |
natažení; muskuloskeletální porucha |
|
nadměrná námaha |
V důsledku konstrukce výrobku je při jeho používání nutná značná síla. |
vyvrtnutí nebo natažení; muskuloskeletální porucha |
|
|
anatomická nevhodnost |
Konstrukce výrobku není uzpůsobena lidské anatomii, a jeho používání je tudíž obtížné nebo nemožné. |
vyvrtnutí nebo natažení |
|
|
zanedbávání osobních ochranných prostředků |
Vzhledem ke konstrukci výrobku je zacházení s výrobkem nebo jeho používání obtížné pro člověka, který má na sobě ochranné prostředky. |
různá poškození |
|
|
neúmyslné spuštění či vypnutí |
Člověk může výrobek snadno zapnout či vypnout, což vede k nechtěnému provozu výrobku. |
různá poškození |
|
|
provozní nedostatečnost |
Konstrukce vede člověka k nesprávnému používání výrobku; nebo u výrobku s ochrannou funkcí není zajištěna předpokládaná ochrana. |
různá poškození |
|
|
selhání ukončování provozu |
Člověk chce ukončit provoz výrobku, ale jeho provoz pokračuje v situaci, kdy to není žádoucí. |
různá poškození |
|
|
neočekávané spuštění |
Výrobek se vypne při výpadku proudu, ale pak se nebezpečným způsobem znovu uvede do provozu. |
různá poškození |
|
|
nemožnost ukončit provoz |
V nouzové situaci člověk nemůže ukončit provoz výrobku. |
různá poškození |
|
|
neadekvátní spojení částí |
Člověk se snaží spojit s výrobkem nějakou část, ta nezapadne bez použití nadměrné síly, výrobek se rozbije; nebo je nějaká část s výrobkem spojena příliš volně a během jeho používání se uvolní. |
vyvrtnutí nebo natažení; tržné rány, řezné rány; pohmožděniny; uvíznutí |
|
|
chybějící nebo nesprávně namontované ochranné prvky |
Nebezpečné části jsou v dosahu člověka. |
různá poškození |
|
|
nedostatečná upozornění, nedostatečné výstražné značky a symboly |
Uživatel si nevšimne upozornění či značek a/nebo nerozumí symbolům. |
různá poškození |
|
|
nedostatečné výstražné signály |
Uživatel nevidí nebo neslyší výstražný signál (vizuální nebo zvukový), což vede k nebezpečnému provozu. |
různá poškození |
|
|
Pozn.: Tato tabulka má sloužit jen jako vodítko; typické scénáře poškození zdraví je při přípravě posouzení rizik třeba přizpůsobit. V případě chemických látek, kosmetických prostředků a případně i dalších výrobků existují zvláštní pokyny pro posuzování rizik. Pro posuzování takových výrobků se důrazně doporučuje používat tyto zvláštní pokyny. Viz oddíl 3.2. |
|||
Tabulka 3
Závažnost poškození zdraví
Úvod
Tyto pokyny pro posuzování rizik rozlišují čtyři stupně závažnosti poškození zdraví. Je důležité si uvědomit, že závažnost je třeba posuzovat naprosto objektivně. Cílem je porovnat závažnost poškození v různých scénářích a stanovit priority, nikoli posuzovat v této fázi přijatelnost určitého poškození. Pro spotřebitele bude obtížně přijatelné každé poškození zdraví, kterému by se dalo snadno zabránit. Je ovšem opodstatněné, aby příslušné orgány vynakládaly více úsilí na předcházení nevratným následkům než dočasným nepříjemným pocitům.
Jako objektivní kritéria pro posuzování závažnosti následků (akutního poranění nebo jiné škody na zdraví) lze použít jednak rozsah lékařského zásahu a jednak důsledky pro budoucí funkční schopnosti postiženého. Oba tyto parametry je možné vyjádřit ve formě nákladů, ale náklady následků poškození zdraví mohou být obtížně vyčíslitelné.
Na základě kombinace těchto kritérií lze uvedené čtyři stupně vymezit takto:
|
1. |
Poškození zdraví nebo následek, které po základním ošetření (první pomoc, kterou obvykle neposkytuje lékař) podstatně nesnižují funkčnost ani nepůsobí nadměrnou bolest. Následky jsou obvykle zcela vratné. |
|
2. |
Poškození zdraví nebo následek, které mohou vyžadovat návštěvu úrazové ambulance nebo oddělení akutního příjmu, ale obvykle nevyžadují hospitalizaci. Funkčnost může být snížená po určitou dobu, která však nepřesahuje přibližně 6 měsíců, a uzdravení je víceméně úplné. |
|
3. |
Poškození zdraví nebo následek, které obvykle vyžadují hospitalizaci a snižují funkčnost na dobu delší než 6 měsíců nebo vedou k trvalé ztrátě funkce. |
|
4. |
Poškození zdraví nebo následek, které jsou nebo mohou být smrtelné, včetně smrti mozku; následky postihující reprodukční schopnost nebo potomky; závažné postižení (ztráta) končetin a/nebo funkce vedoucí k více než asi 10 % invaliditě. |
Níže uvedená tabulka, kterou nelze chápat jako preskriptivní či úplnou, ale spíše jako vodítko, obsahuje příklady všech čtyř stupňů poškození zdraví. V tomto ohledu mohou existovat rozdíly mezi zeměmi, které jsou dány kulturně nebo odlišnými systémy zdravotní péče a odlišnými finančními úpravami. Nicméně odchylky od klasifikace navržené v tabulce budou mít vliv na jednotnost posuzování rizik v EU. Proto by měly být ve zprávě o posouzení rizik jasně uvedeny a vysvětleny, včetně odůvodnění.
|
Druh poškození zdraví |
Závažnost poškození zdraví |
|||
|
1 |
2 |
3 |
4 |
|
|
Tržné rány, řezné rány |
povrchové |
zevní (hluboké) (> 10 cm dlouhé na těle) (> 5 cm dlouhé na obličeji), vyžadující sešití šlacha nebo zasažení kloubu oční bělmo nebo rohovka |
optický nerv krční tepna průdušnice vnitřní orgány |
průdušnice jícen aorta mícha (spodní část) hluboké tržné rány na vnitřních orgánech přerušení míchy v horní části mozek (těžká léze/ dysfunkce) |
|
Pohmoždění (odření/kontuze, otok, edém) |
povrchové ≤ 25 cm2 na obličeji ≤ 50 cm2 na těle |
závažné > 25 cm2 na obličeji > 50 cm2 na těle |
průdušnice vnitřní orgány (lehké poškození) srdce mozek plíce, krev nebo vzduch v hrudní dutině |
mozkový kmen poškození míchy vedoucí k ochrnutí |
|
Otřes mozku |
— |
velmi krátké bezvědomí (minuty) |
delší bezvědomí |
kóma |
|
Zachycení/skřípnutí |
lehké skřípnutí |
— |
(viz, v závislosti na případu, konečné důsledky pohmoždění, rozdrcení, zlomenin, vykloubení či amputace) |
(stejné důsledky jako u dušení/škrcení) |
|
Vyvrtnutí, natažení, muskuloskeletální porucha |
končetiny klouby páteř (žádné vykloubení ani zlomenina) |
natažení kolenních vazů |
natržení/přetržení vazu nebo šlachy natržení svalu hyperflexe krku |
— |
|
Vykloubení/dislokace |
— |
končetiny (prst na ruce nebo na noze, ruka, chodidlo) loket čelist uvolnění zubu |
kotník zápěstí rameno kyčel koleno páteř |
páteř |
|
Zlomenina |
— |
končetiny (prst na ruce nebo na noze, ruka, chodidlo) zápěstí paže žebro hrudní kost nos zub čelist kosti okolo očí |
kotník noha (stehenní kost, lýtková a holenní kost) kyčel stehno lebka páteř (lehká kompresní zlomenina) čelist (těžká zlomenina) hrtan Zlomeniny několika žeber Krev nebo vzduch v hrudní dutině |
krk páteř |
|
Rozdrcení |
— |
— |
končetiny (prsty na ruce nebo na noze, ruka, chodidlo) loket kotník zápěstí předloktí noha rameno průdušnice hrtan pánev |
mícha střední nebo spodní část krku hrudník (rozsáhlé rozdrcení) mozkový kmen |
|
Amputace |
— |
— |
prst(y) na rukou prst(y) na nohou ruka chodidlo (část) paže noha oko |
obě končetiny |
|
Bodnutí, propíchnutí |
omezená hloubka, zasažena pouze kůže |
hlubší než kůže břišní stěna (bez zasažení orgánů) |
oko vnitřní orgány hrudní stěna |
aorta srdce průdušnice hluboká poranění orgánů (játra, ledviny, střeva atd.) |
|
Požití |
— |
— |
poranění vnitřních orgánů (viz též zablokování vnitřních dýchacích cest v případě, že se spolknutý předmět zachytil vysoko v jícnu) |
trvalé poškození vnitřního orgánu |
|
Zablokování vnitřních dýchacích cest |
— |
— |
přerušení přívodu kyslíku do mozku bez trvalých následků |
přerušení přívodu kyslíku do mozku s trvalými následky |
|
Dušení/škrcení |
— |
— |
přerušení přívodu kyslíku do mozku bez trvalých následků |
udušení/uškrcení |
|
Ponoření/utonutí |
— |
— |
— |
utonutí |
|
Popálení/opaření (horko, chlad nebo chemická látka) |
1. stupeň, až 100 % povrchu těla 2. stupeň, < 6 % povrchu těla |
2. stupeň, 6–15 % povrchu těla |
2. stupeň, 16–35 % povrchu těla nebo 3. stupeň až 35 % povrchu těla inhalační popálení |
2. nebo 3. stupeň, > 35 % povrchu těla inhalační popálení vyžadující podporu dýchání |
|
Úraz elektrickým proudem |
(viz též popálení, protože elektrický proud může způsobit popáleniny) |
lokální účinky (přechodné křeče nebo ochrnutí svalů) |
— |
zásah elektrickým proudem |
|
Neurologické poruchy |
— |
— |
vyvolaný epileptický záchvat |
— |
|
Poranění oka, cizí těleso v oku |
přechodná bolest oka nevyžadující léčbu |
přechodná ztráta zraku |
částečná ztráta zraku trvalá ztráta zraku (jedno oko) |
trvalá ztráta zraku (obě oči) |
|
Poškození sluchu, cizí těleso v uchu |
přechodná bolest v uchu nevyžadující léčbu |
přechodné zhoršení sluchu |
částečná ztráta sluchu úplná ztráta sluchu (jedno ucho) |
úplná ztráta sluchu (obě uši) |
|
Otrava látkami (požití, vdechnutí, kontakt s kůží) |
průjem, zvracení, lokální příznaky |
vratné poškození vnitřních orgánů, např. jater či ledvin, lehká hemolytická anémie |
nevratné poškození vnitřních orgánů, např. jícnu, žaludku, jater či ledvin, hemolytická anémie, vratné poškození nervové soustavy |
nevratné poškození nervové soustavy smrt |
|
Podráždění, dermatitida, zánět nebo žíravé účinky látek (vdechnutí, kontakt s kůží) |
lehké lokální podráždění |
vratné poškození oka vratné systémové účinky zánětlivé účinky |
plíce, dechová nedostatečnost, chemická pneumonie nevratné systémové účinky částečná ztráta zraku žíravé účinky |
plíce, poškození vyžadující podporu dýchání asfyxie |
|
Alergická reakce nebo senzibilizace |
lehká nebo lokální alergická reakce |
alergická reakce, rozsáhlá alergická kontaktní dermatitida |
silná senzibilizace vyvolávající alergii na více látek |
anafylaktická reakce, šok smrt |
|
Dlouhodobé poškození ze styku s látkami nebo z expozice záření |
průjem, zvracení, lokální příznaky |
vratné poškození vnitřních orgánů, např. jater či ledvin, lehká hemolytická anémie |
poškození nervové soustavy, např. organický psychosyndrom (nazývaný také chronická toxická encefalopatie, známý též jako „nemoc malířů“); nevratné poškození vnitřních orgánů, např. jícnu, žaludku, jater či ledvin, hemolytická anémie, vratné poškození nervové soustavy |
rakovina (leukémie) účinky na reprodukci účinky na potomky deprese centrální nervové soustavy |
|
Mikrobiologická infekce |
|
vratné poškození |
nevratné účinky |
infekce vyžadující dlouhodobou hospitalizaci, organismy rezistentní vůči antibiotikům smrt |
Tabulka 4
Úroveň rizika daná kombinací závažnosti poškození zdraví a pravděpodobnosti
|
Pravděpodobnost poškození během předpokládané životnosti výrobku |
Závažnost poškození zdraví |
||||
|
1 |
2 |
3 |
4 |
||
|
vysoká
nízká |
> 50 % |
H |
S |
S |
S |
|
> 1/10 |
M |
S |
S |
S |
|
|
> 1/100 |
M |
S |
S |
S |
|
|
> 1/1 000 |
L |
H |
S |
S |
|
|
> 1/10 000 |
L |
M |
H |
S |
|
|
> 1/100 000 |
L |
L |
M |
H |
|
|
> 1/1 000 000 |
L |
L |
L |
M |
|
|
< 1/1 000 000 |
L |
L |
L |
L |
|
|
S – vážné riziko H – vysoké riziko M – střední riziko L – nízké riziko |
Terminologický glosář
Nebezpečí/nebezpečnost (hazard): zdroj nebezpečí (danger) zahrnující možnost zranění nebo jiného poškození zdraví. Prostředkem ke kvantifikaci nebezpečí v rámci posouzení rizik je závažnost možného zranění nebo poškození zdraví.
Nebezpečí výrobku: nebezpečí dané vlastnostmi výrobku.
Riziko: vyvážená kombinace nebezpečí a pravděpodobnosti, že dojde k poškození. Rizikem se nepopisuje nebezpečí ani pravděpodobnost, nýbrž oboje současně.
Posouzení rizik: postup zjišťování a posuzování nebezpečí, sestávající ze tří kroků:
|
1. |
zjištění závažnosti nebezpečí; |
|
2. |
určení pravděpodobnosti, že toto nebezpečí způsobí poškození zdraví spotřebitele; |
|
3. |
kombinace nebezpečí a pravděpodobnosti. |
Úroveň rizika: stupeň rizika; může jít o „vážné“, „vysoké“, „střední“ nebo „nízké“ riziko. Jakmile je stanovena (nejvyšší) úroveň rizika, je posouzení rizik hotové.
Řízení rizik: následná opatření, odlišná od posouzení rizik, jejichž cílem je snížit nebo odstranit riziko.
(1) Na jiných místech v těchto pokynech se výrazem „Komise“ obvykle označuje tým odpovědný za systém RAPEX zřízený v rámci útvaru Komise odpovědného za provádění směrnice 2001/95/ES, případně příslušné útvary Komise.
(2) Informační a komunikační systém pro dozor nad trhem („ICSMS“). Cílem této platformy je usnadnit komunikaci mezi subjekty dozoru nad trhem v EU a zemích ESVO, pokud jde o nevyhovující výrobky.
(3) Viz nejnovější prováděcí rozhodnutí ES zveřejněné na stránkách https://ec.europa.eu/consumers/consumers_safety/safety_products/rapex/alerts/repository/content/pages/rapex/index_en.htm
(4) V tomto dokumentu se pojem „členské státy“ musí vykládat v tom smyslu, že nevylučuje možnost, aby byla ustanovení obsažená v těchto pokynech určena také všem dalším aktérům.
(5) Viz 10. bod odůvodnění směrnice 2001/95/ES.
(6) Nařízení Evropského parlamentu a Rady (ES) č. 178/2002 ze dne 28. ledna 2002, kterým se stanoví obecné zásady a požadavky potravinového práva, zřizuje se Evropský úřad pro bezpečnost potravin a stanoví postupy týkající se bezpečnosti potravin (Úř. věst. L 31, 1.2.2002, s. 1).
(7) Směrnice Evropského parlamentu a Rady 2001/83/ES ze dne 6. listopadu 2001 o kodexu EU týkajícím se humánních léčivých přípravků (Úř. věst. L 311, 28.11.2001, s. 67).
(8) Směrnice Evropského parlamentu a Rady 2001/82/ES ze dne 6. listopadu 2001 o kodexu EU týkajícím se veterinárních léčivých přípravků (Úř. věst. L 311, 28.11.2001, s. 1).
(9) Nařízení Evropského parlamentu a Rady (EU) 2017/745 ze dne 5. dubna 2017 o zdravotnických prostředcích, změně směrnice 2001/83/ES, nařízení (ES) č. 178/2002 a nařízení (ES) č. 1223/2009 a o zrušení směrnic Rady 90/385/EHS a 93/42/EHS (Úř. věst. L 117, 5.5.2017, s. 1).
(10) Směrnice Rady 90/385/EHS ze dne 20. června 1990 o sbližování právních předpisů členských států týkajících se aktivních implantabilních zdravotnických prostředků (Úř. věst. L 189, 20.7.1990, s. 17).
(11) Směrnice Evropského parlamentu a Rady 2015/1535/EU ze dne 9. září 2015 o postupu při poskytování informací v oblasti technických předpisů a předpisů pro služby informační společnosti (Úř. věst. L 241, 17.9.2015, s. 1).
(12) Viz obecná metodika EU pro posuzování rizik (opatření č. 5 víceletého akčního plánu pro dozor nad výrobky v EU (COM(2013) 76)), která poskytuje poradenství orgánům v souvislosti s čl. 20 odst. 2 nařízení (ES) č. 765/2008: http://ec.europa.eu/DocsRoom/documents/17107/attachments/1/translations
(13) Viz https://ec.europa.eu/consumers/consumer-safety/rag/#/screen/home
(14) www.ec.europa.eu/rapex
(15) Viz část I kapitola 6.2 těchto pokynů.
(16) Viz část II kapitola 2.2.1 těchto pokynů.
(17) Viz část II kapitola 2.2.1 těchto pokynů.
(18) Viz část II kapitola 2.2.2 těchto pokynů.
(19) Viz část II kapitola 2.2.2 těchto pokynů.
(20) Pro více informací o následných akcích viz část II kapitola 4.4.5 těchto pokynů.
(21) Pro více informací o oznámeních, u nichž jsou bezpečnostní hlediska předmětem diskuse na úrovni EU, viz část II kapitoly 3.4.4 a 3.4.7.1.1 těchto pokynů.
(22) Viz bod 10 přílohy II směrnice 2001/95/ES.
(23) Viz bod 9 přílohy II směrnice 2001/95/ES.
(24) Pro více informací o oznámeních o bezpečnostních hlediscích, která jsou předmětem diskuse na úrovni EU, viz část II kapitola 3.1.2 písm. d) a 3.4.7.1.1.
(25) https://ec.europa.eu/consumers/consumers_safety/safety_products/rapex/alerts/?event=main.search.
(26) Postup dohodnutý již výborem zřízeným směrnicí o obecné bezpečnosti výrobků dne 24. září 2012, o němž byla kontaktní místa RAPEX informována na zasedání kontaktních míst RAPEX dne 4. října (bod jednání 4) a který se uplatňuje od roku 2013.
(27) Ustanovení čl. 16 odst. 1 směrnice 2001/95/ES a čl. 23 odst. 3 v souvislosti s čl. 19 odst. 5 nařízení (ES) č. 765/2008.
(28) Ustanovení čl. 16 odst. 1 a 2 směrnice 2001/95/ES.
(29) Pro více informací o kritériích oznamování viz část I kapitola 2.
(30) Pro více informací o oznámeních zasílaných prostřednictvím aplikace RAPEX před přijetím opatření viz kapitola 3.1.2 písm. b).
(31) Pro více informací o oznámeních o bezpečnostních hlediscích, která jsou předmětem diskuse na úrovni EU, viz část II kapitola 3.1.2 písm. d) a kapitola 3.4.4.
(32) Pro více informací o lhůtách viz část III dodatek 4 těchto pokynů.
(33) Všechny lhůty uvedené v těchto pokynech jsou vyjádřeny v kalendářních dnech.
(34) Viz bod 10 přílohy II směrnice 2001/95/ES.
(35) Pro účely těchto pokynů se „hospodářským subjektem“ rozumí jakákoli fyzická nebo právnická osoba definovaná jako „hospodářský subjekt“ v nařízení (ES) č. 765/2008 nebo jako „výrobce“ a „distributor“ ve směrnici o obecné bezpečnosti výrobků.
(36) https://webgate.ec.europa.eu/etranslation/translateDocument.html
(37) Oznámení není třeba zasílat prostřednictvím stálého zastoupení členského státu při EU.
(38) Viz část I kapitola 5.3 těchto pokynů.
(39) Kolonky obsažené ve vzoru mohou být aktualizovány na základě vývoje dohodnutého mezi Komisí a členskými státy.
(40) Kolonky obsažené ve vzoru mohou být aktualizovány na základě vývoje dohodnutého mezi Komisí a členskými státy.
(41) Další informace o metodě posuzování rizik u harmonizovaných výrobků (jak u spotřebních, tak u profesionálních výrobků) ve vztahu k širším kategoriím rizik pro veřejné zájmy chráněné harmonizovanými právními předpisy EU, viz část I kapitola 5.3.
(42) Benis HG (1990): A Product Risk Assessment Nomograph (Nomogram pro posouzení rizikovosti výrobků). Zpráva vypracovaná pro Ministerstvo pro záležitosti spotřebitelů Nového Zélandu z února 1990. Citováno v: Evropská komise (2005): Establishing a Comparative Inventory of Approaches and Methods Used by Enforcement Authorities for the Assessment of the Safety of Consumer Products Covered by Directive 2001/95/EC on General Product Safety and Identification of Best Practices. Zpráva vypracovaná společností Risk & Policy Analysts (RPA), Loddon, Norfolk, Spojené království.
(43) Metoda používaná belgickými orgány. Citováno v: Evropská komise (2005): Establishing a Comparative Inventory of Approaches and Methods Used by Enforcement Authorities for the Assessment of the Safety of Consumer Products Covered by Directive 2001/95/EC on General Product Safety and Identification of Best Practices. Zpráva vypracovaná společností Risk & Policy Analysts (RPA), Loddon, Norfolk, Spojené království.
(44) Rozhodnutí Komise 2004/418/ES ze dne 29. dubna 2004, kterým se stanoví pokyny pro řízení systému EU pro rychlou výměnu informací (RAPEX) a pro oznámení předkládaná v souladu s článkem 11 směrnice 2001/95/ES (Úř. věst. L 151, 30.4.2004, s. 83).
(45) Směrnice 2001/95/ES.
(46) https://webgate.ec.europa.eu/idbpa/.
Pozn.: Při srovnávání výsledku zkoušky s mezní hodnotou je vždy třeba brát v úvahu nejistotu. Viz například:
|
— |
„Report on the relationship between analytical results, measurement uncertainty, recovery factors and the provisions of EU food and feed legislation …“ (Zpráva o vztahu mezi výsledky analýz, nejistotou měření, faktory výtěžnosti a ustanoveními právních předpisů EU týkajících se potravin a krmiv) https://ec.europa.eu/food/safety/chemical_safety/contaminants/catalogue_en |
|
— |
souhrnná zpráva „Preparation of a working document in support of the uniform interpretation of legislative standards and the laboratory quality standards prescribed under Directive 93/99/EEC“ (Příprava pracovního dokumentu na podporu jednotného výkladu legislativních norem a norem jakosti pro laboratoře předepsaných podle směrnice 93/99/EHS). http://ec.europa.eu/food/fs/scoop/9.1_sr_en.pdf |
(48) Nařízení Evropského parlamentu a Rady (ES) č. 1907/2006 ze dne 18. prosince 2006 o registraci, hodnocení, povolování a omezování chemických látek, o zřízení Evropské agentury pro chemické látky, o změně směrnice 1999/45/ES a o zrušení nařízení Rady (EHS) č. 793/93, nařízení Komise (ES) č. 1488/94, směrnice Rady 76/769/EHS a směrnic Komise 91/155/EHS, 93/67/EHS, 93/105/ES a 2000/21/ES (Úř. věst. L 396, 30.12.2006, s. 1).
(49) Úř. věst. L 164, 26.6.2009, s. 7.
(50) Norma EN 71-1:2005, oddíl 8.2 +A6:2008.
(51) Článek 10 nařízení (ES) č. 1223/2009 (Úř. věst. L 342, 22.12.2009, s. 59).
(52) Nařízení REACH a pokyny k nařízení REACH, které jsou k dispozici na adrese http://echa.europa.eu/. Evropská agentura pro chemické látky (2008). Pokyn pro požadavky na informace a hodnocení chemické bezpečnosti: http://guidance.echa.europa.eu/docs/guidance_document/information_requirements_en.htm
(53) Prováděcí rozhodnutí Komise 2013/674/EU ze dne 25. listopadu 2013 o pokynech k příloze I nařízení Evropského parlamentu a Rady (ES) č. 1223/2009 o kosmetických přípravcích (Úř. věst. L 315, 26.11.2013, s. 82); Vědecký výbor pro spotřební zboží (SCCP): SCCP's Notes of Guidance for the Testing of Cosmetic Ingredients and their Safety Evaluation (Pokyny SCCP pro zkoušky kosmetických přísad a posuzování jejich bezpečnosti), 9. revize, 29.9.2015, SCCS/1564/15, revize ze dne 25. dubna 2016: http://ec.europa.eu/health/scientific_committees/consumer_safety/docs/sccs_o_190.pdf
(54) Viz část I kapitola 1.1 předposlední odstavec.
(55) Formulace je převzata z definice „bezpečného výrobku“ v čl. 2 písm. b) směrnice 2001/95/ES.
