2013/49/EU2013/49/EU: Prováděcí rozhodnutí Komise ze dne 22. ledna 2013 , kterým se povoluje uvedení syntetického zeaxanthinu na trh jako nové složky potravin podle nařízení Evropského parlamentu a Rady (ES) č. 258/97 (oznámeno pod číslem C(2013) 110)
| Publikováno: | Úř. věst. L 21, 24.1.2013, s. 32-33 | Druh předpisu: | Prováděcí rozhodnutí |
| Přijato: | 22. ledna 2013 | Autor předpisu: | Evropská komise |
| Platnost od: | 24. ledna 2013 | Nabývá účinnosti: | 24. ledna 2013 |
| Platnost předpisu: | Ano | Pozbývá platnosti: | |
Text předpisu s celou hlavičkou je dostupný pouze pro registrované uživatele.
PROVÁDĚCÍ ROZHODNUTÍ KOMISE
ze dne 22. ledna 2013,
kterým se povoluje uvedení syntetického zeaxanthinu na trh jako nové složky potravin podle nařízení Evropského parlamentu a Rady (ES) č. 258/97
(oznámeno pod číslem C(2013) 110)
(Pouze nizozemské znění je závazné)
(2013/49/EU)
EVROPSKÁ KOMISE,
s ohledem na Smlouvu o fungování Evropské unie,
s ohledem na nařízení Evropského parlamentu a Rady (ES) č. 258/97 ze dne 27. ledna 1997 o nových potravinách a nových složkách potravin (1), a zejména na článek 7 uvedeného nařízení,
vzhledem k těmto důvodům:
|
(1) |
Dne 1. června 2004 podala společnost DSM Nutritional Products VML příslušným nizozemským orgánům žádost o uvedení syntetického zeaxanthinu na trh jako nové složky potravin. |
|
(2) |
Dne 16. června 2005 vydal příslušný nizozemský subjekt pro posuzování potravin svou zprávu o prvním posouzení. V této zprávě dospěl k závěru, že syntetický zeaxanthin nepředstavuje při maximálním příjmu nejvýše 20 mg na osobu a na den významné riziko pro lidské zdraví. Dospěl však také k závěru, že posouzení bezpečnosti nemohlo být ukončeno, protože předložené údaje nebyly dostatečné. |
|
(3) |
Z toho důvodu bylo vyžádáno další posouzení. |
|
(4) |
Dne 1. srpna 2005 Komise zaslala zprávu o prvním posouzení všem členským státům s žádostí o připomínky. |
|
(5) |
Žadatel informoval Komisi dne 2. února 2007, že použití zeaxanthinu by mělo být omezeno tak, že by byl používán pouze jako složka v doplňcích stravy. |
|
(6) |
Komise konzultovala dne 20. března 2007 Evropský úřad pro bezpečnost potravin (EFSA). |
|
(7) |
Dne 24. dubna 2008 dospěl EFSA ve vědeckém stanovisku „Scientific Opinion of the safety of ‚synthetic zeaxanthin as an ingredient in food supplements‘“ (Vědecké stanovisko k bezpečnosti syntetického zeaxanthinu jako složky v doplňcích stravy) (2) k závěru, že na základě současných poznatků není možné dokázat bezpečnost syntetického zeaxanthinu jako nové složky v doplňcích stravy při navrhovaném příjmu 20 mg na osobu a na den. |
|
(8) |
Dne 25. ledna 2012 předložil žadatel doplňující informace a navrhl příjem syntetického zeaxanthinu jako složky v doplňcích stravy nejvýše 2 mg na osobu a na den. |
|
(9) |
Na základě žádosti Komise byl EFSA požádán, aby s ohledem na doplňující informace přezkoumal své stanovisko k syntetickému zeaxanthinu jako nové složce v doplňcích stravy. Dne 13. září 2012 dospěl EFSA ve svém prohlášení „Statement on the safety of synthetic zeaxanthin as an ingredient in food supplements“ (Prohlášení k bezpečnosti syntetického zeaxanthinu jako složky v doplňcích stravy) (3) k závěru, že při užití množství navrhovaného žadatelem nevznikají bezpečnostní rizika. |
|
(10) |
Na základě vědeckého posouzení se prokázalo, že syntetický zeaxanthin splňuje kritéria stanovená v čl. 3 odst. 1 nařízení (ES) č. 258/97. |
|
(11) |
Záměrné přidávání syntetického zeaxanthinu do potravin jako barvící přísady spadá do oblasti působnosti nařízení Evropského parlamentu a Rady (ES) č. 1333/2008 ze dne 16. prosince 2008 o potravinářských přídatných látkách (4) a v souladu s uvedeným nařízením by mělo být povoleno. |
|
(12) |
Opatření stanovená tímto rozhodnutím jsou v souladu se stanoviskem Stálého výboru pro potravinový řetězec a zdraví zvířat, |
PŘIJALA TOTO ROZHODNUTÍ:
Článek 1
Syntetický zeaxanthin, jak je specifikován v příloze, může být uveden na trh v Unii jako nová složka potravin pro použití v doplňcích stravy při maximálním denním příjmu nejvýše 2 mg, jak doporučuje výrobce.
Článek 2
Při označování potravin obsahujících syntetický zeaxanthin povolený tímto rozhodnutím se použije označení „syntetický zeaxanthin“.
Článek 3
Toto rozhodnutí je určeno společnosti DSM Nutritional Products, Alexander Fleminglaan 1, 2613 AX Delft, Nizozemsko.
V Bruselu dne 22. ledna 2013.
Za Komisi
Tonio BORG
člen Komise
(1) Úř. věst. L 43, 14.2.1997, s. 1.
(2) EFSA Journal (2008) 728, 1-27.
(3) EFSA Journal 2012; 10(10):2891.
(4) Úř. věst. L 354, 31.12.2008, s. 16.
PŘÍLOHA
SPECIFIKACE SYNTETICKÉHO ZEAXANTHINU
Definice Pigment zeaxanthin je přirozeně se vyskytující xanthofyl, jedná se o oxidovaný karotenoid. Syntetický zeaxanthin se připravuje vícestupňovou chemickou syntézou z menších molekul.
Syntetický zeaxanthin je nabízen buď ve formě rozprašováním sušeného prášku s želatinovým nebo škrobovým základem s přidaným α-tokoferolem a askorbylpalmitátem, nebo ve formě roztoku kukuřičného oleje s přidaným α-tokoferolem.
Popis: Oranžovočervený krystalický prášek, s lehkou nebo žádnou vůní
Chemický vzorec: C40H56O2
Strukturní vzorec:
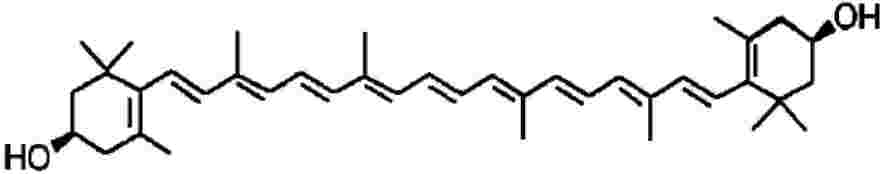
Číslo CAS: 144-68-3
Relativní molekulová hmotnost: 568,9 daltonu
Fyzikálně-chemické vlastnosti syntetického zeaxanthinu
|
Úbytek hmotnosti sušením |
méně než 0,2 % |
|
All-trans-zeaxanthin |
více než 96 % |
|
Cis-zeaxanthin |
méně než 2 % |
|
Ostatní karotenoidy |
méně než 1,5 % |
|
Trifenylfosfinoxid (č. CAS 791-28-6) |
méně než 50 mg/kg |